1 . 健康人体内含铁元素大约 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:_______ ,试剂2的化学式为_______ 。
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是_______ 。
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:_______ ,现象为_______ 。
 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验: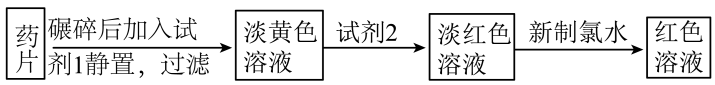
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的
 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:
您最近半年使用:0次
2 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.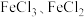 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近半年使用:0次
解题方法
3 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。日常生活中可通过食物摄入铁元素,例如黑木耳中就含有比较丰富的铁元素。某研究性学习小组为测定某地黑木耳中铁的含量,开展了如下研究与实践活动。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取 黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
【研究与实践活动二】
研究黑木耳中铁的含量:称取 黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质___________ (填“难”或“易”)溶于水。
(2)取少量滤液于试管中,滴入 溶液,溶液变红。则滤液中铁元素的存在形式有
溶液,溶液变红。则滤液中铁元素的存在形式有 、
、___________ (填离子符号)。
(3)滤液与Fe生成A的离子方程式为___________ 。
(4)由A转化为B可加入的试剂X可以是___________ (填标号)。
a.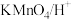 b.
b. c.
c.
(5)由C转化成D的现象:白色沉淀迅速变为灰绿色,最终变为___________ 。C转化成D的化学方程式为___________ 。
(6)将 黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到
黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到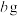 红棕色固体。若流程中加入的铁反应掉
红棕色固体。若流程中加入的铁反应掉 ,则该黑木耳中铁元素的质量分数为
,则该黑木耳中铁元素的质量分数为___________ (用含a、b、c的代数式表示)。
【研究与实践活动一】
研究黑木耳中含铁物质的水溶性:称取
 黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。
黑木耳,洗净切碎,用蒸馏水浸泡后取浸泡液进行铁元素检测,结果未能检测到铁元素。【研究与实践活动二】
研究黑木耳中铁的含量:称取
 黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。
黑木耳,高温灼烧使之完全灰化,按如下流程对得到的黑木耳灰进行处理。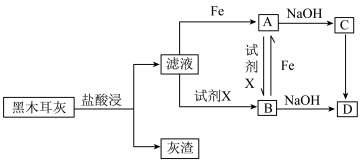
(1)浸泡液中未能检测到铁元素,说明黑木耳中的含铁物质
(2)取少量滤液于试管中,滴入
 溶液,溶液变红。则滤液中铁元素的存在形式有
溶液,溶液变红。则滤液中铁元素的存在形式有 、
、(3)滤液与Fe生成A的离子方程式为
(4)由A转化为B可加入的试剂X可以是
a.
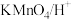 b.
b. c.
c.
(5)由C转化成D的现象:白色沉淀迅速变为灰绿色,最终变为
(6)将
 黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到
黑木耳中的铁元素经流程A→C→D进行完全转化,将D经过一系列处理,得到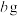 红棕色固体。若流程中加入的铁反应掉
红棕色固体。若流程中加入的铁反应掉 ,则该黑木耳中铁元素的质量分数为
,则该黑木耳中铁元素的质量分数为
您最近半年使用:0次
4 . 以化合价为纵坐标,物质类别为横坐标的图像称为价类二维图.在地壳中的金属含量仅次于铝的某元素价类二维图如图所示,下列说法错误的是
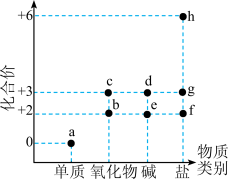

| A.a与水常温下几乎不发生反应,但在高温下可发生置换反应 |
B. 和 和 可分别与水发生反应生成 可分别与水发生反应生成 和 和 |
C.e在潮湿的空气中容易转变为 |
D. 的某种盐可以用作净水剂 的某种盐可以用作净水剂 |
您最近半年使用:0次
名校
解题方法
5 . 如表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑩回答下列问题。
(1)元素①和②的单质化合形成的化合物 中,H元素的化合价为
中,H元素的化合价为___________ , 能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为___________ 。
(2)由元素①和⑥形成的一种物质是天然气的主要成分,其化学式为___________ ;元素⑥还可以和⑧形成一种三原子直线形分子,其结构式为___________ ;元素②的单质在元素⑦的单质中点燃生成淡黄色固体,将该固体投入硫酸亚铁溶液中,预测主要的反应现象是___________ 。
(3)元素③、⑧、⑨的简单离子中半径最大的是___________ ;(填离子符号),元素②和⑤的最高价氧化物对应的水化物之间可以发生反应,其反应的离子方程式为___________ 。
| 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ⑤ | ⑧ | ⑨ | ||||
| 4 | ③ | ④ | ⑩ | |||||
(1)元素①和②的单质化合形成的化合物
 中,H元素的化合价为
中,H元素的化合价为 能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为(2)由元素①和⑥形成的一种物质是天然气的主要成分,其化学式为
(3)元素③、⑧、⑨的简单离子中半径最大的是
您最近半年使用:0次
6 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价-类”二维图。铁元素的“价-类”二维图如图所示,下列说法正确的是


| A.Fe3+转化为Fe2+,可以通过化合反应实现 |
| B.Fe3O4中铁元素为+4价 |
| C.Fe(OH)2在空气中受热,可分解为FeO |
| D.工业上用CO还原Fe2O3炼铁,该反应为置换反应 |
您最近半年使用:0次
解题方法
7 . 某工厂酸性废液中含有 、
、 、
、 、
、 、
、 ,以该废液为原料制备
,以该废液为原料制备 的工艺流程如下(部分操作和反应条件略):
的工艺流程如下(部分操作和反应条件略):
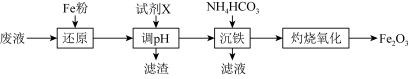
已知:加入试剂X调节pH使 生成沉淀。
生成沉淀。
回答下列问题:
(1)写出“还原”步骤中反应的离子方程式:_____________ 、_________________ 。
(2)若加入Fe粉过量,取少量调节pH过滤后得到的滤液,加入NaOH溶液的现象为_____________ ,请写出沉淀颜色发生变化的化学方程式:_________________________ 。
(3)“沉铁”过程中有 沉淀和气体生成,写出该反应的离子方程式:
沉淀和气体生成,写出该反应的离子方程式:_________________ ; 在空气中经“灼烧氧化”生成
在空气中经“灼烧氧化”生成 ,试写出“灼烧氧化”的化学方程式:
,试写出“灼烧氧化”的化学方程式:____________________ 。
 、
、 、
、 、
、 、
、 ,以该废液为原料制备
,以该废液为原料制备 的工艺流程如下(部分操作和反应条件略):
的工艺流程如下(部分操作和反应条件略):
已知:加入试剂X调节pH使
 生成沉淀。
生成沉淀。回答下列问题:
(1)写出“还原”步骤中反应的离子方程式:
(2)若加入Fe粉过量,取少量调节pH过滤后得到的滤液,加入NaOH溶液的现象为
(3)“沉铁”过程中有
 沉淀和气体生成,写出该反应的离子方程式:
沉淀和气体生成,写出该反应的离子方程式: 在空气中经“灼烧氧化”生成
在空气中经“灼烧氧化”生成 ,试写出“灼烧氧化”的化学方程式:
,试写出“灼烧氧化”的化学方程式:
您最近半年使用:0次
名校
解题方法
8 . 有人设计出一种在隔绝空气条件下让钠与 溶液反应,观察
溶液反应,观察 颜色的实验。实验时,往
颜色的实验。实验时,往 的大试管中先加
的大试管中先加 煤油,取
煤油,取 粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入
粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入 溶液
溶液 不含
不含 使煤油的液面至橡胶塞,并夹紧弹簧夹
使煤油的液面至橡胶塞,并夹紧弹簧夹 如图所示
如图所示 。下列说法错误的是
。下列说法错误的是

 溶液反应,观察
溶液反应,观察 颜色的实验。实验时,往
颜色的实验。实验时,往 的大试管中先加
的大试管中先加 煤油,取
煤油,取 粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入
粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入 溶液
溶液 不含
不含 使煤油的液面至橡胶塞,并夹紧弹簧夹
使煤油的液面至橡胶塞,并夹紧弹簧夹 如图所示
如图所示 。下列说法错误的是
。下列说法错误的是

| A.长颈漏斗中的液面上升 |
| B.大试管下层溶液出现白色沉淀,并可持续较长时间 |
| C.用过氧化钠代替钠也可以观察到此现象 |
| D.该反应同时也能说明钠不能与硫酸亚铁溶液发生置换反应 |
您最近半年使用:0次
2023-10-05更新
|
241次组卷
|
4卷引用:安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题
安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题广东省东莞市东莞中学松山湖学校2023-2024学年高一上学期期中考试化学试卷(已下线)专题03 铁 金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷
名校
解题方法
9 . 各物质间的转化关系如下图所示,请完成下列空白。
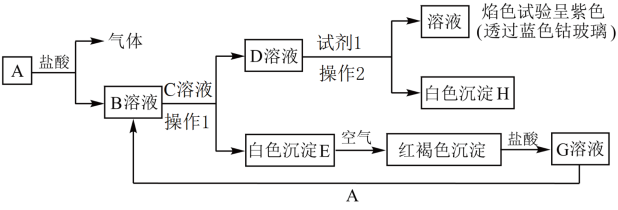
(1)A元素是_______ 。(填元素符号)
(2)C溶液中溶质的电子式为_______ 。
(3)操作1和操作2操作名称是_______ 。
(4)试剂1的化学式为_______ 。
(5)检验G溶液中阳离子的试剂是_______ 。
(6)写出E转化为红褐色沉淀的化学方程式:_______ 。
(7)写出向G溶液中加入A后的离子方程式:_______ 。

(1)A元素是
(2)C溶液中溶质的电子式为
(3)操作1和操作2操作名称是
(4)试剂1的化学式为
(5)检验G溶液中阳离子的试剂是
(6)写出E转化为红褐色沉淀的化学方程式:
(7)写出向G溶液中加入A后的离子方程式:
您最近半年使用:0次
名校
解题方法
10 . 某固体含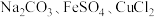 中的一种或几种。现进行如下实验:
中的一种或几种。现进行如下实验:
①向固体混合物中加水并不断搅拌,固体完全溶解;
②向溶液中加入过量铁粉,充分反应后铁粉变少,同时有红色物质析出,过滤;
③向所得滤液中加入 溶液至过量,开始时有白色沉淀生成,沉淀很快变为灰绿色,最终变为红褐色。
溶液至过量,开始时有白色沉淀生成,沉淀很快变为灰绿色,最终变为红褐色。
下列说法错误的是
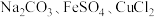 中的一种或几种。现进行如下实验:
中的一种或几种。现进行如下实验:①向固体混合物中加水并不断搅拌,固体完全溶解;
②向溶液中加入过量铁粉,充分反应后铁粉变少,同时有红色物质析出,过滤;
③向所得滤液中加入
 溶液至过量,开始时有白色沉淀生成,沉淀很快变为灰绿色,最终变为红褐色。
溶液至过量,开始时有白色沉淀生成,沉淀很快变为灰绿色,最终变为红褐色。下列说法错误的是
A.原固体中一定有 | B.原固体中不一定有 |
C.原固体中可能有 | D.实验③中既有复分解反应,也有化合反应 |
您最近半年使用:0次
2023-09-10更新
|
139次组卷
|
2卷引用:安徽省蚌埠市固镇县第二中学2023-2024学年高三上学期第三次月考化学试题



