解题方法
1 . 长期放置的FeSO4溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶FeSO4溶液进行了如表实验。
I.分别取2mL新制的FeSO4溶液于两支试管中,进行如图实验。
(1)实验i中,现象a是___________ 。
(2)写出实验ii中酸性双氧水参与反应的的离子方程式:___________ 。
II.久置的FeSO4溶液。
(3)为证明FeSO4溶液部分变质,实验iv操作是___________ 。
(4)小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验v。
由实验v能否得出___________ (填“能”或“否”)“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由___________ 。
I.分别取2mL新制的FeSO4溶液于两支试管中,进行如图实验。
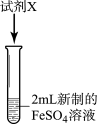 | 实验 | 试剂X | 实验现象 |
| 实验i | 1mL1mol/LNaOH溶液 | 现象a | |
| 实验ii | 依次加入5滴KSCN溶液、5滴酸性双氧水 | 现象b:加入KSCN后无明显现象,加入双氧水后溶液变成红色 |
(1)实验i中,现象a是
(2)写出实验ii中酸性双氧水参与反应的的离子方程式:
II.久置的FeSO4溶液。
| 实验操作 | 实验现象 | 实验结论 | |
| 实验iii | 取少量久置的FeSO4溶液于试管中,向其中滴加5滴KSCN溶液 | 溶液变红 | FeSO4溶液部分变质 |
| 实验iv | |||
(3)为证明FeSO4溶液部分变质,实验iv操作是
(4)小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验v。
| 实验操作 | 实验现象 | |
| 实验v | 取一定量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性KMnO4溶液 | 紫色褪去 |
由实验v能否得出
您最近半年使用:0次
2 . “金相玉振”学习小组设计如图实验装置(部分夹持装置已略去)制取氯酸钾并进行氯气性质探究实验。
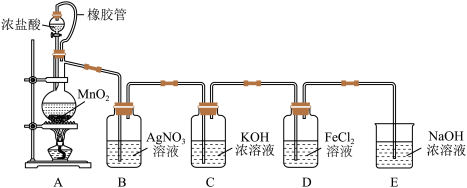
请回答:
(1)装置A中制取 的离子反应方程式是
的离子反应方程式是______ 。
(2)装置B中溶液变浑浊,______ (填“能”或“不能”)说明 与
与 溶液发生反应生成
溶液发生反应生成 ,理由是
,理由是______ 。
(3)装置C中制取氯酸钾的化学方程式为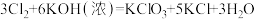 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是______ 。
(4)装置D中导管接错,若导致溶液进入装置E,则E中出现的现象是______ 。
(5)装置D改为“长管进短管出”后,装置E中仍然存在的一处明显错误是______ 。

请回答:
(1)装置A中制取
 的离子反应方程式是
的离子反应方程式是(2)装置B中溶液变浑浊,
 与
与 溶液发生反应生成
溶液发生反应生成 ,理由是
,理由是(3)装置C中制取氯酸钾的化学方程式为
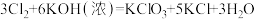 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是(4)装置D中导管接错,若导致溶液进入装置E,则E中出现的现象是
(5)装置D改为“长管进短管出”后,装置E中仍然存在的一处明显错误是
您最近半年使用:0次
解题方法
3 . 各物质的转化关系如下图所示,请完成下列空白。
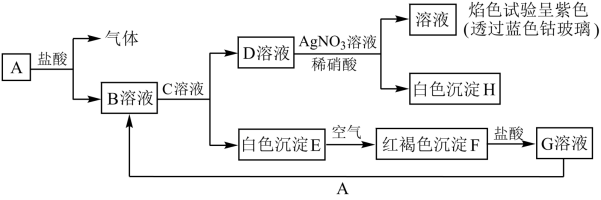
(1)写出B和D 的化学式:B___________ ;D___________ 。
(2)写出E F的化学方程式:
F的化学方程式:___________ 。
(3)向G溶液中加入A,写出反应的离子方程式___________ 。
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子___________ 。

(1)写出B和D 的化学式:B
(2)写出E
 F的化学方程式:
F的化学方程式:(3)向G溶液中加入A,写出反应的离子方程式
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子
您最近半年使用:0次
4 . 下列化合物中不能由化合反应直接制得的是
| A.CuCl2 | B.FeCl2 | C.Fe(OH)2 | D.Fe(OH)3 |
您最近半年使用:0次
解题方法
5 . 请回答下列问题:
(1)氯原子的最外层电子数为___________ ;其最高价氧化物的化学式是___________ 。
(2)维生素 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有___________ 性(填“还原”或“氧化”)。
(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式___________ 。
(1)氯原子的最外层电子数为
(2)维生素
 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式
您最近半年使用:0次
6 . 以下流程中涉及的物质均为中学化学常见物质,其中白色固体A为一种常见的钠盐,混合气体C可使澄清石灰水变浑浊,白色固体F在空气中易迅速变为灰绿色,黑色固体H有磁性。

请回答下列问题:
(1)白色固体E的化学式为___________ ;黑色固体H的化学式为___________ ;无色气体I的化学式为___________ 。
(2)无色混合气体C的组成为___________ 。
(3)白色固体A与少量澄清石灰水反应的离子方程式为___________ 。
(4)白色固体F无氧常温条件下分解的化学方程式为___________ 。
(5)请设计实验验证黑色固体H中金属元素的化合价___________ 。

请回答下列问题:
(1)白色固体E的化学式为
(2)无色混合气体C的组成为
(3)白色固体A与少量澄清石灰水反应的离子方程式为
(4)白色固体F无氧常温条件下分解的化学方程式为
(5)请设计实验验证黑色固体H中金属元素的化合价
您最近半年使用:0次
7 . 下列说法正确的是
| A.FeSO4和Fe(OH)3可以通过化合反应生成 |
| B.50mL0.5mol/LKCl溶液中的Cl-浓度小于100mL0.2mol/LMgCl2溶液 |
| C.将Na、Mg各0.2mol分别与含0.1molHCl的盐酸反应,产生气体体积比为1∶1 |
| D.将40gNaOH固体溶于1L水,所得NaOH溶液物质的量浓度为1mol/L |
您最近半年使用:0次
解题方法
8 . 回答下列问题
(1)危化品仓库的金属钠着火不能用水浇灭,可以用___________ 灭火。
(2)碳酸氢钠( )是一种重要的化工原料,1791年,法国化学家尼古拉斯·勒布朗(Nicolas Leblanc)制备出碳酸钠(
)是一种重要的化工原料,1791年,法国化学家尼古拉斯·勒布朗(Nicolas Leblanc)制备出碳酸钠( ),为碳酸氢钠的合成奠定了基础。写出一种利用
),为碳酸氢钠的合成奠定了基础。写出一种利用化合反应 制备 的化学反应方程式
的化学反应方程式___________ 。
(3)写出实验室制备氯气的离子方程式:___________ 。
(4)氢氧化亚铁为白色絮状沉淀,但在空气中迅速变成灰绿色,最后变成红褐色,试用化学反应方程式说明变色原理:___________ 。
(1)危化品仓库的金属钠着火不能用水浇灭,可以用
(2)碳酸氢钠(
 )是一种重要的化工原料,1791年,法国化学家尼古拉斯·勒布朗(Nicolas Leblanc)制备出碳酸钠(
)是一种重要的化工原料,1791年,法国化学家尼古拉斯·勒布朗(Nicolas Leblanc)制备出碳酸钠( ),为碳酸氢钠的合成奠定了基础。写出一种利用
),为碳酸氢钠的合成奠定了基础。写出一种利用 的化学反应方程式
的化学反应方程式(3)写出实验室制备氯气的离子方程式:
(4)氢氧化亚铁为白色絮状沉淀,但在空气中迅速变成灰绿色,最后变成红褐色,试用化学反应方程式说明变色原理:
您最近半年使用:0次
名校
解题方法
9 . 下列“类比”结果正确的是
| A.Fe和Cl2反应生成FeCl3,则Fe和Br2反应生成FeBr3 |
| B.Na在氧气中燃烧生成Na2O2,则Li在氧气中燃烧生成Li2O2 |
| C.向Na2CO3中加入少量水放出热量,则向NaHCO3中加入少量水也放出热量 |
| D.Fe(OH)3在空气中加热分解生成Fe2O3,则Fe(OH)2在空气中加热分解生成FeO |
您最近半年使用:0次
名校
解题方法
10 . 某化合物A(由三种元素构成),为了探究其组成,进行了如下实验:
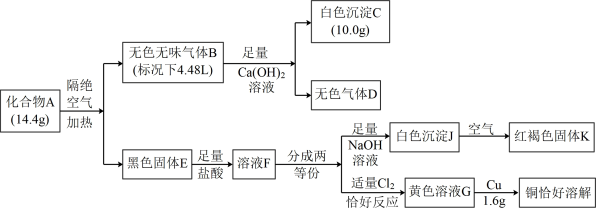
已知:气体D在标准状况下的密度为1.25g/L。试回答:
(1)无色气体D的化学式为___________ ,化合物A的化学式为___________ 。
(2)请写出白色沉淀J变成红褐色固体K的化学方程式___________ 。
(3)请写出溶液F中阳离子的检验方法___________ 。

已知:气体D在标准状况下的密度为1.25g/L。试回答:
(1)无色气体D的化学式为
(2)请写出白色沉淀J变成红褐色固体K的化学方程式
(3)请写出溶液F中阳离子的检验方法
您最近半年使用:0次



