1 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近半年使用:0次
解题方法
2 . 价类二维图是学习元素及其化合物知识的重要模型。铁元素的价类二维图如图,下列有关说法不正确的是
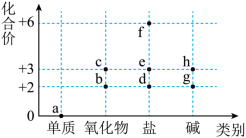
| A.a能导电,能被磁体吸引 | B.铁的氧化物只有b、c |
| C.e转化为f需加入氧化剂 | D.物质g在空气中不能长时间稳定存在 |
您最近半年使用:0次
3 . 高铁酸钾(K2FeO4)是一种高效、无毒的强氧化剂。在工业上,一种通过FeSO4溶液制备K2FeO4的工艺流程如图所示。回答下列问题:
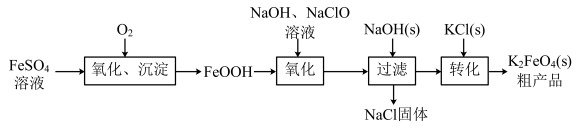
(1)K2FeO4中Fe元素的化合价为_______ 价
(2)“氧化、沉淀”时,氧化剂和还原剂的物质的量之比为_______ 。Fe2+在溶液中放置不稳定,易被氧化成Fe3+,用KSCN溶液检验溶液中的Fe3+是较好的方法,此法的离子方程式为_______ 。
(3)通过“氧化”时FeOOH与NaClO反应生成的Na2FeO4可知,在该条件下物质氧化性:Na2FeO4_______ NaClO(填“>”或“<”)。
(4)写出氢氧化亚铁溶液被空气中氧化为氢氧化铁的化学方程式_______ 。
(5)过滤操作所需要的玻璃仪器有烧杯和_______ 。

(1)K2FeO4中Fe元素的化合价为
(2)“氧化、沉淀”时,氧化剂和还原剂的物质的量之比为
(3)通过“氧化”时FeOOH与NaClO反应生成的Na2FeO4可知,在该条件下物质氧化性:Na2FeO4
(4)写出氢氧化亚铁溶液被空气中氧化为氢氧化铁的化学方程式
(5)过滤操作所需要的玻璃仪器有烧杯和
您最近半年使用:0次
名校
4 . “价类”二维图是学习元素及其化合物的重要工具,如图所示是铁及其化合物的“价类”二维图。
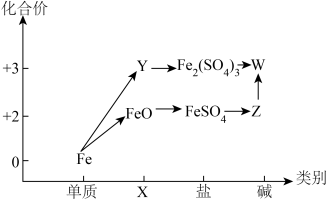
(1)X、Y分别代表_______ 、_______ ;Z在空气中转化为W的化学方程式为_______ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与_______ 发生氧化还原反应(填序号)。
①NaOH溶液②氯水③稀盐酸④酸性 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠
(3)往FeBr2溶液中通入一定量氯气,已知n(FeBr2)∶n(Cl2)=1,写出该反应的离子方程式_______ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、_______ ,然后将少许滤液加入试管中,加入少量稀硝酸(稀硝酸具有氧化性),再滴加几滴KSCN溶液,振荡,若观察到_______ 现象,说明试验样品中含有铁元素。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目_______ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①NaOH溶液②氯水③稀盐酸④酸性
 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠(3)往FeBr2溶液中通入一定量氯气,已知n(FeBr2)∶n(Cl2)=1,写出该反应的离子方程式
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用
 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目
您最近半年使用:0次
名校
5 . 物质类别和核心元素的化合价是研究物质性质的两个基本视角。若以物质类别为横坐标、核心元素化合价为纵坐标绘制的图像叫价类图。下面是有关铁元素的价类图,下列分析正确的是
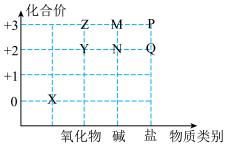

A. 是红棕色粉末,广泛用于高档汽车涂料、建筑涂料等,是较好的环保涂料 是红棕色粉末,广泛用于高档汽车涂料、建筑涂料等,是较好的环保涂料 |
B.向 中加入 中加入 溶液,先生成 溶液,先生成 ,而后迅速转化为灰绿色的 ,而后迅速转化为灰绿色的 |
C. 在氧气中燃烧的产物是 在氧气中燃烧的产物是 , , 是 是 、 、 组成的混合物 组成的混合物 |
D.若 为硫酸盐,则 为硫酸盐,则 、 、 、 、 均能与稀硫酸反应得到 均能与稀硫酸反应得到 |
您最近半年使用:0次
6 . 室温下,反应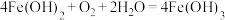 可以自发进行。下列叙述错误的是
可以自发进行。下列叙述错误的是
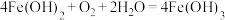 可以自发进行。下列叙述错误的是
可以自发进行。下列叙述错误的是A.该反应 |
| B.该反应有可能是吸热反应 |
| C.反应过程中,白色沉淀逐渐变成灰绿色,最后呈红褐色 |
| D.综合考虑焓变和熵变可以判断反应自发进行的方向 |
您最近半年使用:0次
解题方法
7 . 电子工业中常用覆铜板为基材制作印刷电路板,原理是利用 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
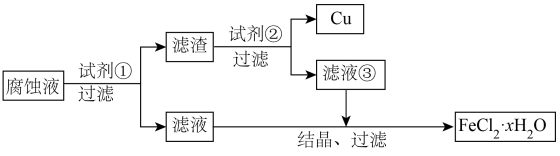
(1) 溶液腐蚀电路板的化学方程式为
溶液腐蚀电路板的化学方程式为___________ 。
(2)过量试剂①为___________ ;过量试剂②为___________ 。
(3)鉴别滤液③中的金属阳离子,应滴加的试剂依次是___________ ,现象是___________ 。 长时间暴露在空气中会变质,主要原因是
长时间暴露在空气中会变质,主要原因是___________ 。
(4)取 滤液③加入试管中,逐滴加入
滤液③加入试管中,逐滴加入 溶液。填写下列表格:
溶液。填写下列表格:
 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
(1)
 溶液腐蚀电路板的化学方程式为
溶液腐蚀电路板的化学方程式为(2)过量试剂①为
(3)鉴别滤液③中的金属阳离子,应滴加的试剂依次是
 长时间暴露在空气中会变质,主要原因是
长时间暴露在空气中会变质,主要原因是(4)取
 滤液③加入试管中,逐滴加入
滤液③加入试管中,逐滴加入 溶液。填写下列表格:
溶液。填写下列表格:| 序号 | 现象 | 用方程式解释现象 |
| ① | 开始无明显现象 | |
| ② | 稍后出现白色沉淀 |  |
| ③ | 空气中放置一段时间后,出现红褐色沉淀 |
您最近半年使用:0次
名校
解题方法
8 . 铁的价 类二维图如图所示
类二维图如图所示 箭头表示物质之间的转化
箭头表示物质之间的转化 。下列说法错误的是
。下列说法错误的是

 类二维图如图所示
类二维图如图所示 箭头表示物质之间的转化
箭头表示物质之间的转化 。下列说法错误的是
。下列说法错误的是
A. 可以在空气中完成转化 可以在空气中完成转化 |
B. 可以加入 可以加入 溶液 溶液 |
C. 在空气中燃烧可得到 在空气中燃烧可得到 |
D.保存 的盐溶液时需加入 的盐溶液时需加入 |
您最近半年使用:0次
名校
9 . 某兴趣小组利用下列试剂:铁粉、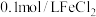 溶液、
溶液、 溶液、
溶液、 溶液、新制氯水,探究
溶液、新制氯水,探究 、
、 的氧化性、还原性以及
的氧化性、还原性以及 还原性,并利用实验结论解决一些问题。
还原性,并利用实验结论解决一些问题。
(1)用所给试剂写出体现 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:___________ 。
(2)设计实验方案,完成下列表格。
(3) 不稳定,易被氧化,请描述向
不稳定,易被氧化,请描述向 溶液中滴加
溶液中滴加 溶液的实验现象?
溶液的实验现象?___________ ;该过程中发生反应的化学方程式为:___________ 。
(4)某同学帮助该兴趣小组配制480mL0.5 的NaOH溶液以备使用。
的NaOH溶液以备使用。
①该同学应称取NaOH的质量为___________ g,如图所示的仪器中,配制溶液需要使用的是___________ (填序号),还缺少的玻璃仪器是___________ (填仪器名称)。
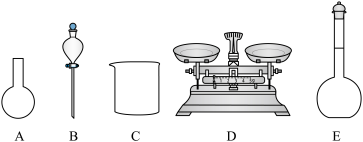
②由于错误操作,使得实际浓度比所要求的浓度偏小的是___________ (填序号)。
A.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
B.使用容量瓶配制溶液时,俯视液面定容
C.没有用蒸馏水洗涤溶解所使用的烧杯
D.容量瓶刚用蒸馏水洗净,没有干燥
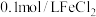 溶液、
溶液、 溶液、
溶液、 溶液、新制氯水,探究
溶液、新制氯水,探究 、
、 的氧化性、还原性以及
的氧化性、还原性以及 还原性,并利用实验结论解决一些问题。
还原性,并利用实验结论解决一些问题。(1)用所给试剂写出体现
 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:(2)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
探究 的化学性质 的化学性质 | 取少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液 溶液 | 加入铁粉后,溶液变成 溶液后,溶液不变色。 溶液后,溶液不变色。 |
结论: 具有 具有 | ||
(3)
 不稳定,易被氧化,请描述向
不稳定,易被氧化,请描述向 溶液中滴加
溶液中滴加 溶液的实验现象?
溶液的实验现象?(4)某同学帮助该兴趣小组配制480mL0.5
 的NaOH溶液以备使用。
的NaOH溶液以备使用。①该同学应称取NaOH的质量为

②由于错误操作,使得实际浓度比所要求的浓度偏小的是
A.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
B.使用容量瓶配制溶液时,俯视液面定容
C.没有用蒸馏水洗涤溶解所使用的烧杯
D.容量瓶刚用蒸馏水洗净,没有干燥
您最近半年使用:0次
名校
10 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)现有铁和铜的混合物,可以通过______把他们分开。
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式:_______ 。反应后的废液中含有Fe3+,可以用______ 检验。
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。
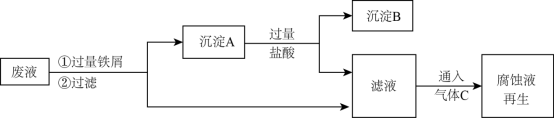
沉淀A中含有的单质:______ ,黄绿色气体C可以把滤液转化成FeCl3腐蚀液,写出反应过程中的离子方程式_______ 。
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_______ 。
(5)把铁皮插入到的硫酸铜和硫酸的混合溶液中,一段后取出,溶液的质量不变,则参加反应的H+与Cu2+物质的量之比为:______ 。
(1)现有铁和铜的混合物,可以通过______把他们分开。
| A.盐酸 | B.Fe3O4 | C.稀硝酸 | D.Fe2O3 |
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。

沉淀A中含有的单质:
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)把铁皮插入到的硫酸铜和硫酸的混合溶液中,一段后取出,溶液的质量不变,则参加反应的H+与Cu2+物质的量之比为:
您最近半年使用:0次



