名校
解题方法
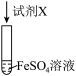
1 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: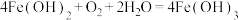 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |
您最近半年使用:0次
名校
解题方法
2 . 下列变化与氧化还原反应无关的是
| A.切开金属钠表面失去金属光泽 |
| B.氯气使湿润的红纸条褪色 |
| C.向硫酸亚铁溶液中滴加氢氧化钠溶液出现白色沉淀 |
| D.氢氧化亚铁在空气中迅速变成灰绿色,最后变为红褐色 |
您最近半年使用:0次
名校
3 . 下列物质的颜色变化与氧化还原反应无关 的是
| A.浓硝酸久置后,显黄色 |
| B.将SO2通入酸性高锰酸钾溶液中,溶液紫红色褪去 |
| C.新制的白色氢氧化亚铁放置在空气中,最终变为红褐色 |
D.向黄色的铬酸钾(K2CrO4)溶液中加入硫酸,溶液变为橙红色(Cr2O ) ) |
您最近半年使用:0次
2024-02-23更新
|
304次组卷
|
2卷引用:北京师范大学附属中学2023-2024学年高三下学期开学考化学试题
名校
4 . 纳米Fe3O4在磁流体、催化剂、医学等领域具有广阔的应用前景。氧化共沉淀制备纳米Fe3O4的方法如下:
Ⅰ.Fe2+的氧化:将FeSO4溶液用NaOH溶液调节pH至a,再加入H2O2溶液,立即得到FeOOH红棕色悬浊液。
(1)①若用NaOH溶液调节pH过高会产生白色沉淀,该反应的离子方程式是___________ 。
②该白色沉淀置于空气中能观察的现象是___________ 。
③上述反应完成后,测得a值与FeOOH产率及其生成后溶液pH的关系,结果如下:
用离子方程式解释FeOOH生成后溶液pH下降的原因:___________ 。
(2)经检验:当a=7时,产物中存在大量Fe2O3。对Fe2O3的产生提出两种假设:
i.反应过程中溶液酸性增强,导致FeOOH向Fe2O3的转化;
ii.溶液中存在少量Fe2+,导致FeOOH向Fe2O3的转化。
①经分析,假设i不成立的实验依据是___________ 。
②其他条件相同时,向FeOOH浊液中加入不同浓度Fe2+,30min后测定物质的组成,结果如下:
以上结果表明:___________ 。
③a=7和a=9时,FeOOH产率差异很大的原因是___________ 。
Ⅱ.Fe2+和Fe3+共沉淀:向FeOOH红棕色悬浊液中同时加入FeSO4溶液和NaOH浓溶液进行共沉淀,再将此混合液加热回流、冷却、过滤、洗涤、干燥,得到纳米Fe3O4。
(3)共沉淀时的反应条件对产物纯度和产率的影响极大。
①共沉淀pH过高时,会导致FeSO4溶液被快速氧化;共沉淀pH过低时,得到的纳米Fe3O4中会混有的物质是___________ 。
②已知N=n(FeOOH)/n(Fe2+),其他条件一定时,测得纳米Fe3O4的产率随N的变化曲线如下图所示:
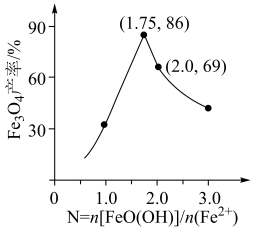
经理论分析,N=2共沉淀时纳米Fe3O4产率应最高,事实并非如此的可能原因是___________ 。
(4)测量制得的纳米Fe3O4中n(Fe3+)/n(Fe2+):取ag样品,加入足量盐酸使之完全溶解,加入SnCl2将Fe3+还原为Fe2+;除去过量SnCl2后,用c1mol/LK2Cr2O7标准溶液滴定(还原产物为Cr3+),消耗K2Cr2O7溶液的体积为v1mL,另取ag样品,加入足量稀硫酸使之完全溶解,用c2mol/LKMnO4标准溶液滴定至终点,消耗KMnO4溶液的体积为v2mL,则样品中n(Fe3+)/n(Fe2+)为___________ 。
Ⅰ.Fe2+的氧化:将FeSO4溶液用NaOH溶液调节pH至a,再加入H2O2溶液,立即得到FeOOH红棕色悬浊液。
(1)①若用NaOH溶液调节pH过高会产生白色沉淀,该反应的离子方程式是
②该白色沉淀置于空气中能观察的现象是
③上述反应完成后,测得a值与FeOOH产率及其生成后溶液pH的关系,结果如下:
| a | 7.0 | 8.0 | 9.0 |
| FeO(OH)的产率 | <50% | 95% | >95% |
| FeO(OH)生成后的pH | 接近4 | 接近4 | 接近4 |
(2)经检验:当a=7时,产物中存在大量Fe2O3。对Fe2O3的产生提出两种假设:
i.反应过程中溶液酸性增强,导致FeOOH向Fe2O3的转化;
ii.溶液中存在少量Fe2+,导致FeOOH向Fe2O3的转化。
①经分析,假设i不成立的实验依据是
②其他条件相同时,向FeOOH浊液中加入不同浓度Fe2+,30min后测定物质的组成,结果如下:
| c(Fe2+)/mol/L | FeO(OH)百分含量/% | Fe2O3百分含量/% |
| 0.00 | 100 | 0 |
| 0.01 | 40 | 60 |
| 0.02 | 0 | 100 |
③a=7和a=9时,FeOOH产率差异很大的原因是
Ⅱ.Fe2+和Fe3+共沉淀:向FeOOH红棕色悬浊液中同时加入FeSO4溶液和NaOH浓溶液进行共沉淀,再将此混合液加热回流、冷却、过滤、洗涤、干燥,得到纳米Fe3O4。
(3)共沉淀时的反应条件对产物纯度和产率的影响极大。
①共沉淀pH过高时,会导致FeSO4溶液被快速氧化;共沉淀pH过低时,得到的纳米Fe3O4中会混有的物质是
②已知N=n(FeOOH)/n(Fe2+),其他条件一定时,测得纳米Fe3O4的产率随N的变化曲线如下图所示:

经理论分析,N=2共沉淀时纳米Fe3O4产率应最高,事实并非如此的可能原因是
(4)测量制得的纳米Fe3O4中n(Fe3+)/n(Fe2+):取ag样品,加入足量盐酸使之完全溶解,加入SnCl2将Fe3+还原为Fe2+;除去过量SnCl2后,用c1mol/LK2Cr2O7标准溶液滴定(还原产物为Cr3+),消耗K2Cr2O7溶液的体积为v1mL,另取ag样品,加入足量稀硫酸使之完全溶解,用c2mol/LKMnO4标准溶液滴定至终点,消耗KMnO4溶液的体积为v2mL,则样品中n(Fe3+)/n(Fe2+)为
您最近半年使用:0次
名校
5 . 下列实验过程中,与氧化还原反应无关 的是
A | B | C | D | |
| 实验 | 将 溶液滴入 溶液滴入 溶液 溶液 | 将酚酞滴入 与水反应后的溶液 与水反应后的溶液 | 将 投入 投入 溶液 溶液 | 将稀盐酸加入 溶液,至过量 溶液,至过量 |
| 现象 | 产生白色沉淀,最终变为红褐色 | 溶液先变红后褪色 | 产生无色气泡 | 先产生白色沉淀后又溶解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 氧化还原反应与四种基本类型的关系如图所示,则下列化学反应属于阴影部分的是


A. |
B.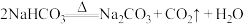 |
C.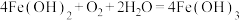 |
D.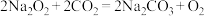 |
您最近半年使用:0次
2024-01-04更新
|
128次组卷
|
23卷引用:北京市北京师范大学附属实验中学2021-2022学年高一上学期期中考试化学试题
北京市北京师范大学附属实验中学2021-2022学年高一上学期期中考试化学试题浙江省金华市云富高级中学2020-2021学年高一上学期第一次月考化学试题浙江省金华市第八中学2021-2022学年高一上学期9月月考卷化学试题河北省张家口市宣化第一中学2021-2022学年高一上学期期初考试化学试题浙江省台州市书生中学2021-2022学年高一上学期第一次月考化学试题甘肃省天水市田家炳中学2021-2022学年高一上学期第一阶段考试化学试卷广东省普宁市第二中学2021-2022学年高一上学期期中考试化学试题(已下线)第07练 氧化还原反应-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)湖南省邵阳市第二中学2021-2022学年高一上学期期中考试化学试题(已下线)衔接点11 氧化还原反应概念-2022年初升高化学无忧衔接?(已下线)第一章 物质及其变化(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)【2022】【高一上】【期中考】【杭九】【高中化学】【赵优萍收集】广东实验中学附属江门学校2022-2023学年高一上学期期中考试化学试题四川省绵阳市南山中学2022-2023学年高一上学期12月线上测试化学试题广东省清远市名校2023-2024学年高一上学期期中调研联考化学试题江苏省苏州工业园区星海实验高级中学2023-2024学年高一上学期10月月考化学试题云南会泽县实验高级中学校2023-2024学年高一上学期10月月考化学试题河北省石家庄卓越中学2023-2024学年高一上学期期中考试化学试题广西钦州市第四中学2023-2024学年高一上学期11月考试化学试卷云南省曲靖市罗平县第一中学2023-2024学年高一上学期9月月考化学试题广东省珠海市第四中学2023-2024学年高一上学期期中考试化学试卷云南省宣威市东升实验中学2023-2024学年高一上学期11月月考化学试题山东省济宁市微山县第二中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
7 . 通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
| 选项 | 操作、现象 | 解释 |
| A | 向淀粉KI溶液中加入FeCl3溶液,溶液变蓝 | Fe3+能与淀粉发生显色反应 |
| B | 把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点 | 铁在潮湿的空气中易生成Fe(OH)3 |
| C | 足量Fe在少量Cl2中燃烧,铁有剩余 | Fe被氧化为Fe2+ |
| D | 新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色 | Fe(OH)2易被O2氧化成Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 铁及其化合物在日常生活中有广泛应用。
(1)向硫酸亚铁溶液中滴加氢氧化钠溶液,生成白色沉淀,迅速___________ (补全实验现象),化学方程式为___________ 。
(2)绿矾( )是补血剂的原料,易变质。设计实验证明绿矾未
)是补血剂的原料,易变质。设计实验证明绿矾未完全 变质________ 。
(3)利用绿矾制备还原铁粉的工业流程如下:
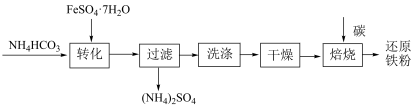
①“转化”是在水溶液中进行,产生白色沉淀和无色无味气体。写出反应的离子方程式___________ 。
②干燥过程主要是为了脱去游离水和结晶水,过程中会有少量 在空气中被氧化为
在空气中被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(4)某同学在:实验室进行铁盐与亚铁盐相互转化的实验:
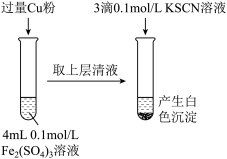
实验 :将
:将 转化为
转化为
① 与
与 粉发生反应的离子方程式为
粉发生反应的离子方程式为___________ 。
②探究白色沉淀产生的原因,请填写实验方案:
查阅资料:i. 的依学性质与
的依学性质与 相似;ii.
相似;ii.
 与
与 反应的离子方程式为
反应的离子方程式为____________________ 。
实验II:将 转化为
转化为
③用离子方程式表示溶液变红的原因是___________ 、 ,为探究红色消失的原因,继续查阅资料:SCN中C为+4价,N为-3价,可被强氧化剂氧化为CO2、N2和
,为探究红色消失的原因,继续查阅资料:SCN中C为+4价,N为-3价,可被强氧化剂氧化为CO2、N2和 ,用离子方程式表示红色消失的原因为:
,用离子方程式表示红色消失的原因为:___________ 。
(1)向硫酸亚铁溶液中滴加氢氧化钠溶液,生成白色沉淀,迅速
(2)绿矾(
 )是补血剂的原料,易变质。设计实验证明绿矾未
)是补血剂的原料,易变质。设计实验证明绿矾未(3)利用绿矾制备还原铁粉的工业流程如下:

①“转化”是在水溶液中进行,产生白色沉淀和无色无味气体。写出反应的离子方程式
②干燥过程主要是为了脱去游离水和结晶水,过程中会有少量
 在空气中被氧化为
在空气中被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为(4)某同学在:实验室进行铁盐与亚铁盐相互转化的实验:

实验
 :将
:将 转化为
转化为
①
 与
与 粉发生反应的离子方程式为
粉发生反应的离子方程式为②探究白色沉淀产生的原因,请填写实验方案:
查阅资料:i.
 的依学性质与
的依学性质与 相似;ii.
相似;ii.
 与
与 反应的离子方程式为
反应的离子方程式为实验II:将
 转化为
转化为
| 实验方案 | 现象 |
| 向0.1mol/LFeCl2溶液中加入一滴KSCN溶液;再通入氯气 | 溶液颜色无明显变化;溶液变红,一段时间后红色消失。 |
 ,为探究红色消失的原因,继续查阅资料:SCN中C为+4价,N为-3价,可被强氧化剂氧化为CO2、N2和
,为探究红色消失的原因,继续查阅资料:SCN中C为+4价,N为-3价,可被强氧化剂氧化为CO2、N2和 ,用离子方程式表示红色消失的原因为:
,用离子方程式表示红色消失的原因为:
您最近半年使用:0次
名校
解题方法
9 . 有人设计出一种在隔绝空气条件下让钠与 溶液反应,观察
溶液反应,观察 颜色的实验。实验时,往
颜色的实验。实验时,往 的大试管中先加
的大试管中先加 煤油,取
煤油,取 粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入
粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入 溶液
溶液 不含
不含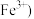 使煤油的液面至橡胶塞,并夹紧弹簧夹
使煤油的液面至橡胶塞,并夹紧弹簧夹 如图所示
如图所示 。下列说法错误的是
。下列说法错误的是

 溶液反应,观察
溶液反应,观察 颜色的实验。实验时,往
颜色的实验。实验时,往 的大试管中先加
的大试管中先加 煤油,取
煤油,取 粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入
粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入 溶液
溶液 不含
不含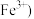 使煤油的液面至橡胶塞,并夹紧弹簧夹
使煤油的液面至橡胶塞,并夹紧弹簧夹 如图所示
如图所示 。下列说法错误的是
。下列说法错误的是

| A.长颈漏斗中的液面上升 |
| B.大试管下层溶液出现白色沉淀,并可持续较长时间 |
| C.用过氧化钠代替钠也可以观察到此现象 |
| D.该反应同时也能说明钠不能与硫酸亚铁溶液发生置换反应 |
您最近半年使用:0次
2023-10-05更新
|
241次组卷
|
4卷引用:北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷
北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题广东省东莞市东莞中学松山湖学校2023-2024学年高一上学期期中考试化学试卷(已下线)专题03 铁 金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)
名校
解题方法
10 . 氨气在工农业生产中有重要应用。
(1)工业合成氨的化学方程式为___________ 。
(2)某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。
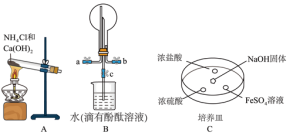
①实验室用装置A制备氨气的化学方程式为___________ 。
②用装置B收集氨时,进气口是___________ (选填“a”或“b”)。打开装置B中的活塞c,烧瓶内产生了红色喷泉,则说明氨具有的性质是___________ ,___________ 。
③向C中NaOH固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___________ ,检验白烟中阳离子的方法是:取少量白烟于试管中,___________ 。FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有Fe2++2NH3·H2O=Fe(OH)2↓+2 和
和___________ 。
(1)工业合成氨的化学方程式为
(2)某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。

①实验室用装置A制备氨气的化学方程式为
②用装置B收集氨时,进气口是
③向C中NaOH固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 和
和
您最近半年使用:0次