1 . 以下流程中涉及的物质均为中学化学常见物质,其中白色固体A为一种常见的钠盐,混合气体C可使澄清石灰水变浑浊,白色固体F在空气中易迅速变为灰绿色,黑色固体H有磁性。

请回答下列问题:
(1)白色固体E的化学式为___________ ;黑色固体H的化学式为___________ ;无色气体I的化学式为___________ 。
(2)无色混合气体C的组成为___________ 。
(3)白色固体A与少量澄清石灰水反应的离子方程式为___________ 。
(4)白色固体F无氧常温条件下分解的化学方程式为___________ 。
(5)请设计实验验证黑色固体H中金属元素的化合价___________ 。

请回答下列问题:
(1)白色固体E的化学式为
(2)无色混合气体C的组成为
(3)白色固体A与少量澄清石灰水反应的离子方程式为
(4)白色固体F无氧常温条件下分解的化学方程式为
(5)请设计实验验证黑色固体H中金属元素的化合价
您最近一年使用:0次
名校
解题方法
2 . 碳酸亚铁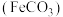 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
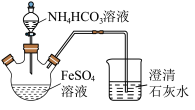
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是___________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3) 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:___________ 。
(4)某 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入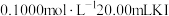 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程___________ 。
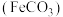 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)
 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:(4)某
 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入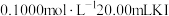 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程
您最近一年使用:0次
解题方法
3 . 利用矿铁厂的废铁屑(主要成分为 ,含有沙土、油污、
,含有沙土、油污、 和
和 )制备磁性纳米
)制备磁性纳米 的流程如图:
的流程如图:
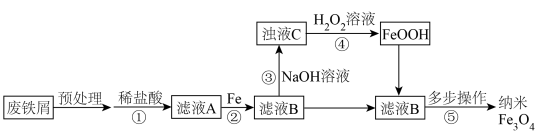
下列说法中错误的是
 ,含有沙土、油污、
,含有沙土、油污、 和
和 )制备磁性纳米
)制备磁性纳米 的流程如图:
的流程如图:
下列说法中错误的是
A.预处理时,需要使用 溶液,可将溶液进行适当升温 溶液,可将溶液进行适当升温 |
B.纳米 属于胶体,能发生丁达尔效应 属于胶体,能发生丁达尔效应 |
| C.滤液B中加入氢氧化钠溶液时,可观察到有白色沉淀生成,迅速转为灰绿色,最后转化为红褐色 |
D.步骤⑤发生反应的离子方程式为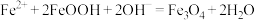 |
您最近一年使用:0次
2023-09-10更新
|
457次组卷
|
2卷引用:辽宁省辽西联合校2023-2024学年高三上学期期中考试化学试题
解题方法
4 . 草酸亚铁晶体(FeC2O4·2H2O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如下:

(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是(用化学方程式表示)________ 。
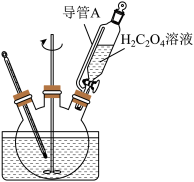
(2)“转化”在如图所示的装置中进行,导管A的作用是___________ 。
(3)检验“洗涤”完全的实验操作是___________ 。
(4)草酸亚铁晶体在空气中易氧化,检验草酸亚铁晶体是否氧化变质的实验操作是________ 。
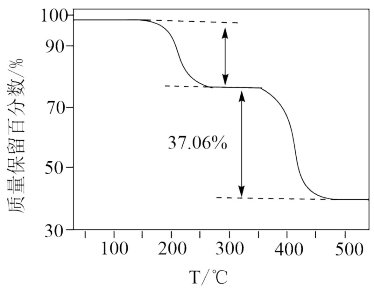
(5)在氩气中加热草酸亚铁晶体(FeC2O4∙2H2O),FeC2O4∙2H2O的质量变化曲线随温度升高出现两个失重“台阶”,如图所示。结合表格,计算第一阶段的质量损失率为___________ (保留4位有效数字),推断第二阶段产生气体的化学式为___________ 。(质量损失率=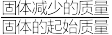 ×100%)
×100%)

(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是(用化学方程式表示)
(2)“转化”在如图所示的装置中进行,导管A的作用是

(3)检验“洗涤”完全的实验操作是
(4)草酸亚铁晶体在空气中易氧化,检验草酸亚铁晶体是否氧化变质的实验操作是
(5)在氩气中加热草酸亚铁晶体(FeC2O4∙2H2O),FeC2O4∙2H2O的质量变化曲线随温度升高出现两个失重“台阶”,如图所示。结合表格,计算第一阶段的质量损失率为
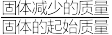 ×100%)
×100%)| 失重阶段 | 温度范围/℃ | 质量损失率% | 产物 |
| 第一阶段 | 室温~255 | __________ | FeC2O4 |
| 第二阶段 | 255-520 | 37.06 | Fe3O4 |

您最近一年使用:0次
2023-04-27更新
|
519次组卷
|
2卷引用:江苏省扬州市高邮市2022-2023学年高一下学期4月期中考试化学试题
22-23高二上·浙江·期中
5 . 为了探究某不溶性固体化合物X (仅含两种元素)。的组成和性质,设计并完成如下实验(假设各步反应均完全,反应中气体完全逸出)。已知甲是密度最小的气体,乙能使湿润的红色石蕊试纸变蓝。
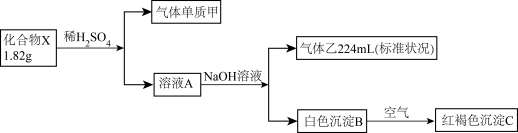
(1)组成X的元素是_______ 。
(2)写出B →C的化学反应方程式_______ 。
(3)写出化合物X与稀硫酸反应的离子方程式_______ 。
(4)请设计实验方案,检验溶液A中的金属阳离子_______ 。

(1)组成X的元素是
(2)写出B →C的化学反应方程式
(3)写出化合物X与稀硫酸反应的离子方程式
(4)请设计实验方案,检验溶液A中的金属阳离子
您最近一年使用:0次
名校
解题方法
6 . 用油造气的废镍催化剂(含NiCO3、Na2SiO3、少量Fe2+、Fe3+及Cr3+的化合物)制取NiSO4•7H2O的工艺流程如图所示(CTAC一种硅酸胶体凝聚剂)。回答下列问题:
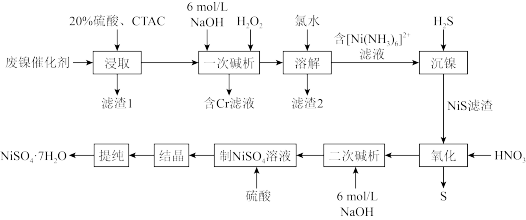
(1)“浸取”时,在硫酸浓度和用量、溶解时温度、搅拌速率均一定时,提高镍的回收率还可采取的措施是___ (写出一条)。
(2)“滤渣1”的主要成分是__ 。
(3)“一次碱析”时,Cr(OH)3转化为的CrO 的离子方程式为
的离子方程式为___ 。
(4)加氨水“溶解”的目的是__ ,‘滤渣2”的主要成分是__ 。
(5)“氧化”时,HNO3被还原为NO,该反应的化学方程式为__ 。

(1)“浸取”时,在硫酸浓度和用量、溶解时温度、搅拌速率均一定时,提高镍的回收率还可采取的措施是
(2)“滤渣1”的主要成分是
(3)“一次碱析”时,Cr(OH)3转化为的CrO
 的离子方程式为
的离子方程式为(4)加氨水“溶解”的目的是
(5)“氧化”时,HNO3被还原为NO,该反应的化学方程式为
您最近一年使用:0次
名校
7 . X溶液中可能含有下列8种离子中的几种:Fe3+、Fe2+、Na+、NH 、CO
、CO 、Cl−、SO
、Cl−、SO 、SO
、SO 。某同学为确定其成分,设计并完成以下实验(已知:Fe3+与SCN−呈血红色,且不考虑水解,所加试剂均足量):
。某同学为确定其成分,设计并完成以下实验(已知:Fe3+与SCN−呈血红色,且不考虑水解,所加试剂均足量):
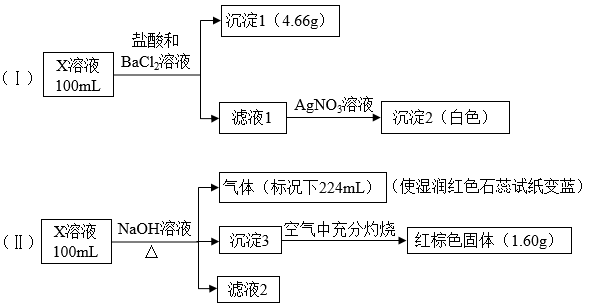
下列说法正确的是
 、CO
、CO 、Cl−、SO
、Cl−、SO 、SO
、SO 。某同学为确定其成分,设计并完成以下实验(已知:Fe3+与SCN−呈血红色,且不考虑水解,所加试剂均足量):
。某同学为确定其成分,设计并完成以下实验(已知:Fe3+与SCN−呈血红色,且不考虑水解,所加试剂均足量):
下列说法正确的是
A.X溶液中一定存在Na+、SO 、SO 、SO 、CO 、CO |
B.X溶液中一定存在NH 、Na+、SO 、Na+、SO ,至少含有Fe3+、Fe2+离子中的一种 ,至少含有Fe3+、Fe2+离子中的一种 |
| C.取少量X溶液,先加入适量氯水,再加少量KSCN溶液,若溶液呈血红色,则含有Fe2+ |
D.X溶液中一定含有Cl−,且c(Cl−)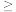 0.1mol·L−1 0.1mol·L−1 |
您最近一年使用:0次
2020-11-29更新
|
655次组卷
|
2卷引用:安徽省安庆市第一中学2020-2021学年高一上学期期中考试化学试题
8 . 食品包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧过程与电化学知识相关。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长食品保质期 |
| B.脱氧过程中炭作原电池正极,电极反应为:4H++O2+4e-=2H2O |
| C.含有0.56 g铁粉的脱氧剂,理论上最多能吸收氧气168 mL(标准状况) |
| D.该过程实现了电能到化学能的转化 |
您最近一年使用:0次
2020-11-18更新
|
731次组卷
|
6卷引用:河北省张家口市第一中学2021届高三上学期期中考试(衔接班)化学试题
河北省张家口市第一中学2021届高三上学期期中考试(衔接班)化学试题(已下线)练习10 金属的腐蚀与防护-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)广东省广州市第六中学2022届高三第二次月考化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高二上学期第一次月考化学试题江苏省丹阳高级中学2021-2022学年高二下学期期初考试化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题1-5)
9 . 已知A为单质,与某物质反应生成气体与B,有以下物质相互转化:
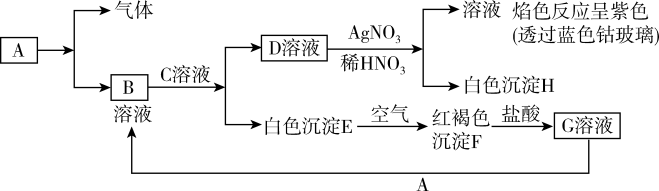
(1)写出B的化学式____ ,D的化学式________ 。
(2)写出由E转变成F的化学方程式______ 。
(3)写出用KSCN鉴别G溶液的离子方程式__ ,向G溶液加入A的有关离子反应方程式__ 。

(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)写出用KSCN鉴别G溶液的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现血红色。

(1)物质A的化学式为___ ,F化学式为___ ;
(2)B和R在溶液中反应生成F的离子方程式为___ ;
(3)H在潮湿空气中变成M的实验现象是___ ,化学方程式为___ 。
(4)A和水反应生成B和C的离子方程式为___ ,由此反应可知A有作为___ 的用途。
(5)M投入盐酸中的离子方程式___ 。

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)A和水反应生成B和C的离子方程式为
(5)M投入盐酸中的离子方程式
您最近一年使用:0次
2019-11-15更新
|
635次组卷
|
5卷引用:安徽省蚌埠市田家炳中学、五中2020届高三上学期期中考试化学试题



