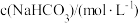名校
解题方法
1 . 某研究小组欲探究 能否与
能否与 溶液反应。
溶液反应。
【查阅资料】
i. 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。
ii. 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。
【提出猜想】
(1)小组同学经过讨论后,认为 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:___________ 。
【设计实验】
(2)实验I:在试管中加入 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液_____ ,小组同学认为 和
和 溶液反应生成了
溶液反应生成了 。
。
(3)甲同学注意到盛放 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是______ 。
重新设计实验:
实验II:在试管中加入 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。
【获得结论】
(4)过氧化氢___________ (填“能”或者“不能”)氧化 。
。
【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。
(5)补全实验III的方案:在试管中加入 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入___________ ,产生___________ 。
【总结反思】
(6)小组同学经过讨论后,提出了 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中,___________ ,证明待测液含有 。
。
(7)从上述实验中可以得出结论,在物质性质的检验中,应注意___________ (至少写出两条)对实验结果的影响。
 能否与
能否与 溶液反应。
溶液反应。【查阅资料】
i.
 具有较强的还原性,
具有较强的还原性, 具有较强的氧化性。
具有较强的氧化性。ii.
 遇
遇 可生成
可生成 ,
, 溶液呈血红色,可用于
溶液呈血红色,可用于 的检验。
的检验。【提出猜想】
(1)小组同学经过讨论后,认为
 溶液可以与
溶液可以与 溶液反应,请从化合价的角度加以解释:
溶液反应,请从化合价的角度加以解释:【设计实验】
(2)实验I:在试管中加入
 溶液和
溶液和 溶液,再加入
溶液,再加入 溶液,发现溶液
溶液,发现溶液 和
和 溶液反应生成了
溶液反应生成了 。
。(3)甲同学注意到盛放
 溶液的试剂瓶中有空气,因此不同意该结论,他的理由是
溶液的试剂瓶中有空气,因此不同意该结论,他的理由是重新设计实验:
实验II:在试管中加入
 溶液,然后加入
溶液,然后加入 溶液,发现溶液无明显变化,再加入
溶液,发现溶液无明显变化,再加入 溶液,发现溶液变红。
溶液,发现溶液变红。【获得结论】
(4)过氧化氢
 。
。【发现异常】
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将
 氧化为
氧化为 。乙同学设计实验III并证实了该资料中的说法。
。乙同学设计实验III并证实了该资料中的说法。(5)补全实验III的方案:在试管中加入
 溶液,加入
溶液,加入 溶液,再加入
溶液,再加入【总结反思】
(6)小组同学经过讨论后,提出了
 的检验方法:取待测液于试管中,
的检验方法:取待测液于试管中, 。
。(7)从上述实验中可以得出结论,在物质性质的检验中,应注意
您最近一年使用:0次
2021-11-07更新
|
1003次组卷
|
4卷引用:河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题
名校
2 . 铁元素的“价—类”二维图如图所示:
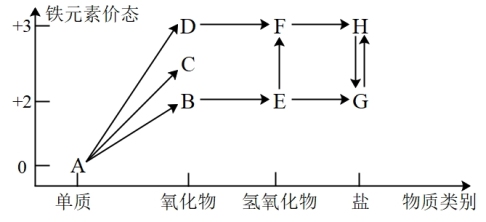
(1)C的化学式是_______ , 反应的化学方程式是
反应的化学方程式是_______ ,反应过程的现象为_______ 。
(2)维生素C可将H转化为G,维生素C具有_______ (填“酸性”、“氧化性”或“还原性”)。
(3)在指定条件下,下列铁及其化合物之间的转化不能实现的是_______ 。
A. B.
B.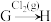 C.
C.
(4)某小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
试剂:酸化的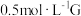 溶液,
溶液,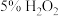 溶液
溶液
①上述实验中 溶液与G溶液反应的离子方程式是
溶液与G溶液反应的离子方程式是_______ 。
②产生气泡的原因是_______ 。

(1)C的化学式是
 反应的化学方程式是
反应的化学方程式是(2)维生素C可将H转化为G,维生素C具有
(3)在指定条件下,下列铁及其化合物之间的转化不能实现的是
A.
 B.
B.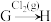 C.
C.
(4)某小组同学设计如下实验,研究亚铁盐与
 溶液的反应。
溶液的反应。试剂:酸化的
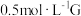 溶液,
溶液,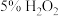 溶液
溶液| 操作 | 现象 |
取 酸化的G溶液于试管中,加入5滴 酸化的G溶液于试管中,加入5滴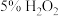 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡。 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与G溶液反应的离子方程式是
溶液与G溶液反应的离子方程式是②产生气泡的原因是
您最近一年使用:0次
2022-01-23更新
|
803次组卷
|
8卷引用:江西省南昌市进贤县第一中学2022-2023学年高一下学期第一次月考化学试题
名校
3 . 某兴趣小组利用下列试剂:铁粉、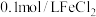 溶液、
溶液、 溶液、
溶液、 溶液、新制氯水,探究
溶液、新制氯水,探究 、
、 的氧化性、还原性以及
的氧化性、还原性以及 还原性,并利用实验结论解决一些问题。
还原性,并利用实验结论解决一些问题。
(1)用所给试剂写出体现 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:___________ 。
(2)设计实验方案,完成下列表格。
(3) 不稳定,易被氧化,请描述向
不稳定,易被氧化,请描述向 溶液中滴加
溶液中滴加 溶液的实验现象?
溶液的实验现象?___________ ;该过程中发生反应的化学方程式为:___________ 。
(4)某同学帮助该兴趣小组配制480mL0.5 的NaOH溶液以备使用。
的NaOH溶液以备使用。
①该同学应称取NaOH的质量为___________ g,如图所示的仪器中,配制溶液需要使用的是___________ (填序号),还缺少的玻璃仪器是___________ (填仪器名称)。
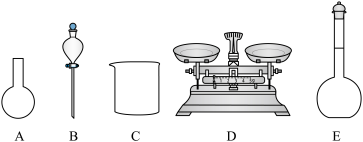
②由于错误操作,使得实际浓度比所要求的浓度偏小的是___________ (填序号)。
A.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
B.使用容量瓶配制溶液时,俯视液面定容
C.没有用蒸馏水洗涤溶解所使用的烧杯
D.容量瓶刚用蒸馏水洗净,没有干燥
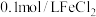 溶液、
溶液、 溶液、
溶液、 溶液、新制氯水,探究
溶液、新制氯水,探究 、
、 的氧化性、还原性以及
的氧化性、还原性以及 还原性,并利用实验结论解决一些问题。
还原性,并利用实验结论解决一些问题。(1)用所给试剂写出体现
 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:(2)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
探究 的化学性质 的化学性质 | 取少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液 溶液 | 加入铁粉后,溶液变成 溶液后,溶液不变色。 溶液后,溶液不变色。 |
结论: 具有 具有 | ||
(3)
 不稳定,易被氧化,请描述向
不稳定,易被氧化,请描述向 溶液中滴加
溶液中滴加 溶液的实验现象?
溶液的实验现象?(4)某同学帮助该兴趣小组配制480mL0.5
 的NaOH溶液以备使用。
的NaOH溶液以备使用。①该同学应称取NaOH的质量为

②由于错误操作,使得实际浓度比所要求的浓度偏小的是
A.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
B.使用容量瓶配制溶液时,俯视液面定容
C.没有用蒸馏水洗涤溶解所使用的烧杯
D.容量瓶刚用蒸馏水洗净,没有干燥
您最近一年使用:0次
名校
解题方法
4 . 广东省珠江第二大水系北江流域因当地矿业的开发,造成附近河底沉积物中铊含量严重超标,致使当地人“靠江不饮北江水”。铊(Tl)是某超导体材料的组成元素之一, 与Ag在酸性介质中发生反应
与Ag在酸性介质中发生反应 。
。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于___________ 。
(2)下列推断正确的是___________ (填序号)。
A.单质的还原性: B.原子半径:
B.原子半径:
C.碱性: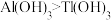 D.氧化性:
D.氧化性: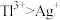
E.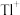 最外层只有1个电子 F.Tl能形成+3价和+1价的化合物
最外层只有1个电子 F.Tl能形成+3价和+1价的化合物
(3)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是___________ 。
(4)下列铁的化合物中,不能直接化合得到的是___________(用字母代号填)。
(5)工业利用硼矿石(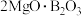 )制备单质B(硼)并联产轻质MgO的流程如下,硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
)制备单质B(硼)并联产轻质MgO的流程如下,硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
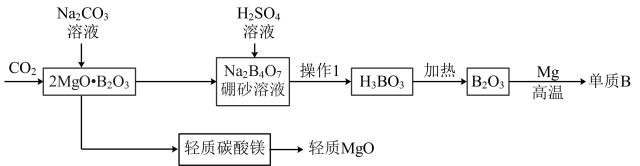
硼酸(H3BO3)的溶解度
①为了加快硼矿石与Na2CO3溶液和CO2的反应速率,可以采取的措施有___________ (填一种)。
②操作1是蒸发浓缩,___________ ,过滤,洗涤,干燥。
③制备过程中可循环的物质(填一种即可)___________ 。
④硼酸(H3BO3)是一元弱酸,在溶液中能电离生成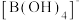 ,硼酸的电离方程式为
,硼酸的电离方程式为___________ 。
 与Ag在酸性介质中发生反应
与Ag在酸性介质中发生反应 。
。(1)铊(Tl)的原子序数为81,铊在元素周期表中位于
(2)下列推断正确的是
A.单质的还原性:
 B.原子半径:
B.原子半径:
C.碱性:
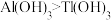 D.氧化性:
D.氧化性: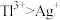
E.
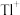 最外层只有1个电子 F.Tl能形成+3价和+1价的化合物
最外层只有1个电子 F.Tl能形成+3价和+1价的化合物(3)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是
(4)下列铁的化合物中,不能直接化合得到的是___________(用字母代号填)。
A. | B. | C. | D. |
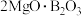 )制备单质B(硼)并联产轻质MgO的流程如下,硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
)制备单质B(硼)并联产轻质MgO的流程如下,硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
硼酸(H3BO3)的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 80 |
| 溶解度/g | 2.77 | 3.65 | 4.87 | 6.77 | 8.90 | 23.54 |
②操作1是蒸发浓缩,
③制备过程中可循环的物质(填一种即可)
④硼酸(H3BO3)是一元弱酸,在溶液中能电离生成
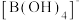 ,硼酸的电离方程式为
,硼酸的电离方程式为
您最近一年使用:0次
5 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近一年使用:0次
名校
6 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制500mL0.6mol·L的NaOH溶液,需用托盘天平(用纸垫着)称量氢氧化钠固体12.0g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制500mL0.6mol·L的NaOH溶液,需用托盘天平(用纸垫着)称量氢氧化钠固体12.0g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近一年使用:0次
名校
7 . 某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用___________ 来区分 胶体和
胶体和 溶液。
溶液。
(2)向盛有 溶液的试管中滴加
溶液的试管中滴加 溶液,请描述发生的现象
溶液,请描述发生的现象___________ 。
(3)铁粉与水蒸气在高温条件下反应的化学方程式是___________ 。
(4)电子工业中,人们常用 溶液腐蚀覆铜板来制作印刷电路板。现欲配制
溶液腐蚀覆铜板来制作印刷电路板。现欲配制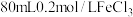 溶液,回答下列问题:
溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需___________ 。
②使用托盘天平称量 的质量为
的质量为___________ g。
③定容时,若仰视容量瓶刻度线会使配制的 溶液浓度
溶液浓度________ (填“偏大”“偏小”或“不变”)。
(5)实验室模拟用 溶液腐蚀铜板并从废液中回收
溶液腐蚀铜板并从废液中回收 和
和 溶液流程如图所示:
溶液流程如图所示:
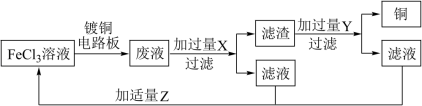
①请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
②试剂 在反应中体现
在反应中体现___________ (填“氧化性”或“还原性”)。
③Z可选用的试剂有___________ (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
(1)可利用
 胶体和
胶体和 溶液。
溶液。(2)向盛有
 溶液的试管中滴加
溶液的试管中滴加 溶液,请描述发生的现象
溶液,请描述发生的现象(3)铁粉与水蒸气在高温条件下反应的化学方程式是
(4)电子工业中,人们常用
 溶液腐蚀覆铜板来制作印刷电路板。现欲配制
溶液腐蚀覆铜板来制作印刷电路板。现欲配制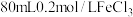 溶液,回答下列问题:
溶液,回答下列问题:①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需
②使用托盘天平称量
 的质量为
的质量为③定容时,若仰视容量瓶刻度线会使配制的
 溶液浓度
溶液浓度(5)实验室模拟用
 溶液腐蚀铜板并从废液中回收
溶液腐蚀铜板并从废液中回收 和
和 溶液流程如图所示:
溶液流程如图所示:
①请写出
 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式②试剂
 在反应中体现
在反应中体现③Z可选用的试剂有
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
您最近一年使用:0次
2023-08-03更新
|
364次组卷
|
5卷引用:山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题
山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题湖南省株洲市南方中学2022-2023学年高一上学期期末考试化学试题(已下线)巩固测试卷02-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)湖南省娄底市新化县2023-2024学年高一上学期期末考试化学试题甘肃省天水市第一中学2023-2024学年高一下学期开学化学试题
名校
解题方法
8 .  具有较强的还原性,新制的白色
具有较强的还原性,新制的白色 会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色
会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色 ,某实验小组做了如下探究实验。
,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用蒸馏水的水分子空间结构为__________ ;使用的 晶体类型为
晶体类型为__________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的 也仅能存在几分钟,其原因可能是
也仅能存在几分钟,其原因可能是__________ 。
(3)甲同学按如图a所示操作制备 (溶液均用煮沸过的蒸馏水配制)。挤入少量
(溶液均用煮沸过的蒸馏水配制)。挤入少量 溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:
溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:__________ 。
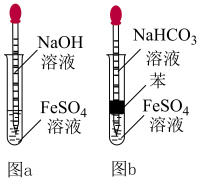
(4)乙同学经查阅资料后设计了如图 所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色
所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色 。
。
①该反应的原理为__________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色 的原因:
的原因:__________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
(1)由以上实验可得到的规律是
①由以上实验可得到的规律是__________ 。
② 溶液的浓度为
溶液的浓度为 时,
时, 溶液的最佳浓度为
溶液的最佳浓度为__________ (填“1.0”“1.5”或“2.0”) 。
。
(6)实验创新:
延长 沉淀的稳定时间还可以采取的措施为
沉淀的稳定时间还可以采取的措施为__________ (任写一条)。
 具有较强的还原性,新制的白色
具有较强的还原性,新制的白色 会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色
会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色 ,某实验小组做了如下探究实验。
,某实验小组做了如下探究实验。(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用蒸馏水的水分子空间结构为
 晶体类型为
晶体类型为(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的
 也仅能存在几分钟,其原因可能是
也仅能存在几分钟,其原因可能是(3)甲同学按如图a所示操作制备
 (溶液均用煮沸过的蒸馏水配制)。挤入少量
(溶液均用煮沸过的蒸馏水配制)。挤入少量 溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:
溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:
(4)乙同学经查阅资料后设计了如图
 所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色
所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色 。
。①该反应的原理为
②结合原理和装置特点分析能较长时间观察到白色
 的原因:
的原因:(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
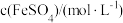 | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 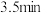 | 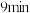 | 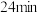 | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 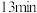 |  | 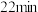 | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 |  | 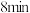 |  | |
①由以上实验可得到的规律是
②
 溶液的浓度为
溶液的浓度为 时,
时, 溶液的最佳浓度为
溶液的最佳浓度为 。
。(6)实验创新:
延长
 沉淀的稳定时间还可以采取的措施为
沉淀的稳定时间还可以采取的措施为
您最近一年使用:0次
名校
解题方法
9 . 某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用______ 来区分Fe(OH)3胶体和FeCl3溶液。
(2)向盛有FeSO4溶液的试管中滴加NaOH溶液,请描述发生的现象______ 。
(3)铁粉与水蒸气在高温条件下反应的化学方程式是______ 。
(4)电子工业中,人们常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并从废液中回收 和FeCl3溶液。实验室模拟流程如图所示:
和FeCl3溶液。实验室模拟流程如图所示:
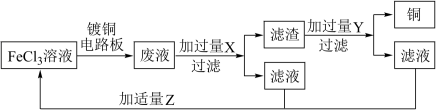
①请写出FeCl3溶液与铜反应的离子方程式______ 。
②试剂X在反应中体现______ (填“氧化性”或“还原性”)。
③Z可选用的试剂有______ (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
(1)可利用
(2)向盛有FeSO4溶液的试管中滴加NaOH溶液,请描述发生的现象
(3)铁粉与水蒸气在高温条件下反应的化学方程式是
(4)电子工业中,人们常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并从废液中回收
 和FeCl3溶液。实验室模拟流程如图所示:
和FeCl3溶液。实验室模拟流程如图所示:
①请写出FeCl3溶液与铜反应的离子方程式
②试剂X在反应中体现
③Z可选用的试剂有
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
您最近一年使用:0次
2021-01-19更新
|
287次组卷
|
2卷引用:广东省广州市广外附设外语学校2021-2022学年高一上学期12月月考化学试题
10 . 下列说法正确的是
①碱性氧化物一定是金属氧化物
②电解质溶液的导电过程伴随化学变化
③HCl 既有氧化性又有还原性
④Fe(OH)3、FeCl3、HNO3 都能用化合反应制备
⑤SO2 能使酸性高锰酸钾溶液褪色,所以它具有还原性
①碱性氧化物一定是金属氧化物
②电解质溶液的导电过程伴随化学变化
③HCl 既有氧化性又有还原性
④Fe(OH)3、FeCl3、HNO3 都能用化合反应制备
⑤SO2 能使酸性高锰酸钾溶液褪色,所以它具有还原性
| A.②⑤ | B.①②③④ | C.①②③ | D.①②③④⑤ |
您最近一年使用:0次