1 . Fe3S4固体是一种重要的磁性材料,以它为原料实现如下化合物的转化: 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。
请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为___________ ,无色酸性溶液F中的含硫阴离子有___________ 。
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式___________ 。
(3)下列说法正确的是___________。
(4)写出F→G反应的化学方程式___________ 。请设计实验方案确定溶液G中的阴离子___________ 。

 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式
(3)下列说法正确的是___________。
| A.固体A中可能含有FeO | B.无色气体E能完全溶于水 |
| C.溶液C呈酸性,是由于Fe3+水解 | D.溶液B可溶解铜 |
(4)写出F→G反应的化学方程式
您最近一年使用:0次
2024·河南南阳·模拟预测
解题方法
2 . 根据实验操作及现象,得出结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A |  和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体 和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体 | 硫酸表现氧化性, 表现还原性 表现还原性 |
| B | 向酸性 溶液中滴加乙苯,溶液褪色 溶液中滴加乙苯,溶液褪色 | 乙苯的苯环中含有碳碳双键 |
| C | Ag与HI溶液生成黄色沉淀和无色气体 |  和 和 生成AgI,促进Ag和HI溶液发生反应生成AgI和 生成AgI,促进Ag和HI溶液发生反应生成AgI和 |
| D | 在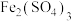 溶液中加入铜粉,溶液变蓝色 溶液中加入铜粉,溶液变蓝色 | 氧化性: , ,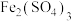 和Cu发生置换反应 和Cu发生置换反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023高三·全国·专题练习
3 . FeCl3溶液中滴加HI溶液:2Fe3++2HI=2Fe2++2H++I2。( )
您最近一年使用:0次
22-23高一上·四川绵阳·期末
4 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在空气中点燃氢气,然后把导管伸入盛满氯气的集气瓶中 | 氢气安静地燃烧,发出淡蓝色火焰 | 燃烧反应不一定要有氧气参加 |
| B | 将一小块钠投入盛有 溶液的烧杯中 溶液的烧杯中 | 烧杯底部析出红色固体 | 金属活动性: |
| C | 向 溶液中逐滴加入少量稀 溶液中逐滴加入少量稀 | 溶液导电能力不断减弱 | 生成的 不能发生电离 不能发生电离 |
| D | 向盛有 溶液的试管中滴加无色的维生素C溶液 溶液的试管中滴加无色的维生素C溶液 | 溶液黄色褪去 | 维生素 具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-18更新
|
340次组卷
|
3卷引用:2022年重庆高考真题化学试题变式题(选择题6-10)
5 . 聚合硫酸铁是一种常用净水剂,其分子式可表示为 。以工业废铁屑(含少量
。以工业废铁屑(含少量 、FeS)为原料制取聚合硫酸铁的工艺流程如图1所示。
、FeS)为原料制取聚合硫酸铁的工艺流程如图1所示。
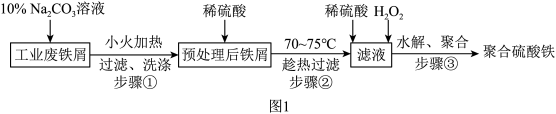
已知:硫酸亚铁的溶解度如表所示。
回答下列问题:
(1)步骤②将预处理后铁屑转移至三颈烧瓶,加入适量3mol·L
 溶液,水浴加热至70~75℃,直到不再有气泡产生。装置如图2所示。
溶液,水浴加热至70~75℃,直到不再有气泡产生。装置如图2所示。
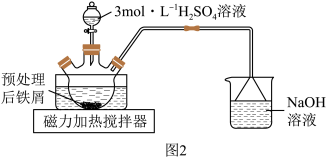
盛放3mol·L
 溶液的仪器名称为
溶液的仪器名称为___________ 。装置中用到的热源是磁力加热搅拌器,不宜使用酒精灯,是因为___________ 。
(2)步骤②趁热过滤所得的滤渣的主要成分为___________ (填化学式);过滤需要趁热的原因是___________ 。
(3)向步骤②所得滤液中滴加几滴KSCN溶液,无明显现象,是因为___________ (用离子方程式表示)。
(4)向滤液中滴加少量稀硫酸,分批加入 ,边加边搅拌,直到出现少量气泡。滤液中开始时发生反应的离子方程式为
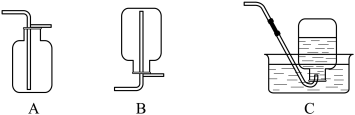
,边加边搅拌,直到出现少量气泡。滤液中开始时发生反应的离子方程式为___________ 。后期出现少量气泡的原因是___________ (用化学方程式表示),收集该气体的装置为___________ (填标号)。
(5)经上述处理后的溶液先水解后聚合得到红棕色黏稠液体即聚合硫酸铁,则水解产生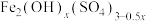 的化学方程式为
的化学方程式为___________ 。
 。以工业废铁屑(含少量
。以工业废铁屑(含少量 、FeS)为原料制取聚合硫酸铁的工艺流程如图1所示。
、FeS)为原料制取聚合硫酸铁的工艺流程如图1所示。
已知:硫酸亚铁的溶解度如表所示。
| T/℃ | 10 | 20 | 30 | 40 | 50 |
| S/g | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 |
回答下列问题:
(1)步骤②将预处理后铁屑转移至三颈烧瓶,加入适量3mol·L

 溶液,水浴加热至70~75℃,直到不再有气泡产生。装置如图2所示。
溶液,水浴加热至70~75℃,直到不再有气泡产生。装置如图2所示。
盛放3mol·L

 溶液的仪器名称为
溶液的仪器名称为(2)步骤②趁热过滤所得的滤渣的主要成分为
(3)向步骤②所得滤液中滴加几滴KSCN溶液,无明显现象,是因为
(4)向滤液中滴加少量稀硫酸,分批加入
 ,边加边搅拌,直到出现少量气泡。滤液中开始时发生反应的离子方程式为
,边加边搅拌,直到出现少量气泡。滤液中开始时发生反应的离子方程式为
(5)经上述处理后的溶液先水解后聚合得到红棕色黏稠液体即聚合硫酸铁,则水解产生
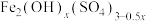 的化学方程式为
的化学方程式为
您最近一年使用:0次
18-19高三上·天津滨海新·期中
名校
解题方法
6 . 氢氧化铁与HI溶液反应仅能发生中和反应。(______)
您最近一年使用:0次
2022·湖南·模拟预测
解题方法
7 . 某小组探究FeCl3和Na2S竟色反应。
【查阅资料】
①硫单质微溶于乙醇,难溶于水;
②FeS、Fe2S3均为黑色固体,难溶于水:
③Fe3++6F-=[FeF6]3-,[FeF6]3-为无色离子。
【设计实验】
下列推断正确的是
【查阅资料】
①硫单质微溶于乙醇,难溶于水;
②FeS、Fe2S3均为黑色固体,难溶于水:
③Fe3++6F-=[FeF6]3-,[FeF6]3-为无色离子。
【设计实验】
| 序号 | I | II | III |
| 操作 | 在1mL0.1mol·L-1Na2S溶液中加入1mL0.1mol·L-1FeCl3溶液 | 在1.5mL0.1mol·L-1 溶液中加入0.5mL0.1mol·L-1FeCl3溶液 溶液中加入0.5mL0.1mol·L-1FeCl3溶液 | 在2mLlmol·L-1NaF溶液中加入0.5mL0.1mol·L-1FeCl3溶液,得无色溶液,再加入1.5mL0.1mol·L-1Na2S溶液 |
| 现象 | 迅速产生黑色沉淀X,振荡,黑色沉淀溶解,放出臭鸡蛋气味气体,最终得到棕黄色浊液Y | 产生棕黑色沉淀Z | 产生黑色沉淀W |
| 结论 | 分离Y得到Fe(OH)3和S | 经检验,Z的主要成分是Fe2S3,含少量Fe(OH)3 | 经检验,W为Fe2S3 |
| A.黑色沉淀X溶解只发生复分解反应 |
| B.实验II不生成S可能是氧化还原速率较大 |
| C.生成黑色沉淀W的反应为2Fe3++3S2-=Fe2S3↓ |
D.反应物中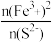 越小,氧化还原的趋势越小 越小,氧化还原的趋势越小 |
您最近一年使用:0次
21-22高一·全国·课时练习
8 . 将FeCl3溶液滴加到KI-淀粉试纸上,试纸变蓝色,发生反应的离子方程式为:_______ 。
您最近一年使用:0次
2022·广东·二模
名校
解题方法
9 . 下列关于生产生活的描述Ⅰ和Ⅱ均正确且有因果关系的是
| 选项 | 描述Ⅰ | 描述Ⅱ |
| A | 合成氨工业需要科研人员不断寻找高效的催化剂 | 催化剂可以提高平衡转化率 |
| B | 疫情防控环境卫生消杀常选用84消毒液 | 其主要成分NaClO具有强氧化性 |
| C | 铁质槽罐车可储运浓硝酸,但不能储运稀硝酸 | 稀硝酸比浓硝酸氧化性更强 |
| D | 用FeCl3溶液刻蚀电路板 | Cu与FeCl3溶液发生了置换反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-29更新
|
774次组卷
|
5卷引用:专项06 元素及其化合物-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)
(已下线)专项06 元素及其化合物-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题广东省深圳市福田区红岭中学2022-2023学年高三上学期第一次统一考试化学试题(已下线)化学(广东B卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)化学(广东卷03)-2024年高考押题预测卷
21-22高一下·湖南长沙·期中
名校
解题方法
10 . 印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。下列说法正确的是
| A.用KSCN溶液可检验腐蚀后溶液中的Fe2+ |
| B.Fe3+能溶解Cu,说明金属性Cu>Fe |
| C.当有1mol电子转移时,溶液中Cu2+增加1mol |
| D.腐蚀后溶液中的金属阳离子有Fe3+、Fe2+、Cu2+ |
您最近一年使用:0次
2022-04-26更新
|
480次组卷
|
3卷引用:第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)湖南省长沙市长郡中学2021-2022学年高一下学期期中考试化学试题上海市嘉定区第一中学2021-2022学年高一下学期质量诊断二 化学试题



