2023高一·全国·专题练习
解题方法
1 . 氯化铁可用于金属蚀刻,如日常生活中不锈钢广告牌上的图形和文字就可用氯化铁溶液来蚀刻。
(1)写出氯化铁溶液蚀刻铁制品时发生反应的离子方程式。_________
(2)用化学方程式解释氯化铁蚀刻铜箔电路板的反应原理。_________
(1)写出氯化铁溶液蚀刻铁制品时发生反应的离子方程式。
(2)用化学方程式解释氯化铁蚀刻铜箔电路板的反应原理。
您最近一年使用:0次
2 . 在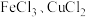 混合溶液中,加入铁粉与铜粉的混合物。
混合溶液中,加入铁粉与铜粉的混合物。
(1)若金属无剩余,则溶液中一定存在的金属阳离子有_______ ,可能存在的有_______ 。
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有_______ ,一定不存在_______ 。
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有_______ ,可能存在的有_______ ,一定不存在_______ 。
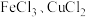 混合溶液中,加入铁粉与铜粉的混合物。
混合溶液中,加入铁粉与铜粉的混合物。(1)若金属无剩余,则溶液中一定存在的金属阳离子有
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
3 . 将 溶液和
溶液和 溶液混合(写离子方程式)
溶液混合(写离子方程式)_______ 。
 溶液和
溶液和 溶液混合(写离子方程式)
溶液混合(写离子方程式)
您最近一年使用:0次
21-22高一·全国·课时练习
4 . 将FeCl3溶液滴加到KI-淀粉试纸上,试纸变蓝色,发生反应的离子方程式为:_______ 。
您最近一年使用:0次
20-21高一下·福建福州·期末
名校
5 . 某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如图:
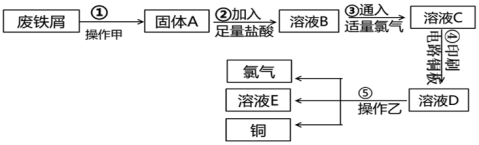
请回答下列问题:
(1)步骤①中操作甲是加饱和碳酸钠溶液并加热其作用是___________ 。
(2)写出步骤②中生成Fe2+的离子方程式___________ 。(写一个即可)
(3)若将③改加入H2O2,写出反应的离子方程式:___________ 。
(4)若溶液B中只含有Fe2+而不含Fe3+,可证明该事实的实验方法是___________ (填序号)。
①先加氯水,后加KSCN溶液后显红色
②先加KSCN溶液,不显红色,再加氯水后显红色
③滴加NaOH溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
④只滴加KSCN溶液不显红色
A.①② B.②③ C.③④ D.①④
(5)溶液D中可能含有的金属阳离子___________ 。
(6)若除去氯化铜中的氯化铁可以加入试剂___________ 。(填序号,可选的试剂有A.NaOH B.CuO C.Fe粉 D.Cu(OH)2 E.CaO)

请回答下列问题:
(1)步骤①中操作甲是加饱和碳酸钠溶液并加热其作用是
(2)写出步骤②中生成Fe2+的离子方程式
(3)若将③改加入H2O2,写出反应的离子方程式:
(4)若溶液B中只含有Fe2+而不含Fe3+,可证明该事实的实验方法是
①先加氯水,后加KSCN溶液后显红色
②先加KSCN溶液,不显红色,再加氯水后显红色
③滴加NaOH溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
④只滴加KSCN溶液不显红色
A.①② B.②③ C.③④ D.①④
(5)溶液D中可能含有的金属阳离子
(6)若除去氯化铜中的氯化铁可以加入试剂
您最近一年使用:0次
2021-07-26更新
|
773次组卷
|
3卷引用:专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)
(已下线)专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)福建省福州市八县一中2020-2021学年高一年下学期期末考化学试题江苏省海门中学2021-2022学年度高二上学期10月月考化学试题
解题方法
6 . 已知反应2FeCl2+Cl2=2FeCl3。现有铁粉、氯气、氧化铁和盐酸四种物质,试用三种方法制取FeCl3(用化学方程式表示)。
(1)___________________ 。
(2)__________________ 。
(3)_______________ 。
(1)
(2)
(3)
您最近一年使用:0次
18-19高三上·北京·期中
名校
7 . 某兴趣小组研究I2与FeCl2溶液的反应。
配制FeCl2溶液:向0.1 mol·L-1FeCl3溶液中加入足量铁粉,充分振荡,备用。
(1)FeCl3溶液与铁粉反应的离子方程式是________ 。
(2)检验FeCl3完全反应的实验方案是____________ 。
(3)设计如下实验,研究I2是否能够氧化FeCl2:
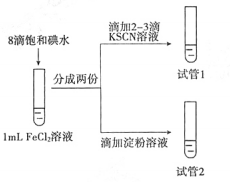
实验现象:试管1溶液变红,试管2溶液呈现较浅的蓝色。
实验结论:I2能够氧化FeCl2。
①有的同学认为上述实验现象不足以得出上述结论,原因是________ 。
②欲证实实验结论,再次设计对比实验。实验方案和相应的现象是________ 。
(4)继续进行实验:
①针对Ⅱ中现象,小组同学提出假设:在一定量KI的存在下,I-+I2 I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):
I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):____________

②应用化学平衡移动原理,结合离子方程式,解释实验I中溶液红色褪去的原因:_______________________ 。
配制FeCl2溶液:向0.1 mol·L-1FeCl3溶液中加入足量铁粉,充分振荡,备用。
(1)FeCl3溶液与铁粉反应的离子方程式是
(2)检验FeCl3完全反应的实验方案是
(3)设计如下实验,研究I2是否能够氧化FeCl2:

实验现象:试管1溶液变红,试管2溶液呈现较浅的蓝色。
实验结论:I2能够氧化FeCl2。
①有的同学认为上述实验现象不足以得出上述结论,原因是
②欲证实实验结论,再次设计对比实验。实验方案和相应的现象是
(4)继续进行实验:
| 实验 | 实验操作 | 实验现象 |
| I | 向试管1中加入KI固体,充分振荡 | 溶液红色完全褪去,变为黄色。 |
| Ⅱ | 向I中所得的黄色溶液中加入0.5mL CCl4,充分振荡、静置 | 水层仍为黄色,CCl4层几乎无色。 |
①针对Ⅱ中现象,小组同学提出假设:在一定量KI的存在下,I-+I2
 I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):
I3-,使CCl4很难萃取黄色溶液中的I2。该小组同学设计实验,证实了I-和I2可以反应。在下图虚框中,将实验方案补充完整(按试题图示方式呈现):
②应用化学平衡移动原理,结合离子方程式,解释实验I中溶液红色褪去的原因:
您最近一年使用:0次
2014·山东·高考真题
真题
名校
8 . 离子液体是一种室温熔融盐,为非水体系.由有机阳离子、Al2Cl7﹣和AlCl4﹣组成的离子液体做电解液时,可在钢制品上电镀铝.
(1)钢制品应接电源的_______ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为________________ ,若改用AlCl3水溶液作电解液,则阴极产物为_____________ .
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为________ mol.
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有__________
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,_______ (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是__________________ (用离子方程式说明).
(1)钢制品应接电源的
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a、KCl b、KClO3 c、MnO2 d、Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近一年使用:0次
2016-12-08更新
|
2512次组卷
|
6卷引用:2019高考备考二轮复习精品资料-专题10 电化学及其应用(教学案)
(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(教学案)2014年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)2015-2016学年浙江省湖州中学高二上学期期中化学试卷2016-2017学年河北省唐山一中高二上10月月考化学卷贵州省习水县一中2019届高三上学期12月份考试理科综合化学试题云南省广南二中2018-2019学年高二6月考试化学试题



