1 . 按要求完成下列填空。
(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生成水煤气,其中还原剂是_______ (填化学式)。
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2+3H2 2NH3。
2NH3。
①合成氨的反应中的能量变化如图所示。该反应是_______ 反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量_______ (填“大于”或“小于”)生成物化学键形成放出的总能量。

②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是_______ (填字母)。
a.容器中N2、H2、NH3共存
b.N2、H2、NH3的物质的量之比为1∶3∶2
c.容器中的压强不随时间变化
d.N2、NH3浓度相等
(3)下列各反应中,符合如图所示能量变化的是_______ (填字母)。

a.H2和Cl2的反应
b.Al和盐酸的反应
c.Na和H2O的反应
d.Ba(OH)2·8H2O和NH4Cl的反应
(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生成水煤气,其中还原剂是
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2+3H2
 2NH3。
2NH3。①合成氨的反应中的能量变化如图所示。该反应是

②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是
a.容器中N2、H2、NH3共存
b.N2、H2、NH3的物质的量之比为1∶3∶2
c.容器中的压强不随时间变化
d.N2、NH3浓度相等
(3)下列各反应中,符合如图所示能量变化的是

a.H2和Cl2的反应
b.Al和盐酸的反应
c.Na和H2O的反应
d.Ba(OH)2·8H2O和NH4Cl的反应
您最近一年使用:0次
2 . 如图表示298.15K时,N2、H2与NH3的平均能量与合成氨反应的活化能的曲线图,据图回答下列问题:

(1)若反应中生成2mol氨,则反应___ (填“吸热”或“放热”) ____ kJ。
(2)图中曲线_______ (填“a”或“b”)表示加入铁触媒的能量变化曲线,铁触媒能加快反应速率的原理是________ 。
(3)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如图所示。若曲线a对应的温度为500℃,则曲线b对应的温度可能是 (填字母)。

(4)合成氨所需的氢气可由甲烷与水反应制备。发生反应为CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0。一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
①表中x=________ mol·L-1;前2min内CH4的平均反应速率为_________ 。
②反应在3~4min之间,氢气的物质的量增多的原因可能是__________ (填字母)。
A.充入水蒸气 B.升高温度 C.使用催化剂 D.充入氢气

(1)若反应中生成2mol氨,则反应
(2)图中曲线
(3)合成氨反应中平衡混合物中氨气的体积分数与压强、温度的关系如图所示。若曲线a对应的温度为500℃,则曲线b对应的温度可能是 (填字母)。

| A.600℃ | B.550℃ | C.500℃ | D.450℃ |
| t/min | CH4/mol·L-1 | H2O/mol·L-1 | CO/mol·L-1 | H2/mol·L-1 |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.3 |
| 3 | n1 | n2 | n3 | 0.3 |
| 4 | 0.09 | 0.19 | x | 0.33 |
①表中x=
②反应在3~4min之间,氢气的物质的量增多的原因可能是
A.充入水蒸气 B.升高温度 C.使用催化剂 D.充入氢气
您最近一年使用:0次
2022-03-18更新
|
408次组卷
|
3卷引用:河北省张家口市第一中学2021-2022学年高二上学期10月月考化学试题
名校
3 . 有机物催化脱氢制备氢气和化工原料是当前石化工业研究的重要课题之一、
(1)以甲烷、水蒸气为原料进行催化重整是制氢的常见方法之一,过程可能涉及反应:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ∙mol−1
CO(g)+H2O(g)=CO2(g)+H2(g) △H2=−41.1 kJ∙mol−1
CH4(g)=C(g)+2H2(g) △H3=+74.8 kJ∙mol−1
①反应C(g)+2H2O(g)=CO2(g)+2H2(g) △H4=___________ kJ·mol-1
②向原料中添加正硅酸锂Li4SiO4作为CO2的吸附剂,除产生氢气外还生成两种盐,写出该反应的方程式___________ 。
(2)甲基环己烷催化脱氢(

 +3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是
+3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是___________ 。

(3)以H2O、CaBr2、Fe3O4为原料进行气固相反应可以实现水的分解制得氢气,其反应原理如图2所示。反应“①”中生成3molHBr,生成氢气的物质的量为_______ ,从原料到O2的生成过程可描述为_______ 。
(1)以甲烷、水蒸气为原料进行催化重整是制氢的常见方法之一,过程可能涉及反应:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2 kJ∙mol−1
CO(g)+H2O(g)=CO2(g)+H2(g) △H2=−41.1 kJ∙mol−1
CH4(g)=C(g)+2H2(g) △H3=+74.8 kJ∙mol−1
①反应C(g)+2H2O(g)=CO2(g)+2H2(g) △H4=
②向原料中添加正硅酸锂Li4SiO4作为CO2的吸附剂,除产生氢气外还生成两种盐,写出该反应的方程式
(2)甲基环己烷催化脱氢(


 +3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是
+3H2)是石油工业制氢常见方法,以Ni−Cu为催化剂,固定反应温度为650K,以氮气为载气,在不同载气流速情况下,甲基环己烷脱氢转化率如图1所示,b点转化率能与a点保持相当的原因是
(3)以H2O、CaBr2、Fe3O4为原料进行气固相反应可以实现水的分解制得氢气,其反应原理如图2所示。反应“①”中生成3molHBr,生成氢气的物质的量为
您最近一年使用:0次
2021-12-14更新
|
974次组卷
|
4卷引用:江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题
江苏省南通市海门区2021-2022学年高三第二次诊断测试化学试题(已下线)黄金卷6-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)江苏省南京市第九中学2023-2024学年高二上学期期末化学试卷
4 . 苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反应:
I.主反应: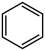 (g)+3H2(g)⇌
(g)+3H2(g)⇌ 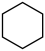 (g)
(g) 
II.副反应: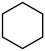 (g)⇌
(g)⇌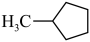 (g)
(g) 
回答下列问题:
(1)已知:III.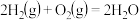

IV.2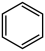 (g)+15O2(g)=12CO2(g)+6H2O(l)
(g)+15O2(g)=12CO2(g)+6H2O(l) 
V.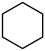 (g)+9O2(g)=6CO2(g)+6H2O(l)
(g)+9O2(g)=6CO2(g)+6H2O(l) 
则
___________ (用 、
、 和
和 表示)。
表示)。
(2)有利于提高平衡体系中环己烷体积分数的措施有___________。
(3)反应I在管式反应器中进行,实际投料往往在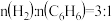 的基础上适当增大
的基础上适当增大 用量,其目的是
用量,其目的是___________ 。
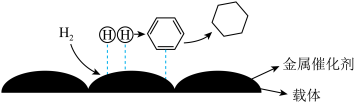
(4)氢原子和苯分子吸附在催化剂表面活性中心时,才能发生反应,机理如图。当 中混有微量
中混有微量 或CO等杂质时,会导致反应I的产率降低,推测其可能原因为
或CO等杂质时,会导致反应I的产率降低,推测其可能原因为___________ 。
(5)恒压反应器中,按照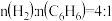 投料,发生I、II反应,总压为
投料,发生I、II反应,总压为 ,平衡时苯的转化率为α,环己烷的分压为p,则反应I的
,平衡时苯的转化率为α,环己烷的分压为p,则反应I的
___________ (列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
I.主反应:
 (g)+3H2(g)⇌
(g)+3H2(g)⇌  (g)
(g) 
II.副反应:
 (g)⇌
(g)⇌ (g)
(g) 
回答下列问题:
(1)已知:III.
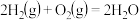

IV.2
 (g)+15O2(g)=12CO2(g)+6H2O(l)
(g)+15O2(g)=12CO2(g)+6H2O(l) 
V.
 (g)+9O2(g)=6CO2(g)+6H2O(l)
(g)+9O2(g)=6CO2(g)+6H2O(l) 
则

 、
、 和
和 表示)。
表示)。(2)有利于提高平衡体系中环己烷体积分数的措施有___________。
| A.适当升温 | B.适当降温 | C.适当加压 | D.适当减压 |
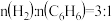 的基础上适当增大
的基础上适当增大 用量,其目的是
用量,其目的是(4)氢原子和苯分子吸附在催化剂表面活性中心时,才能发生反应,机理如图。当
 中混有微量
中混有微量 或CO等杂质时,会导致反应I的产率降低,推测其可能原因为
或CO等杂质时,会导致反应I的产率降低,推测其可能原因为
(5)恒压反应器中,按照
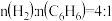 投料,发生I、II反应,总压为
投料,发生I、II反应,总压为 ,平衡时苯的转化率为α,环己烷的分压为p,则反应I的
,平衡时苯的转化率为α,环己烷的分压为p,则反应I的
您最近一年使用:0次
2021-12-07更新
|
650次组卷
|
2卷引用:辽宁省实验中学2021-2022学年高二上学期期中考试化学试题
5 . 碳和氮的化合物是广泛的化工原料,回答下列问题:
I.在一定体积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度t的关系如下表:
,其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应为反应___________ (填“吸热”、“放热”)。
(2)某温度下,平衡浓度符合下式: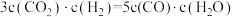 ,试判断此时的温度为
,试判断此时的温度为___________ ℃。
(3)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 ,
, ,
, ,
, ,则下一时刻,
,则下一时刻,
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关说法正确的是___________。
II.的二聚体 是火箭中常用氧化剂。完成下列问题。
是火箭中常用氧化剂。完成下列问题。
(5)在1000K下,在某恒容容器中发生下列反应: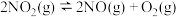 ,将一定量的
,将一定量的 放入恒容密闭容器中,测得其平衡转化率
放入恒容密闭容器中,测得其平衡转化率 随温度变化如图所示。图中a点对应温度下,已知
随温度变化如图所示。图中a点对应温度下,已知 的起始压强
的起始压强 为120KPa,列式计算该温度下反应的平衡常数
为120KPa,列式计算该温度下反应的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。

I.在一定体积的密闭容器中,进行如下化学反应:
 ,其化学平衡常数K和温度t的关系如下表:
,其化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为反应
(2)某温度下,平衡浓度符合下式:
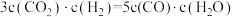 ,试判断此时的温度为
,试判断此时的温度为(3)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为
 ,
, ,
, ,
, ,则下一时刻,
,则下一时刻,
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关说法正确的是___________。
| A.反应物转化率增大 | B.逆反应速率增大 |
| C.各物质的比例不变 | D. 增大、 增大、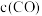 减小 减小 |
II.的二聚体
 是火箭中常用氧化剂。完成下列问题。
是火箭中常用氧化剂。完成下列问题。(5)在1000K下,在某恒容容器中发生下列反应:
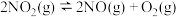 ,将一定量的
,将一定量的 放入恒容密闭容器中,测得其平衡转化率
放入恒容密闭容器中,测得其平衡转化率 随温度变化如图所示。图中a点对应温度下,已知
随温度变化如图所示。图中a点对应温度下,已知 的起始压强
的起始压强 为120KPa,列式计算该温度下反应的平衡常数
为120KPa,列式计算该温度下反应的平衡常数

您最近一年使用:0次
解题方法
6 . 利用工业废气CO2制甲醇Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1,可以一定程度摆脱当下对化石燃料的依赖。用CO2为碳源制备甲醇,为早日实现“碳达峰、碳中和”提供了一种较好的研究方向。
CH3OH(g)+H2O(g) △H1,可以一定程度摆脱当下对化石燃料的依赖。用CO2为碳源制备甲醇,为早日实现“碳达峰、碳中和”提供了一种较好的研究方向。
(1)上述反应的△H1___ 0(填“>”或“<”),理由是___ 。
(2)在VL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生上述反应,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势___ 。

(3)将1.0molCO2和3.0molH2充入2L恒容密闭容器中,使其按反应Ⅰ进行,在不同催化剂作用下,相同时间内CO2的转化率随温度变化如图所示。下列说法正确的是___ 。

(4)某工业废气中含CO2 6.76%,含CO 4.5×10-50%,请结合以下化学方程式:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
Ⅱ.CO(g)+2H2(g) CH3OH(g) △H2(2△H1=△H2)
CH3OH(g) △H2(2△H1=△H2)
分析为何工业废气制甲醇选取CO2而不选CO作碳源:___ 。
(5)现向恒温恒压(0.1MPa)的密闭容器中充入1mol CO2,3mol H2和6mol He,上述反应达平衡时,测得CO2的转化率为0.2,则该反应的Kp=___ MPa-2。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,结果保留小数点后1位)
(6)CO2制备CH3OH的过程中,往往伴随着另一反应发生:CO2(g)+H2(g) CO(g)+H2O(g) △H3=40.9kJ•mol-1,从而导致CH3OH的选择性下降,有研究表明,在原料气中掺入适量CO,能提高CH3OH的选择性,试说明其可能的原因:
CO(g)+H2O(g) △H3=40.9kJ•mol-1,从而导致CH3OH的选择性下降,有研究表明,在原料气中掺入适量CO,能提高CH3OH的选择性,试说明其可能的原因:___ 。
 CH3OH(g)+H2O(g) △H1,可以一定程度摆脱当下对化石燃料的依赖。用CO2为碳源制备甲醇,为早日实现“碳达峰、碳中和”提供了一种较好的研究方向。
CH3OH(g)+H2O(g) △H1,可以一定程度摆脱当下对化石燃料的依赖。用CO2为碳源制备甲醇,为早日实现“碳达峰、碳中和”提供了一种较好的研究方向。(1)上述反应的△H1
(2)在VL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生上述反应,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势

(3)将1.0molCO2和3.0molH2充入2L恒容密闭容器中,使其按反应Ⅰ进行,在不同催化剂作用下,相同时间内CO2的转化率随温度变化如图所示。下列说法正确的是

| A.T3对应的平衡常数小于T4对应的平衡常数 |
| B.根据图中曲线分析,催化剂Ⅰ的催化效果好 |
| C.b点v正可能等于v逆 |
| D.a点的转化率比c点高可能的原因是该反应为放热反应,升温平衡逆向移动,转化率降低 |
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1Ⅱ.CO(g)+2H2(g)
 CH3OH(g) △H2(2△H1=△H2)
CH3OH(g) △H2(2△H1=△H2)分析为何工业废气制甲醇选取CO2而不选CO作碳源:
(5)现向恒温恒压(0.1MPa)的密闭容器中充入1mol CO2,3mol H2和6mol He,上述反应达平衡时,测得CO2的转化率为0.2,则该反应的Kp=
(6)CO2制备CH3OH的过程中,往往伴随着另一反应发生:CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=40.9kJ•mol-1,从而导致CH3OH的选择性下降,有研究表明,在原料气中掺入适量CO,能提高CH3OH的选择性,试说明其可能的原因:
CO(g)+H2O(g) △H3=40.9kJ•mol-1,从而导致CH3OH的选择性下降,有研究表明,在原料气中掺入适量CO,能提高CH3OH的选择性,试说明其可能的原因:
您最近一年使用:0次
7 . 氢气是一种理想的绿色能源,有科学家预言,氢能将成为人类的主要能源。已知以水为原料通过下列途径均可制得氢气。
ⅰ)太阳光催化分解水:
ⅱ)焦炭与水反应:
ⅲ)甲烷与水反应:
(1)反应ⅰ中主要的能量转化为___________ ;你认为通过此途径进行H2工业化生产的最突出优点是___________ 。
(2)相同温度压强下,若分别以ⅰ、ⅱ反应生成1mol H2,反应ⅱ比ⅰ要少吸收___________ 热量;你认为ⅱ反应需要吸热较小的原因可能是___________ 。
(3)①写出反应ⅲ的化学平衡常数的表达式:
___________ ;
②一定温度下,ⅲ反应中使用催化剂后,下列物理量能保持不变的有___________ 。
a.焓变 b.反应活化能Ea c.活化分子百分比 d.平衡常数K3
b.反应活化能Ea c.活化分子百分比 d.平衡常数K3
(4)①利用上述热化学方程式,推测反应
___________ ;
②以 为燃料、KOH溶液为电解液的燃料电池,负极的电极反应式为
为燃料、KOH溶液为电解液的燃料电池,负极的电极反应式为___________ 。
ⅰ)太阳光催化分解水:

ⅱ)焦炭与水反应:

ⅲ)甲烷与水反应:

(1)反应ⅰ中主要的能量转化为
(2)相同温度压强下,若分别以ⅰ、ⅱ反应生成1mol H2,反应ⅱ比ⅰ要少吸收
(3)①写出反应ⅲ的化学平衡常数的表达式:

②一定温度下,ⅲ反应中使用催化剂后,下列物理量能保持不变的有
a.焓变
 b.反应活化能Ea c.活化分子百分比 d.平衡常数K3
b.反应活化能Ea c.活化分子百分比 d.平衡常数K3(4)①利用上述热化学方程式,推测反应

②以
 为燃料、KOH溶液为电解液的燃料电池,负极的电极反应式为
为燃料、KOH溶液为电解液的燃料电池,负极的电极反应式为
您最近一年使用:0次
2021高三·全国·专题练习
8 . 实验测得反应溶液的pH、温度对铁黄产率的影响如图所示。反应温度宜选择___________ ;pH大于4.5时铁黄产率降低的主要原因可能是___________ 。


您最近一年使用:0次
解题方法
9 . 研究CO2的再利用有利于低碳减排的同时获得新的能源物质。如一定条件下,CO2加氢可制得甲醇: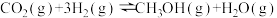
 。回答下列问题:
。回答下列问题:
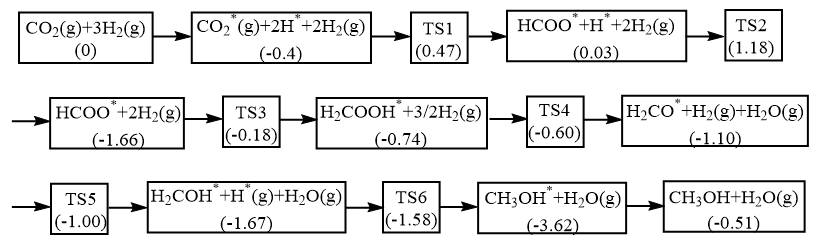
(1)我国科研人员研究的该反应历程如图,吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态,括号里的数字表示微粒的相对总能量(单位为eV)。
该反应
___________ 0(填“>”或“<”);该历程中总反应的决速步方程式为___________ 。
(2)T℃时,在一容积为2L的恒容密闭容器中充入2mol CO2和6molH2,测得不同时刻容器中的压强关系如下表所示:
①用H2表示该反应0~5min内的平均反应速率为___________ 。
②CO2的平衡转化率为___________ ;T℃时,该反应的平衡常数为___________ (保留一位小数)。
③其它条件不变,下列措施能同时增大反应速率和H2平衡转化率的是___________ (填标号)。
a.升高温度 b.按原比例再充入一定量CO2和H2
c.将 和
和 液化移出 d.缩小容器体积
液化移出 d.缩小容器体积
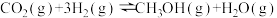
 。回答下列问题:
。回答下列问题:(1)我国科研人员研究的该反应历程如图,吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态,括号里的数字表示微粒的相对总能量(单位为eV)。

该反应

(2)T℃时,在一容积为2L的恒容密闭容器中充入2mol CO2和6molH2,测得不同时刻容器中的压强关系如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
 | 0.80 | 0.72 | 0.66 | 0.62 | 0.60 | 0.60 |
①用H2表示该反应0~5min内的平均反应速率为
②CO2的平衡转化率为
③其它条件不变,下列措施能同时增大反应速率和H2平衡转化率的是
a.升高温度 b.按原比例再充入一定量CO2和H2
c.将
 和
和 液化移出 d.缩小容器体积
液化移出 d.缩小容器体积
您最近一年使用:0次
名校
10 . 铬是造成水体重度污染的元素之一,水体除铬主要有还原沉淀法、离子交换法、光催化还原法等。
(1)还原沉淀法:向水体中加入FeSO4、CaSO3等将高毒性Cr(Ⅵ)还原为低毒性Cr(Ⅲ),再调节pH使Cr(Ⅲ)生成Cr(OH)3沉淀除去。
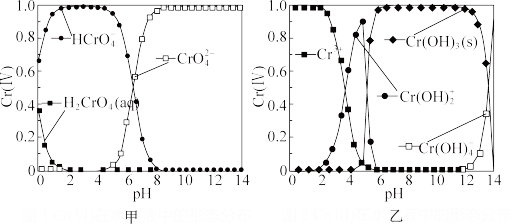
①Cr(Ⅵ)在水溶液中的存在形态分布如图甲所示。向pH=1.5的含Cr(Ⅵ)污水中加入FeSO4,发生的主要反应的离子方程式为___ 。
②Cr(Ⅲ)在水溶液中的存在形态分布如图乙所示。当pH>12时,铬去除率下降的原因可用离子方程式表示为___ 。
(2)离子交换法:用强碱性离子交换树脂(ROH)与含铬离子(CrO 、HCrO
、HCrO 等)发生离子交换。如与CrO
等)发生离子交换。如与CrO 的交换可表示为2ROH(s)+CrO
的交换可表示为2ROH(s)+CrO (aq)
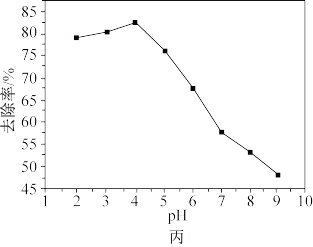
(aq) R2CrO4(s)+2OH-(aq)。Cr(Ⅵ)去除率与pH关系如图丙所示,当pH>4时,Cr(Ⅵ)去除率下降的原因是
R2CrO4(s)+2OH-(aq)。Cr(Ⅵ)去除率与pH关系如图丙所示,当pH>4时,Cr(Ⅵ)去除率下降的原因是___ 。
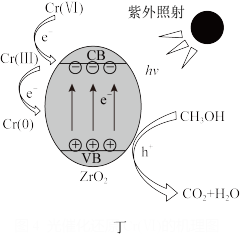
(3)光催化还原法:可能的反应机理如图丁所示,ZrO2纳米管为催化剂,在紫外光照射下,VB端光生空穴(h+)被牺牲剂甲醇(CH3OH)消耗。在紫外光照射下,甲醇还原Cr(Ⅵ)的过程可描述为:___ 。
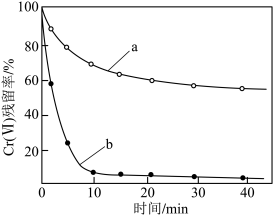
(4)金属也可用于还原废水中的Cr(Ⅵ)。其他条件相同时,用相同物质的量的Zn粉、Zn—Cu粉分别处理pH=2.5的含Cr(Ⅵ)废水,废水中Cr(Ⅵ)残留率随时间的变化如图所示。图中b对应的实验方法处理含Cr(Ⅵ)废水的效果更好,其原因是___ 。

(1)还原沉淀法:向水体中加入FeSO4、CaSO3等将高毒性Cr(Ⅵ)还原为低毒性Cr(Ⅲ),再调节pH使Cr(Ⅲ)生成Cr(OH)3沉淀除去。
①Cr(Ⅵ)在水溶液中的存在形态分布如图甲所示。向pH=1.5的含Cr(Ⅵ)污水中加入FeSO4,发生的主要反应的离子方程式为
②Cr(Ⅲ)在水溶液中的存在形态分布如图乙所示。当pH>12时,铬去除率下降的原因可用离子方程式表示为
(2)离子交换法:用强碱性离子交换树脂(ROH)与含铬离子(CrO
 、HCrO
、HCrO 等)发生离子交换。如与CrO
等)发生离子交换。如与CrO 的交换可表示为2ROH(s)+CrO
的交换可表示为2ROH(s)+CrO (aq)
(aq) R2CrO4(s)+2OH-(aq)。Cr(Ⅵ)去除率与pH关系如图丙所示,当pH>4时,Cr(Ⅵ)去除率下降的原因是
R2CrO4(s)+2OH-(aq)。Cr(Ⅵ)去除率与pH关系如图丙所示,当pH>4时,Cr(Ⅵ)去除率下降的原因是

(3)光催化还原法:可能的反应机理如图丁所示,ZrO2纳米管为催化剂,在紫外光照射下,VB端光生空穴(h+)被牺牲剂甲醇(CH3OH)消耗。在紫外光照射下,甲醇还原Cr(Ⅵ)的过程可描述为:
(4)金属也可用于还原废水中的Cr(Ⅵ)。其他条件相同时,用相同物质的量的Zn粉、Zn—Cu粉分别处理pH=2.5的含Cr(Ⅵ)废水,废水中Cr(Ⅵ)残留率随时间的变化如图所示。图中b对应的实验方法处理含Cr(Ⅵ)废水的效果更好,其原因是

您最近一年使用:0次



