名校
解题方法
1 . 氨性硫代硫酸盐浸金是一种高效的黄金浸取工艺。
(1)金可在硫代硫酸钠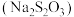 溶液中缓慢溶解:
溶液中缓慢溶解: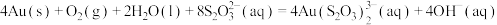 。
。
① 含Au
含Au 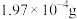 金矿中,加入
金矿中,加入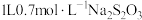 溶液,10小时后,金的浸出率为0.1%,则浸出过程
溶液,10小时后,金的浸出率为0.1%,则浸出过程 的平均消耗速率为
的平均消耗速率为___________  。
。
②为提高金的浸出速率,可采取的措施为___________ 。
(2) 可催化金在
可催化金在 溶液中的溶解,其电化学催化腐蚀过程如图所示。
溶液中的溶解,其电化学催化腐蚀过程如图所示。
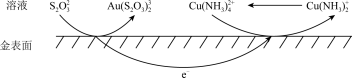
①负极的电极反应式为___________ 。
②正极可能的催化过程如下:
a.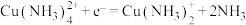
b.___________
③反应温度对金的浸出率影响如图所示。分析50℃时金浸出率最高的原因是___________ 。

(3)为研究浸金过程 与
与 的反应,进行如下实验:向
的反应,进行如下实验:向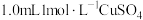 溶液中加入
溶液中加入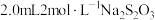 溶液,溶液从蓝色变为绿色,后逐渐变浅至无色。体系中涉及的反应如下:
溶液,溶液从蓝色变为绿色,后逐渐变浅至无色。体系中涉及的反应如下:
ⅰ.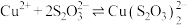 (绿色)
(绿色) 
ⅱ.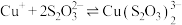 (无色)
(无色) 
ⅲ.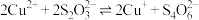

由实验现象可推测:反应ⅰ的速率___________ 反应ⅲ的速率(填“>”或“<”)、
___________  。
。
(4)若采用 催化硫代硫酸盐浸金,催化效果较
催化硫代硫酸盐浸金,催化效果较 差的原因是
差的原因是___________ 。
(1)金可在硫代硫酸钠
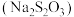 溶液中缓慢溶解:
溶液中缓慢溶解: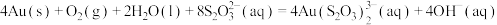 。
。①
 含Au
含Au 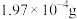 金矿中,加入
金矿中,加入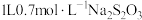 溶液,10小时后,金的浸出率为0.1%,则浸出过程
溶液,10小时后,金的浸出率为0.1%,则浸出过程 的平均消耗速率为
的平均消耗速率为 。
。②为提高金的浸出速率,可采取的措施为
(2)
 可催化金在
可催化金在 溶液中的溶解,其电化学催化腐蚀过程如图所示。
溶液中的溶解,其电化学催化腐蚀过程如图所示。
①负极的电极反应式为
②正极可能的催化过程如下:
a.
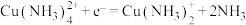
b.
③反应温度对金的浸出率影响如图所示。分析50℃时金浸出率最高的原因是

(3)为研究浸金过程
 与
与 的反应,进行如下实验:向
的反应,进行如下实验:向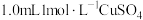 溶液中加入
溶液中加入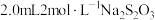 溶液,溶液从蓝色变为绿色,后逐渐变浅至无色。体系中涉及的反应如下:
溶液,溶液从蓝色变为绿色,后逐渐变浅至无色。体系中涉及的反应如下:ⅰ.
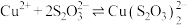 (绿色)
(绿色) 
ⅱ.
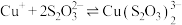 (无色)
(无色) 
ⅲ.
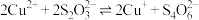

由实验现象可推测:反应ⅰ的速率

 。
。(4)若采用
 催化硫代硫酸盐浸金,催化效果较
催化硫代硫酸盐浸金,催化效果较 差的原因是
差的原因是
您最近一年使用:0次
2023-08-05更新
|
271次组卷
|
5卷引用:山东省泰安市2022-2023学年高二上学期期末考试化学试题
名校
2 . 气候变化是目前全球最重要、最紧迫的议题之一,中国作为负责任大国,自主提出力争2030年碳达峰、2060年碳中和的目标。 的综合利用是解决该问题的有效途径。
的综合利用是解决该问题的有效途径。
(1)将 转化为乙醇可以实现降碳,过程中发生的反应如下:
转化为乙醇可以实现降碳,过程中发生的反应如下:





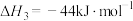
则

_______ 。
(2)研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。雨水中含有来自大气中的 ,溶于水的
,溶于水的 只有部分转化为
只有部分转化为 。已知25℃时,
。已知25℃时,
 正反应的速率可表示为
正反应的速率可表示为 ,逆反应的速率可表示为
,逆反应的速率可表示为 ,则
,则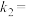
_______ (用含 的代数式表示)。
的代数式表示)。
(3)将 转化为甲醇也可以实现降碳。一定条件下,发生反应
转化为甲醇也可以实现降碳。一定条件下,发生反应 。往2L恒容密闭容器中充入
。往2L恒容密闭容器中充入 和
和 ,在甲、乙不同催化剂作用下,反应时间均为t min时,测得甲醇的物质的量分数随温度变化如图所示:
,在甲、乙不同催化剂作用下,反应时间均为t min时,测得甲醇的物质的量分数随温度变化如图所示:_______ (填“甲”或“乙”), 温度下甲醇的平均反应速率v=
温度下甲醇的平均反应速率v=_______ 。
②在甲催化作用下,甲醇的物质的量分数随温度的升高呈现如图变化的原因是_______ 。(不考虑催化剂失活问题)
③在 和
和 温度下,平衡常数
温度下,平衡常数
_______  (填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是
(填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是_______ 。
a.混合气体的密度不变 b.容器内压强不变
c. d.混合气体平均相对分子质量不变
d.混合气体平均相对分子质量不变
④已知气体分压=气体总压×气体的物质的量分数。 温度下,反应开始时容器中的总压为
温度下,反应开始时容器中的总压为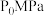 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
_______ (只列出计算式,不必化简)。
 的综合利用是解决该问题的有效途径。
的综合利用是解决该问题的有效途径。(1)将
 转化为乙醇可以实现降碳,过程中发生的反应如下:
转化为乙醇可以实现降碳,过程中发生的反应如下:




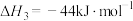
则


(2)研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。雨水中含有来自大气中的
 ,溶于水的
,溶于水的 只有部分转化为
只有部分转化为 。已知25℃时,
。已知25℃时,
 正反应的速率可表示为
正反应的速率可表示为 ,逆反应的速率可表示为
,逆反应的速率可表示为 ,则
,则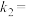
 的代数式表示)。
的代数式表示)。(3)将
 转化为甲醇也可以实现降碳。一定条件下,发生反应
转化为甲醇也可以实现降碳。一定条件下,发生反应 。往2L恒容密闭容器中充入
。往2L恒容密闭容器中充入 和
和 ,在甲、乙不同催化剂作用下,反应时间均为t min时,测得甲醇的物质的量分数随温度变化如图所示:
,在甲、乙不同催化剂作用下,反应时间均为t min时,测得甲醇的物质的量分数随温度变化如图所示:
 温度下甲醇的平均反应速率v=
温度下甲醇的平均反应速率v=②在甲催化作用下,甲醇的物质的量分数随温度的升高呈现如图变化的原因是
③在
 和
和 温度下,平衡常数
温度下,平衡常数
 (填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是
(填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是a.混合气体的密度不变 b.容器内压强不变
c.
 d.混合气体平均相对分子质量不变
d.混合气体平均相对分子质量不变④已知气体分压=气体总压×气体的物质的量分数。
 温度下,反应开始时容器中的总压为
温度下,反应开始时容器中的总压为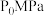 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
您最近一年使用:0次
2023-01-13更新
|
373次组卷
|
4卷引用:山东省临沂第一中学2021-2022学年高二上学期期末检测化学试题
名校
解题方法
3 . 全球大气 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①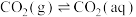
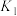
②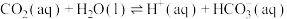

过程①的混合平衡常数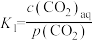 ,其中
,其中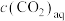 表示溶液中的
表示溶液中的 浓度,
浓度,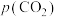 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
______ (填“增大”或“减小”);当大气压强为akPa,溶液中的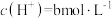 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为______ 。
(2)由 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应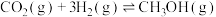
 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
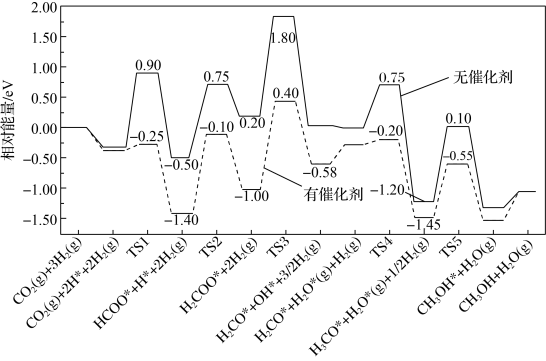
该反应历程中决速步骤的化学方程式为______ ,有催化剂时决速步骤的活化能为______ eV。
(3)一种脱除和利用工厂废气中 方法的示意图如下:
方法的示意图如下:
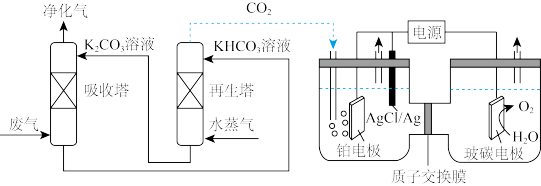
①某温度下,吸收塔中 溶液吸收一定量的
溶液吸收一定量的 后,溶液的
后,溶液的 ,则
,则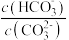 =
=______ (该温度下 的
的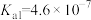 ,
,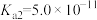 );
);
②再生塔中产生 的离子方程式为
的离子方程式为______ 。
③利用电化学原理将 同时转化为多种燃料(
同时转化为多种燃料( 、
、 、
、 及CO),将
及CO),将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为______ 。若铂电极上只生成6.4g ,则正极区产生气体标准状况下的体积为
,则正极区产生气体标准状况下的体积为______ L。
 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:(1)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
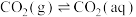
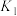
②
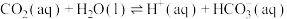

过程①的混合平衡常数
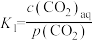 ,其中
,其中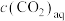 表示溶液中的
表示溶液中的 浓度,
浓度,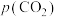 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
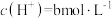 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为(2)由
 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应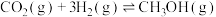
 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
该反应历程中决速步骤的化学方程式为
(3)一种脱除和利用工厂废气中
 方法的示意图如下:
方法的示意图如下:
①某温度下,吸收塔中
 溶液吸收一定量的
溶液吸收一定量的 后,溶液的
后,溶液的 ,则
,则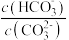 =
= 的
的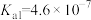 ,
,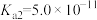 );
);②再生塔中产生
 的离子方程式为
的离子方程式为③利用电化学原理将
 同时转化为多种燃料(
同时转化为多种燃料( 、
、 、
、 及CO),将
及CO),将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为 ,则正极区产生气体标准状况下的体积为
,则正极区产生气体标准状况下的体积为
您最近一年使用:0次
2022-12-08更新
|
539次组卷
|
2卷引用:山东省烟台市2023届高三上学期期中学业水平诊断化学试卷
名校
4 . “绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。烟道气和汽车尾气(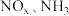 等)是造成雾霾天气的原因之一,对这些排放气的处理以及再利用是化学工作者研究的重要课题。请思考回答下列问题:
等)是造成雾霾天气的原因之一,对这些排放气的处理以及再利用是化学工作者研究的重要课题。请思考回答下列问题:
(1) 在一定条件下可发生分解:2N2O5(g)
在一定条件下可发生分解:2N2O5(g)  4NO2(g)+O2(g),一定温度下,在恒容密闭容器中充入一定量
4NO2(g)+O2(g),一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是_______(填字母)。
进行该反应,能判断反应已达到化学平衡状态的是_______(填字母)。
(2) 是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:
是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应: ,该反应中正反应速率
,该反应中正反应速率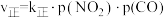 ,逆反应速率v逆=k逆·p(NO)·p(CO2),其中
,逆反应速率v逆=k逆·p(NO)·p(CO2),其中 为速率常数,则Kp为
为速率常数,则Kp为_______ (用 表示)。
表示)。
(3)1093K时,NO与 以物质的量2:1混合,置于某密闭容器中还能发生如下化学反应:
以物质的量2:1混合,置于某密闭容器中还能发生如下化学反应: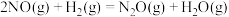 ,实验测得该反应速率方程(以
,实验测得该反应速率方程(以 为基准)为
为基准)为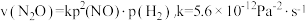 。某时刻测得体系中NO的分压为2.0kPa,则此时的反应速率为
。某时刻测得体系中NO的分压为2.0kPa,则此时的反应速率为_______ 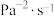 。
。
(4)在有氧和新型催化剂作用下, 和
和 可以反应生成
可以反应生成 ,将一定比例的
,将一定比例的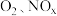 和
和 通入装有新型催化剂的反应器。测得相同时间内
通入装有新型催化剂的反应器。测得相同时间内 去除率随温度变化如图所示:
去除率随温度变化如图所示:
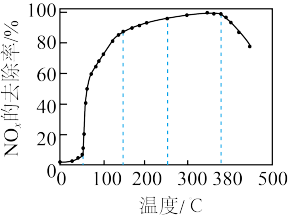
在50~250℃范围内, 的去除率先快速上升后变缓的主要原因是
的去除率先快速上升后变缓的主要原因是_______ ;380℃后去除率下降的可能原因是_______ 。
(5)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在催化剂存在下生成NO和副产物 的化学方程式如下:
的化学方程式如下:
I.
II.
已知:有效的转化率=
在1L恒容密闭容器中充入1molNH3、1.45mol ,在催化剂作用下发生两个竞争反应Ⅰ、Ⅱ,测得不同温度下反应相同时间有关物质的量关系如图所示:
,在催化剂作用下发生两个竞争反应Ⅰ、Ⅱ,测得不同温度下反应相同时间有关物质的量关系如图所示:
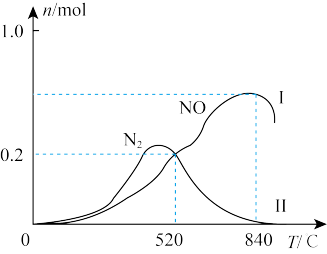
①520℃时,NH3的有效转化率=_______ (保留1位小数)。
②工业用氨催化氧化制备 ,选择的最佳温度是
,选择的最佳温度是_______ 。
③520℃时,反应Ⅱ的平衡常数K=_______ (保留3位有效数字)。
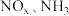 等)是造成雾霾天气的原因之一,对这些排放气的处理以及再利用是化学工作者研究的重要课题。请思考回答下列问题:
等)是造成雾霾天气的原因之一,对这些排放气的处理以及再利用是化学工作者研究的重要课题。请思考回答下列问题:(1)
 在一定条件下可发生分解:2N2O5(g)
在一定条件下可发生分解:2N2O5(g)  4NO2(g)+O2(g),一定温度下,在恒容密闭容器中充入一定量
4NO2(g)+O2(g),一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是_______(填字母)。
进行该反应,能判断反应已达到化学平衡状态的是_______(填字母)。A. 和 和 的浓度比保持不变 的浓度比保持不变 | B.容器中压强不再变化 |
| C.2v正 (NO2)=v逆 (N2O5) | D.气体的密度保持不变 |
 是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:
是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应: ,该反应中正反应速率
,该反应中正反应速率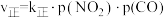 ,逆反应速率v逆=k逆·p(NO)·p(CO2),其中
,逆反应速率v逆=k逆·p(NO)·p(CO2),其中 为速率常数,则Kp为
为速率常数,则Kp为 表示)。
表示)。(3)1093K时,NO与
 以物质的量2:1混合,置于某密闭容器中还能发生如下化学反应:
以物质的量2:1混合,置于某密闭容器中还能发生如下化学反应: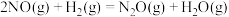 ,实验测得该反应速率方程(以
,实验测得该反应速率方程(以 为基准)为
为基准)为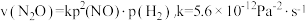 。某时刻测得体系中NO的分压为2.0kPa,则此时的反应速率为
。某时刻测得体系中NO的分压为2.0kPa,则此时的反应速率为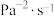 。
。(4)在有氧和新型催化剂作用下,
 和
和 可以反应生成
可以反应生成 ,将一定比例的
,将一定比例的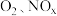 和
和 通入装有新型催化剂的反应器。测得相同时间内
通入装有新型催化剂的反应器。测得相同时间内 去除率随温度变化如图所示:
去除率随温度变化如图所示:
在50~250℃范围内,
 的去除率先快速上升后变缓的主要原因是
的去除率先快速上升后变缓的主要原因是(5)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在催化剂存在下生成NO和副产物
 的化学方程式如下:
的化学方程式如下:I.

II.

已知:有效的转化率=

在1L恒容密闭容器中充入1molNH3、1.45mol
 ,在催化剂作用下发生两个竞争反应Ⅰ、Ⅱ,测得不同温度下反应相同时间有关物质的量关系如图所示:
,在催化剂作用下发生两个竞争反应Ⅰ、Ⅱ,测得不同温度下反应相同时间有关物质的量关系如图所示:
①520℃时,NH3的有效转化率=
②工业用氨催化氧化制备
 ,选择的最佳温度是
,选择的最佳温度是③520℃时,反应Ⅱ的平衡常数K=
您最近一年使用:0次
2022-11-30更新
|
577次组卷
|
3卷引用:山东省济南市历城二中2022-2023学年高二上学期期中考试化学试题
名校
解题方法
5 .  是导致温室效应的主要气体,为减少
是导致温室效应的主要气体,为减少 对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:
对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:
(1)工业上用 与
与 反应合成甲醇(a和b均大于零):
反应合成甲醇(a和b均大于零):
①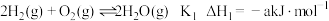 ;
;
②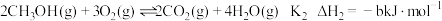 ;
;
③ 。
。
则
_______ (用含 的代数式表示),
的代数式表示),
_______  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
(2) 催化加氢合成乙烯:
催化加氢合成乙烯:
往某恒容密闭容器中,充入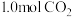 和
和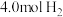 ,发生反应:
,发生反应: ,当反应达到平衡时,测得
,当反应达到平衡时,测得 的物质的量分数随温度的变化曲线如图所示:
的物质的量分数随温度的变化曲线如图所示:

①对于 ,下列说法正确的是
,下列说法正确的是_______ (填标号)。
A.该反应中反应物的总键能小于生成物的总键能
B.升高温度,该反应的 的值增大
的值增大
C.加入合适的催化剂,有利于提高 的转化率
的转化率
D.当混合气体的相对分子质量不再随时间而改变,则该反应达到平衡
②若反应达到平衡时,a点时容器内气体的总压强为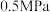 ,则该反应的平衡常数
,则该反应的平衡常数
_______  (列出计算式即可,用分压表示,分压=总压×物质的量分数)。
(列出计算式即可,用分压表示,分压=总压×物质的量分数)。
(3)草酸锌可应用于有机合成、电子工业等。工业上制取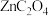 的原理如图所示(电解液不参加反应):
的原理如图所示(电解液不参加反应):
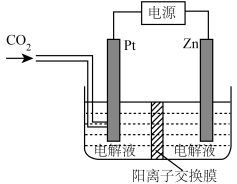
①该电池属于_______ (填“电解池”或“原电池”)。
②Pt电极上的电极反应式为_______ 。
③每转移0.2mol电子,此时消耗 的体积为
的体积为_______ L(标准状况下)。
(4) 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:_______ 。
 是导致温室效应的主要气体,为减少
是导致温室效应的主要气体,为减少 对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:
对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:(1)工业上用
 与
与 反应合成甲醇(a和b均大于零):
反应合成甲醇(a和b均大于零):①
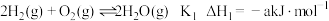 ;
;②
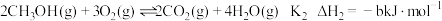 ;
;③
 。
。则

 的代数式表示),
的代数式表示),
 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(2)
 催化加氢合成乙烯:
催化加氢合成乙烯:往某恒容密闭容器中,充入
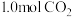 和
和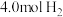 ,发生反应:
,发生反应: ,当反应达到平衡时,测得
,当反应达到平衡时,测得 的物质的量分数随温度的变化曲线如图所示:
的物质的量分数随温度的变化曲线如图所示:
①对于
 ,下列说法正确的是
,下列说法正确的是A.该反应中反应物的总键能小于生成物的总键能
B.升高温度,该反应的
 的值增大
的值增大C.加入合适的催化剂,有利于提高
 的转化率
的转化率D.当混合气体的相对分子质量不再随时间而改变,则该反应达到平衡
②若反应达到平衡时,a点时容器内气体的总压强为
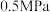 ,则该反应的平衡常数
,则该反应的平衡常数
 (列出计算式即可,用分压表示,分压=总压×物质的量分数)。
(列出计算式即可,用分压表示,分压=总压×物质的量分数)。(3)草酸锌可应用于有机合成、电子工业等。工业上制取
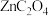 的原理如图所示(电解液不参加反应):
的原理如图所示(电解液不参加反应):
①该电池属于
②Pt电极上的电极反应式为
③每转移0.2mol电子,此时消耗
 的体积为
的体积为(4)
 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
名校
6 . 我国政府一直高度关注气候变化对国家和社会的影响,并积极推进碳减排的工作。其中, 的综合利用是目前研究的重要课题之一、请运用所学知识,回答下列问题:
的综合利用是目前研究的重要课题之一、请运用所学知识,回答下列问题:
 在一定催化剂条件下可以与
在一定催化剂条件下可以与 发生以下两个反应:
发生以下两个反应:
反应I:

反应II:

在恒压密闭容器中通入3
 、1
、1
 ,初始体积均为V L,分别在0.1
,初始体积均为V L,分别在0.1 和1
和1 下进行反应。分析温度对平衡体系中
下进行反应。分析温度对平衡体系中 、
、 、
、 的影响,设这三种气体物质的量分数之和为1,其中
的影响,设这三种气体物质的量分数之和为1,其中 和
和 的物质的量分数与温度变化关系如图所示。
的物质的量分数与温度变化关系如图所示。

(1)表示1 时
时 的物质的量分数随温度变化关系的曲线是
的物质的量分数随温度变化关系的曲线是_______ (填字母)。
(2)N点低于M点的原因是_______ 。
(3)分析200-400℃b、d曲线基本重合的原因_______ 。
(4)590℃条件下,t min反应达到平衡,平衡时容器的体积为_______ ,用压强变化表示的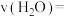
_______  ,反应II的
,反应II的 为
为_______ 。
 的综合利用是目前研究的重要课题之一、请运用所学知识,回答下列问题:
的综合利用是目前研究的重要课题之一、请运用所学知识,回答下列问题: 在一定催化剂条件下可以与
在一定催化剂条件下可以与 发生以下两个反应:
发生以下两个反应:反应I:


反应II:


在恒压密闭容器中通入3

 、1
、1
 ,初始体积均为V L,分别在0.1
,初始体积均为V L,分别在0.1 和1
和1 下进行反应。分析温度对平衡体系中
下进行反应。分析温度对平衡体系中 、
、 、
、 的影响,设这三种气体物质的量分数之和为1,其中
的影响,设这三种气体物质的量分数之和为1,其中 和
和 的物质的量分数与温度变化关系如图所示。
的物质的量分数与温度变化关系如图所示。
(1)表示1
 时
时 的物质的量分数随温度变化关系的曲线是
的物质的量分数随温度变化关系的曲线是(2)N点低于M点的原因是
(3)分析200-400℃b、d曲线基本重合的原因
(4)590℃条件下,t min反应达到平衡,平衡时容器的体积为
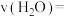
 ,反应II的
,反应II的 为
为
您最近一年使用:0次
2022-11-11更新
|
208次组卷
|
3卷引用:山东省菏泽市郓城第一中学2022-2023学年高二上学期期中考试化学试题
解题方法
7 . 合成氨工业涉及固体燃料的气化,需要研究 与
与 之间的转化。为了弄清其规律,让一定量的
之间的转化。为了弄清其规律,让一定量的 与足量碳在体积可变的密闭容器中反应:
与足量碳在体积可变的密闭容器中反应: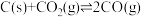
 ,测得压强、温度对
,测得压强、温度对 、
、 的平衡组成的影响如图所示,回答下列问题:
的平衡组成的影响如图所示,回答下列问题:
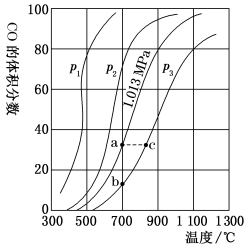
(1) 、
、 、
、 的大小关系是
的大小关系是_______ ,欲提高C与CO2反应中CO2的平衡转化率,应采取的措施为_______ 。图中a、b、c三点对应的平衡常数大小关系是_______ 。
(2)一定条件下,在 与足量碳反应所得平衡体系中加入
与足量碳反应所得平衡体系中加入 和适当催化剂,有下列反应发生:
和适当催化剂,有下列反应发生:
反应1: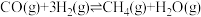
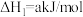
反应2: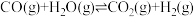
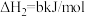
①则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是_______ 。
②已知 时相关化学键键能数据为:
时相关化学键键能数据为:
根据键能计算,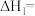
_______ 。
 与
与 之间的转化。为了弄清其规律,让一定量的
之间的转化。为了弄清其规律,让一定量的 与足量碳在体积可变的密闭容器中反应:
与足量碳在体积可变的密闭容器中反应: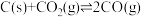
 ,测得压强、温度对
,测得压强、温度对 、
、 的平衡组成的影响如图所示,回答下列问题:
的平衡组成的影响如图所示,回答下列问题:
(1)
 、
、 、
、 的大小关系是
的大小关系是(2)一定条件下,在
 与足量碳反应所得平衡体系中加入
与足量碳反应所得平衡体系中加入 和适当催化剂,有下列反应发生:
和适当催化剂,有下列反应发生:反应1:
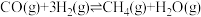
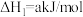
反应2:
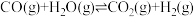
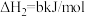
①则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是
②已知
 时相关化学键键能数据为:
时相关化学键键能数据为:| 化学键 | H-H | O-H | C-H | C≡O |
 | 436 | 465 | 413 | 1076 |
根据键能计算,
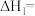
您最近一年使用:0次
名校
8 . 碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)已知反应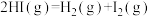 的
的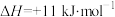 ,1 mol
,1 mol  、1 mol
、1 mol  分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1 molHI(g)分子中化学键断裂时需吸收的能量为
分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1 molHI(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(2)Bodensteins研究了下列反应: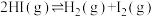 ,在716K时,气体混合物中碘化氢的物质的量分数
,在716K时,气体混合物中碘化氢的物质的量分数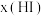 与反应时间t的关系如下表:
与反应时间t的关系如下表:
①根据上述实验结果,该反应的平衡常数K的计算式为:_______ 。
②上述反应中,正反应速率为 ,逆反应速率为
,逆反应速率为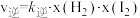 ,其中
,其中 、
、 为速率常数,若
为速率常数,若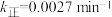 ,在t=40min时,
,在t=40min时,
_______ 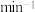 (保留三位有效数字)。如图(
(保留三位有效数字)。如图( ,T表示温度)所示a、b、c、d四条斜线中,能表示
,T表示温度)所示a、b、c、d四条斜线中,能表示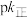 随T变化的是斜线
随T变化的是斜线_______ ,能表示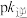 随T变化的是斜线,图中A、B、C、D点的坐标分别为m+4、m+2、m-2、m-4,则温度T1时化学平衡常数
随T变化的是斜线,图中A、B、C、D点的坐标分别为m+4、m+2、m-2、m-4,则温度T1时化学平衡常数
_______ 。

③由上述实验数据计算得到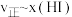 和
和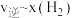 的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_______ 、_______ (填字母)

(1)已知反应
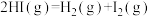 的
的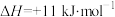 ,1 mol
,1 mol  、1 mol
、1 mol  分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1 molHI(g)分子中化学键断裂时需吸收的能量为
分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1 molHI(g)分子中化学键断裂时需吸收的能量为(2)Bodensteins研究了下列反应:
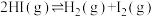 ,在716K时,气体混合物中碘化氢的物质的量分数
,在716K时,气体混合物中碘化氢的物质的量分数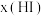 与反应时间t的关系如下表:
与反应时间t的关系如下表:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:
②上述反应中,正反应速率为
 ,逆反应速率为
,逆反应速率为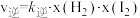 ,其中
,其中 、
、 为速率常数,若
为速率常数,若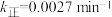 ,在t=40min时,
,在t=40min时,
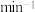 (保留三位有效数字)。如图(
(保留三位有效数字)。如图( ,T表示温度)所示a、b、c、d四条斜线中,能表示
,T表示温度)所示a、b、c、d四条斜线中,能表示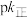 随T变化的是斜线
随T变化的是斜线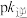 随T变化的是斜线,图中A、B、C、D点的坐标分别为m+4、m+2、m-2、m-4,则温度T1时化学平衡常数
随T变化的是斜线,图中A、B、C、D点的坐标分别为m+4、m+2、m-2、m-4,则温度T1时化学平衡常数

③由上述实验数据计算得到
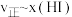 和
和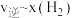 的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
您最近一年使用:0次
名校
解题方法
9 . 尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g) NH2COONH4(l)
NH2COONH4(l) [CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。
[CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应2NH3(g)+CO2(g)⇌[CO(NH2)2](s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
①NH3的平衡转化率为_______ 。
②能说明上述反应达到平衡状态的是_______ (填标号)。
A. n(CO2):n(NH3)=1:2
B. 混合气体的密度不再发生变化
C. 单位时间内消耗2molNH3,同时生成1molH2O
D. CO2的体积分数在混合气体中保持不变
③若10min时保持温度和压强不变,再向容器中同时充入0.5molCO2和0.5molH2O(g),则此时平衡____ (填正向移动,逆向移动或不移动)。
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)⇌[CO(NH2)2](s)+H2O(g),若原料气中 =m,测得m与CO2的平衡转化率(α)的关系如图所示。
=m,测得m与CO2的平衡转化率(α)的关系如图所示。
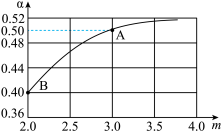
①若平衡时A点容器内总压强为0.5MPa,则上述反应的平衡常数Kp=_____ (MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②若平衡时A、B对应容器的压强相等,则A、B对应的容器中,起始时投入氨气的物质的量之比nA(NH3):nB(NH3)=____ 。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g)
 NH2COONH4(l)
NH2COONH4(l) [CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。
[CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。A. | B. |
C.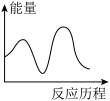 | D. |
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应2NH3(g)+CO2(g)⇌[CO(NH2)2](s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
①NH3的平衡转化率为
②能说明上述反应达到平衡状态的是
A. n(CO2):n(NH3)=1:2
B. 混合气体的密度不再发生变化
C. 单位时间内消耗2molNH3,同时生成1molH2O
D. CO2的体积分数在混合气体中保持不变
③若10min时保持温度和压强不变,再向容器中同时充入0.5molCO2和0.5molH2O(g),则此时平衡
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)⇌[CO(NH2)2](s)+H2O(g),若原料气中
 =m,测得m与CO2的平衡转化率(α)的关系如图所示。
=m,测得m与CO2的平衡转化率(α)的关系如图所示。
①若平衡时A点容器内总压强为0.5MPa,则上述反应的平衡常数Kp=
②若平衡时A、B对应容器的压强相等,则A、B对应的容器中,起始时投入氨气的物质的量之比nA(NH3):nB(NH3)=
您最近一年使用:0次
2022-10-08更新
|
384次组卷
|
3卷引用:山东省德州市第一中学2022-2023学年高二上学期10月月考化学试题
解题方法
10 . 我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的担当。高效经济性的 捕集及利用是有效应对全球气候变化、促进低碳社会构建的重要方法。由
捕集及利用是有效应对全球气候变化、促进低碳社会构建的重要方法。由 转化制甲醇具有重要的经济效益。
转化制甲醇具有重要的经济效益。
回答下列问题:
(1)反应 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注, 为过渡态)。
为过渡态)。
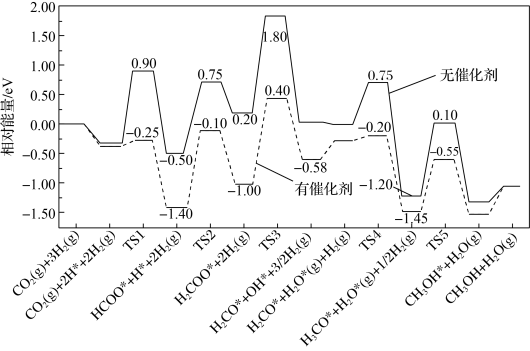
该反应的
_______ 0(填“>”“,”或“=”);该反应历程中决速步骤的化学方程式为_______ ,有催化剂时决速步骤的活化能为_______  。
。
(2)在 催化加氢制甲醇过程中除发生主反应Ⅰ:
催化加氢制甲醇过程中除发生主反应Ⅰ: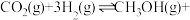
 外,还存在竞争反应Ⅱ:
外,还存在竞争反应Ⅱ: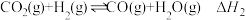 。已知甲醇选择性
。已知甲醇选择性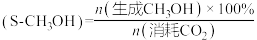 ,
, 的平衡转化率
的平衡转化率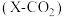 、甲醇的选择性
、甲醇的选择性 随温度、压强变化如图所示:
随温度、压强变化如图所示:

①由图可知压强大小关系:
_______ 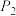 (填“>”“<”或“=”,下同),
(填“>”“<”或“=”,下同),
_______ 0。
② 时体系发生的反应主要是
时体系发生的反应主要是_______ (填“反应Ⅰ”或“反应Ⅱ”);图中a、b两点的反应速率
_______ 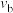 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③将 和
和 的混合气体通入反应器,在温度t、压强P的条件下进行反应。达到平衡状态时,
的混合气体通入反应器,在温度t、压强P的条件下进行反应。达到平衡状态时, 平衡转化率为
平衡转化率为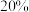 ,甲醇的选择性为
,甲醇的选择性为 。
。 的平衡转化率为
的平衡转化率为_______ ;该温度下反应Ⅰ的平衡常数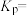
_______ (以分压表示,列出计算式)。
 捕集及利用是有效应对全球气候变化、促进低碳社会构建的重要方法。由
捕集及利用是有效应对全球气候变化、促进低碳社会构建的重要方法。由 转化制甲醇具有重要的经济效益。
转化制甲醇具有重要的经济效益。回答下列问题:
(1)反应
 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注, 为过渡态)。
为过渡态)。
该反应的

 。
。(2)在
 催化加氢制甲醇过程中除发生主反应Ⅰ:
催化加氢制甲醇过程中除发生主反应Ⅰ: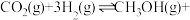
 外,还存在竞争反应Ⅱ:
外,还存在竞争反应Ⅱ: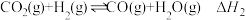 。已知甲醇选择性
。已知甲醇选择性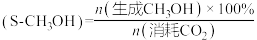 ,
, 的平衡转化率
的平衡转化率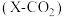 、甲醇的选择性
、甲醇的选择性 随温度、压强变化如图所示:
随温度、压强变化如图所示:
①由图可知压强大小关系:

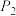 (填“>”“<”或“=”,下同),
(填“>”“<”或“=”,下同),
②
 时体系发生的反应主要是
时体系发生的反应主要是
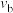 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③将
 和
和 的混合气体通入反应器,在温度t、压强P的条件下进行反应。达到平衡状态时,
的混合气体通入反应器,在温度t、压强P的条件下进行反应。达到平衡状态时, 平衡转化率为
平衡转化率为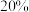 ,甲醇的选择性为
,甲醇的选择性为 。
。 的平衡转化率为
的平衡转化率为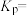
您最近一年使用:0次



