名校
解题方法
1 . 已知: 时,1mol相关物质的相对能量如图所示。
时,1mol相关物质的相对能量如图所示。

(1)写出C2H4完全燃烧生成气态水的热化学方程式___________ 。
(2)H2的燃烧热ΔH=___________ 。
(3)相同条件下,C2H4的稳定性比C2H6___________ (填“强”“弱”或“相同”),等物质的量的C2H4和C2H6完全燃烧放热较多的是___________ 。
(4) 是
是___________ 反应(填“吸热”或“放热”)。
(5)已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,相关的化学键键能如下。
已知: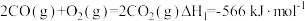 ;则a =
;则a =___________ 。
 时,1mol相关物质的相对能量如图所示。
时,1mol相关物质的相对能量如图所示。
(1)写出C2H4完全燃烧生成气态水的热化学方程式
(2)H2的燃烧热ΔH=
(3)相同条件下,C2H4的稳定性比C2H6
(4)
 是
是(5)已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,相关的化学键键能如下。
| 化学键 | C O(CO) O(CO) | O=O | C=O |
| 键能(KJ/mol) | a | 500 | 1075 |
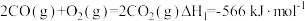 ;则a =
;则a =
您最近一年使用:0次
2023-10-18更新
|
177次组卷
|
2卷引用:山东学情2023-2024学年高二上学期10月质量检测(鲁科版)化学试题
2 . 研究化学反应中的能量变化有利于更好的开发和使用化学能源。
(1)已知 、CO、
、CO、 的燃烧热分别为285.8
的燃烧热分别为285.8 、283.0
、283.0 、890.3
、890.3 。
。
①相同条件下,等质量的 、CO、
、CO、 分别完全燃烧,放出热量最多的是
分别完全燃烧,放出热量最多的是_______ 。
②

_______  。
。
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a_______ 途径b(填“>”、“<”或“=”)
途径a: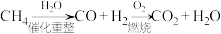
途径b: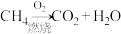
(2)已知白磷( )和
)和 的分子结构和部分化学键的键能分别如图、表所示:
的分子结构和部分化学键的键能分别如图、表所示:

①写出白磷与氧气反应生成 固体的热化学方程式:
固体的热化学方程式:_______ 。
②已知
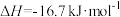 。比较稳定的是
。比较稳定的是_______ 。等质量的白磷、红磷分别完全燃烧,放出热量更多的是_______ 。
(1)已知
 、CO、
、CO、 的燃烧热分别为285.8
的燃烧热分别为285.8 、283.0
、283.0 、890.3
、890.3 。
。①相同条件下,等质量的
 、CO、
、CO、 分别完全燃烧,放出热量最多的是
分别完全燃烧,放出热量最多的是②


 。
。③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a
途径a:
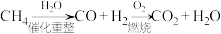
途径b:
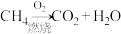
(2)已知白磷(
 )和
)和 的分子结构和部分化学键的键能分别如图、表所示:
的分子结构和部分化学键的键能分别如图、表所示:
| 化学键 | P-P | O=O | P-O |
键能( ) ) | a | b | c |
①写出白磷与氧气反应生成
 固体的热化学方程式:
固体的热化学方程式:②已知

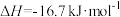 。比较稳定的是
。比较稳定的是
您最近一年使用:0次
3 . 甲烷是常见的燃料,可作为化工原料生产一系列化工有机产品,可用多种方法进行人工合成。回答下列问题:
(1) 加氢制备甲烷:
加氢制备甲烷: 。已知:
。已知: ,298K时,几种气态物质的标准摩尔生成焓如下表:
,298K时,几种气态物质的标准摩尔生成焓如下表:
则x=_______ 。
(2)一种微生物电化学方法生产甲烷的装置如图所示。

b为_______ (填“负极”或“正极”),阳极电极反应式为_______ 。理论上,每生成1L甲烷,阳极室产生
_______ L(标准状况)。
(3)2021年中科院设计并制备了一种介孔二氧化硅纳米球催化剂,可通过催化断裂生物质中的碳氧键和碳碳键,而将木质纤维素生物质直接转化为天然气,部分反应历程如图所示:

反应历程中最大能垒
_______ eV,写出该步的反应方程式_______ 。
(1)
 加氢制备甲烷:
加氢制备甲烷: 。已知:
。已知: ,298K时,几种气态物质的标准摩尔生成焓如下表:
,298K时,几种气态物质的标准摩尔生成焓如下表:| 物质 |  |  |  |  |
 | -393.5 | -241.8 | x | 0 |
(2)一种微生物电化学方法生产甲烷的装置如图所示。

b为

(3)2021年中科院设计并制备了一种介孔二氧化硅纳米球催化剂,可通过催化断裂生物质中的碳氧键和碳碳键,而将木质纤维素生物质直接转化为天然气,部分反应历程如图所示:

反应历程中最大能垒

您最近一年使用:0次
2022-10-11更新
|
315次组卷
|
3卷引用:山东德州市普通高中2022-2023学年高三上学期10月过程性检测化学试题
2022高二·上海·专题练习
4 . 在100 kPa时,C(石墨,s )= C(金刚石,s ) ΔH = 1.9 kJ·mol-1。
(1)石墨转化为金刚石是化学变化吗_______ ?
(2)1mol石墨与1mol金刚石相比,哪种物质的焓更高_______ ?
(3)你认为金刚石和石墨哪个物质更稳定_______ ?
(1)石墨转化为金刚石是化学变化吗
(2)1mol石墨与1mol金刚石相比,哪种物质的焓更高
(3)你认为金刚石和石墨哪个物质更稳定
您最近一年使用:0次
5 . 合理处理碳、氮氧化物,减少在大气中的排放,在生产、生活中有重要意义。回答下列问题:

(1)利用H2还原CO2是减少CO2排放的一种方法。H2在Cu-ZnO催化下可与CO2同时发生反应I、II,两反应的反应过程与能量的关系如图所示。
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
II.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
由图可知反应I是_________ 反应(填“吸热”或“放热”),ΔH1_________ ΔH2(填“>”、“<”或“=”)。
(2)H2还可以将CO2还原为CH4(g)和H2O(l)。已知25℃、101 kPa时H2和CH4的燃烧热分别为285.8 kJ·mol-1和890.3 kJ·mol-1,则25℃、101 kPa时H2与CO2反应生成CH4(g)和H2O(l)的热化学方程式为__________________ 。
(3)利用反应II生成的CO可将N2O转化为N2,反应的能量变化及反应历程如图所示,依次进行两步反应的化学方程式分别为①N2O+Fe+=N2+FeO+(慢),②FeO++CO=CO2+Fe+(快)。

反应过程中的中间产物是______________ ,每转化22.4 L(标准状况)N2O转移电子的数目为______________ ,反应①和反应②的活化能Ea①_________ Ea②(填“>”或“<”)。

(1)利用H2还原CO2是减少CO2排放的一种方法。H2在Cu-ZnO催化下可与CO2同时发生反应I、II,两反应的反应过程与能量的关系如图所示。
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1II.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2由图可知反应I是
(2)H2还可以将CO2还原为CH4(g)和H2O(l)。已知25℃、101 kPa时H2和CH4的燃烧热分别为285.8 kJ·mol-1和890.3 kJ·mol-1,则25℃、101 kPa时H2与CO2反应生成CH4(g)和H2O(l)的热化学方程式为
(3)利用反应II生成的CO可将N2O转化为N2,反应的能量变化及反应历程如图所示,依次进行两步反应的化学方程式分别为①N2O+Fe+=N2+FeO+(慢),②FeO++CO=CO2+Fe+(快)。

反应过程中的中间产物是
您最近一年使用:0次
名校
6 . (1)为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
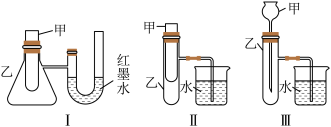
①上述装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是___________ (填序号)。
②某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是_________ 。
③除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是________ 反应(填“放热”或“吸热”)。
(2)化学反应的焓变通常用实验进行测定,也可进行理论推算。
①实验测得,标准状况下11.2L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出akJ的热量,试写出表示甲烷燃烧热的热化学方程式:_______ ;
②已知反应CH3—CH3(g)→CH2=CH2(g)+H2(g) ΔH,有关化学键的键能如下:
通过计算得出该反应的焓变ΔH=_________ ;
(3)研究NO2、SO2、CO等大气污染气体的处理有重要意义。
如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134kJ·mol-1,E2=368kJ·mol-1(E1、E2为反应的活化能)。
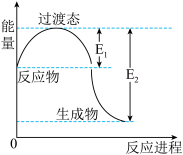
若在反应体系中加入催化剂,反应速率增大,则E1、ΔH的变化分别是________ 、________ (填“增大”、“减小”或“不变”);该反应放出的热量为__________ kJ。

①上述装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
②某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是
③除了图示某些装置,还有其它方法能证明超氧化钾粉末与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是
(2)化学反应的焓变通常用实验进行测定,也可进行理论推算。
①实验测得,标准状况下11.2L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出akJ的热量,试写出表示甲烷燃烧热的热化学方程式:
②已知反应CH3—CH3(g)→CH2=CH2(g)+H2(g) ΔH,有关化学键的键能如下:
| 化学键 | C—H | C=C | C—C | H—H |
| 键能/kJ·mol-1 | 414.4 | 615.3 | 347.3 | 435.3 |
通过计算得出该反应的焓变ΔH=
(3)研究NO2、SO2、CO等大气污染气体的处理有重要意义。
如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134kJ·mol-1,E2=368kJ·mol-1(E1、E2为反应的活化能)。

若在反应体系中加入催化剂,反应速率增大,则E1、ΔH的变化分别是
您最近一年使用:0次
2020-10-16更新
|
240次组卷
|
2卷引用:山东省滕州市第一中2020-2021学年高二上学期10月月考化学试题
名校
解题方法
7 . (1)用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和热。回答下列问题:
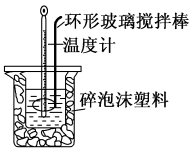
①烧杯间填满碎泡沫塑料的作用是____________ 。
②若大烧杯上改用薄铁板,求得的反应热将_____ (填“偏大”“偏小”或“无影响”)。
③若通过测定计算出产生的热量为1.42 kJ,请写出该反应的热化学方程式:_________________________________________ 。
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为___________________________________ 。
②一定条件下,在水溶液中所含离子Cl-、ClO-、ClO 、ClO
、ClO 、ClO
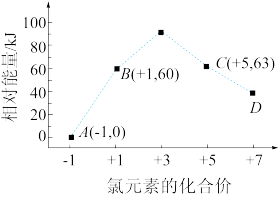
、ClO 各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO
各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO (aq)+2Cl-(aq)的ΔH=
(aq)+2Cl-(aq)的ΔH=____________ kJ·mol-1。

①烧杯间填满碎泡沫塑料的作用是
②若大烧杯上改用薄铁板,求得的反应热将
③若通过测定计算出产生的热量为1.42 kJ,请写出该反应的热化学方程式:
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
②一定条件下,在水溶液中所含离子Cl-、ClO-、ClO
 、ClO
、ClO 、ClO
、ClO 各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO
各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO (aq)+2Cl-(aq)的ΔH=
(aq)+2Cl-(aq)的ΔH=
您最近一年使用:0次
名校
8 . 一定温度下,在2L 的密闭容器中,A、B、C 三种气体物质的量随时间变化的曲线如图I, 能量变化如图 II 所示:

(1)从反应开始到到5s,用C 表示的反应速度为_____ , A 的转化率为_______ ,该化学反应的平衡常数为____________ 。
(2)分析图 II , 该反应的反应热ΔH =______ ,逆反应的活化能是___ 。
(3)将2. 00molA(g)、2. 00molB(g)的混合气体分别置于a、b、c 三个起始体积相同的密闭容器中,使反应在不同条件下进行,反应过程中 C 的浓度随时间的变化如图 III所示。

①反应从开始到达到平衡.反应速率由大到小的顺序为________ (用a、b、c 表示)。
② 与容器a中的反应相比,容器b中的反应改变的实验条件可能是______ ,容器c 中的反应改变的实验条件可能是___________ 。

(1)从反应开始到到5s,用C 表示的反应速度为
(2)分析图 II , 该反应的反应热ΔH =
(3)将2. 00molA(g)、2. 00molB(g)的混合气体分别置于a、b、c 三个起始体积相同的密闭容器中,使反应在不同条件下进行,反应过程中 C 的浓度随时间的变化如图 III所示。

①反应从开始到达到平衡.反应速率由大到小的顺序为
② 与容器a中的反应相比,容器b中的反应改变的实验条件可能是
您最近一年使用:0次
9 . 为研究反应 (aq)+2I−(aq)
(aq)+2I−(aq) 2
2 (aq)+I2(aq)的反应机理及反应进程中的能量变化,在
(aq)+I2(aq)的反应机理及反应进程中的能量变化,在 和I−的混合溶液中加入Fe3+,过程及图像如下:
和I−的混合溶液中加入Fe3+,过程及图像如下:
步骤①:2Fe3+(aq)+2I−(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
步骤②:2Fe2+(aq)+ (aq)
(aq) 2Fe3+(aq)+2
2Fe3+(aq)+2 (aq)
(aq)
下列有关该反应的说法正确的是______
A.步骤①和②都是吸热反应
B.Fe3+是该反应的中间产物
C.步骤①比②所需活化能大
D.该反应可设计成原电池
 (aq)+2I−(aq)
(aq)+2I−(aq) 2
2 (aq)+I2(aq)的反应机理及反应进程中的能量变化,在
(aq)+I2(aq)的反应机理及反应进程中的能量变化,在 和I−的混合溶液中加入Fe3+,过程及图像如下:
和I−的混合溶液中加入Fe3+,过程及图像如下:步骤①:2Fe3+(aq)+2I−(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)步骤②:2Fe2+(aq)+
 (aq)
(aq) 2Fe3+(aq)+2
2Fe3+(aq)+2 (aq)
(aq)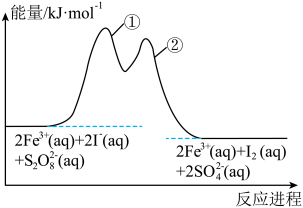
下列有关该反应的说法正确的是
A.步骤①和②都是吸热反应
B.Fe3+是该反应的中间产物
C.步骤①比②所需活化能大
D.该反应可设计成原电池
您最近一年使用:0次



