2021高三·全国·专题练习
名校
1 . 回答下列问题
(1)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用﹡标注。
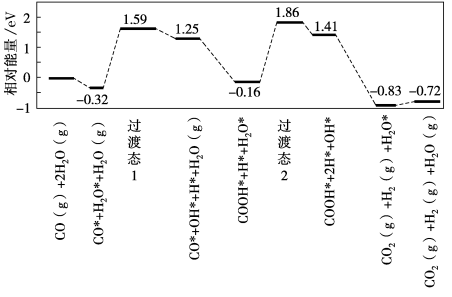
可知水煤气变换的ΔH___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=___________ eV。
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是___________ 。
(3)已知反应器中还存在如下反应:
ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用___________ 反应的ΔH。
(1)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用﹡标注。

可知水煤气变换的ΔH
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是
(3)已知反应器中还存在如下反应:
ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用
您最近一年使用:0次
2021-08-18更新
|
1464次组卷
|
6卷引用:黑龙江省鹤岗市第一中学2021-2022学年高二上学期开学考试化学试题
黑龙江省鹤岗市第一中学2021-2022学年高二上学期开学考试化学试题(已下线)第15讲 化学反应的热效应(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)新疆昌吉州2021-2022学年高二上学期期中质量检测化学试题(已下线)第15讲 化学反应的热效应 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第04讲 第一章《化学反应的热效应》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)广西钦州市第四中学2023-2024学年高二上学期9月考试化学试卷
名校
解题方法
2 . 据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s)ΔH=-989.2kJ·mol-1,有关键能数据如下表:
则x的值为______ 。
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等。硅光电池是一种把____ 能转化为______ 能的装置。
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s)ΔH=-989.2kJ·mol-1,有关键能数据如下表:
| 化学键 | Si-O | O=O | Si-Si |
| 键能/kJ·mol-1 | x | 498.8 | 176 |
则x的值为
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等。硅光电池是一种把
您最近一年使用:0次
2020-11-30更新
|
192次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学2021届高三上学期期末考试化学试题
名校
解题方法
3 . (1)某化学兴趣小组的同学进行了如下图所示的实验来探究复分解反应的热效应。在一个小烧杯中加入 晶体,将小烧杯放在事先已滴有
晶体,将小烧杯放在事先已滴有 滴水的玻璃片上。然后向小烧杯中加入
滴水的玻璃片上。然后向小烧杯中加入 晶体,并用玻璃棒迅速搅拌。稍后用手拿起烧杯时发现玻璃片与烧杯黏结在一起。
晶体,并用玻璃棒迅速搅拌。稍后用手拿起烧杯时发现玻璃片与烧杯黏结在一起。

①实验中玻璃棒的作用是________ ,所发生反应的化学方程式是________ 。
②若用手触摸烧杯外壁,将会有________ 的感觉,说明该反应为________ 反应,反应热
_________ (填“>”“<”或“=”)0。由该实验能否得出复分解反应就是吸热反应或放热反应的结论?________ (填“能”或“不能”),原因是________ 。
(2)如下图所示,某反应在不同条件下的反应历程分别为 、
、 。
。

①据图可判断出反应物的总键能________ (填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热
________ 0。
②其中 反应历程采用的条件为
反应历程采用的条件为________ (填序号)。
A.升高温度 B.增大反应物的浓度 C.增大压强 D.使用催化剂
 晶体,将小烧杯放在事先已滴有
晶体,将小烧杯放在事先已滴有 滴水的玻璃片上。然后向小烧杯中加入
滴水的玻璃片上。然后向小烧杯中加入 晶体,并用玻璃棒迅速搅拌。稍后用手拿起烧杯时发现玻璃片与烧杯黏结在一起。
晶体,并用玻璃棒迅速搅拌。稍后用手拿起烧杯时发现玻璃片与烧杯黏结在一起。
①实验中玻璃棒的作用是
②若用手触摸烧杯外壁,将会有

(2)如下图所示,某反应在不同条件下的反应历程分别为
 、
、 。
。
①据图可判断出反应物的总键能

②其中
 反应历程采用的条件为
反应历程采用的条件为A.升高温度 B.增大反应物的浓度 C.增大压强 D.使用催化剂
您最近一年使用:0次
2020-10-12更新
|
708次组卷
|
4卷引用:黑龙江省齐齐哈尔市第八中学2021-2022学年高二上学期期中考试化学试题
黑龙江省齐齐哈尔市第八中学2021-2022学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第一节 反应热 课时1 反应热 焓变(已下线)1.1.1 焓变 反应热-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第1章 化学反应的热效应(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)
解题方法
4 . 已知氮化硅陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得: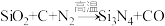 (未配平)。该反应过程中的能量变化如图所示:
(未配平)。该反应过程中的能量变化如图所示:
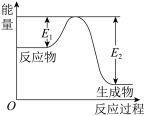
试回答下列问题。
(1)该反应中的氧化剂是________ ,还原产物是________ 。
(2)该反应是________ (填“吸热反应”或“放热反应”),
________ (填“>” “<”或“=”)0。
(3)该反应过程中,断裂旧化学键吸收的总能量________ (填“>”“<”或“=”)形成新化学键释放的总能量。
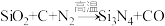 (未配平)。该反应过程中的能量变化如图所示:
(未配平)。该反应过程中的能量变化如图所示:
试回答下列问题。
(1)该反应中的氧化剂是
(2)该反应是

(3)该反应过程中,断裂旧化学键吸收的总能量
您最近一年使用:0次
2020-10-12更新
|
385次组卷
|
4卷引用:黑龙江省哈尔滨市阿城区龙涤中学校2019-2020学年高二上学期期中考试化学试题
名校
解题方法
5 . 如图是500 ℃时, 1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图。若在温度恒定,体积不变的容器中反应达到平衡,再充入NO2则,ΔH________ (填“增大”、“减小”或“不变”,下同)。请写出NO2和CO反应的热化学方程式:__________ 。该反应能自发进行的主要原因为_____________________ 。


您最近一年使用:0次
6 . Ⅰ.(1)在反应A(g)+3B(g)===2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物质B的化学反应速率为__________ mol·L-1·min-1。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的此化学反应速率为vB=_________ mol·L-1·s-1。
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________ ,若此后各物质的量均不再变化,则证明此可逆反应达到了______ 的程度。
A.反应彻底 B.反应终止 C.化学平衡 D.无法判断
Ⅱ. 已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1;②N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH =________ 。
Ⅲ. 下列热化学方程式书写正确的是(ΔH的绝对值均正确)________ 。
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热)
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的此化学反应速率为vB=
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有A.反应彻底 B.反应终止 C.化学平衡 D.无法判断
Ⅱ. 已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1;②N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH =
Ⅲ. 下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热)
您最近一年使用:0次



