1 . 某反应过程的能量变化如图所示。请填写下列空白。
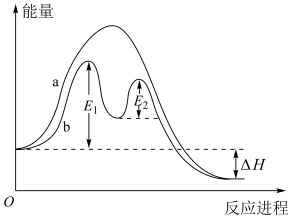
(1)反应过程___________ (填“a”或“b”)有催化剂参与。
(2)该反应为反应___________ (填“放热”或“吸热”),反应热为___________ 。

(1)反应过程
(2)该反应为反应
您最近半年使用:0次
2021-12-01更新
|
616次组卷
|
3卷引用:新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题
2 . 反应热或者焓变我们用___________ 符号来表示,它的单位是 kJ/mol。当△H为“-”或△H <0时,反应为___________ ,当△H为“+”或△H>0时,反应为___________ 。
您最近半年使用:0次
解题方法
3 . 完成下列问题
(1)1 mol C与1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),需要吸收131.5 kJ的热量,该反应的反应热为△H=___________ kJ/mol。
(2)已知反应A(g)+3B(g) 2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为
2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为___________
(3)若各物质的平衡浓度分别为c(A)=2.0 mol/L、c(B)=2.0 mol/L、c(C)=1.0 mol/L,则K=___________ 。
(1)1 mol C与1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),需要吸收131.5 kJ的热量,该反应的反应热为△H=
(2)已知反应A(g)+3B(g)
 2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为
2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为(3)若各物质的平衡浓度分别为c(A)=2.0 mol/L、c(B)=2.0 mol/L、c(C)=1.0 mol/L,则K=
您最近半年使用:0次
名校
4 . 回答下列问题
(1)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用﹡标注。
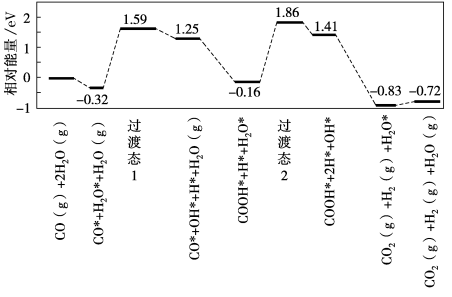
可知水煤气变换的ΔH___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=___________ eV。
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是___________ 。
(3)已知反应器中还存在如下反应:
ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用___________ 反应的ΔH。
(1)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用﹡标注。

可知水煤气变换的ΔH
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是
(3)已知反应器中还存在如下反应:
ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
……
ⅲ为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用
您最近半年使用:0次
2021-08-18更新
|
1457次组卷
|
6卷引用:新疆昌吉州2021-2022学年高二上学期期中质量检测化学试题
新疆昌吉州2021-2022学年高二上学期期中质量检测化学试题(已下线)第15讲 化学反应的热效应(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)黑龙江省鹤岗市第一中学2021-2022学年高二上学期开学考试化学试题(已下线)第15讲 化学反应的热效应 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第04讲 第一章《化学反应的热效应》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)广西钦州市第四中学2023-2024学年高二上学期9月考试化学试卷
名校
解题方法
5 . 碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下: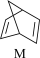

 ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是___________ 。
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+ O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a___________ 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:___________ 。
(4)根据下表中键能数据估算CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为___________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:


 ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+
 O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(4)根据下表中键能数据估算CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol-1) | a | b | c | d |
您最近半年使用:0次
2020-12-14更新
|
150次组卷
|
2卷引用:新疆北屯高级中学2020-2021学年高二上学期10月月考化学试题
名校
6 . 合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。
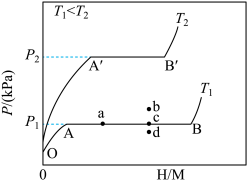
在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐渐增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)=ZMHy(s)△H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=___ (用含x和y的代数式表示)。温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=___ mL•g-1•min。反应的焓变△H1__ 0(填“>”“<”或“=”)。
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)____ η(T2)(填“>”“<”或“=”)。当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(Ⅰ)可能处于图中的___ 点(填“b”“c”或“d”),该贮氢合金可通过___ 或___ 的方式释放氢气。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。

在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐渐增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)=ZMHy(s)△H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)
您最近半年使用:0次
2020-04-16更新
|
302次组卷
|
4卷引用:新疆昌吉市第九中学2021届高三下学期开学考试化学试题
新疆昌吉市第九中学2021届高三下学期开学考试化学试题(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题天津市南开中学2020届高三教学质量监测理科综合化学部分
7 . 能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式:
①2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1;
②H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1;
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1;
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1;
⑤CO2(g)+2H2O(g)===2CH4(g)+2O2(g) ΔH=+890 kJ·mol-1
回答下列问题:
(1)上述反应中属于吸热反应的___________________________________________ 。
(2)H2的燃烧热为_______________________________________________________ 。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s)+H2O(g)===H2(g)+CO(g) ΔH=a kJ·mol-1;则a=________ ;
①2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1;
②H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1;
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1;
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1;
⑤CO2(g)+2H2O(g)===2CH4(g)+2O2(g) ΔH=+890 kJ·mol-1
回答下列问题:
(1)上述反应中属于吸热反应的
(2)H2的燃烧热为
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s)+H2O(g)===H2(g)+CO(g) ΔH=a kJ·mol-1;则a=
您最近半年使用:0次
名校
8 . 已知某反应A(g)+B(g)=C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题。
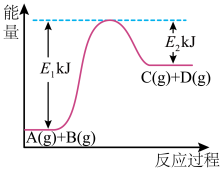
(1)该反应是_____ (填“吸热”或“放热”)反应,该反应的ΔH=________ kJ/mol (用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量______ (填“一定高”“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使反应速率增大,则E1和E2的变化是:E1_______ ,E2________ ΔH______ (填“增大”“减小”或“不变”)。

(1)该反应是
(2)若在反应体系中加入催化剂使反应速率增大,则E1和E2的变化是:E1
您最近半年使用:0次
2019-08-13更新
|
397次组卷
|
6卷引用:新疆维吾尔自治区且末县第二中学2018-2019学年高二上学期期末考试化学试题
新疆维吾尔自治区且末县第二中学2018-2019学年高二上学期期末考试化学试题(已下线)2014年高考化学苏教版总复习 6-1 化学反应中的热效应练习卷2016-2017学年宁夏吴忠中学高二下学期第一次月考化学试卷内蒙古北京八中乌兰察布分校2019-2020学年高二上学期第二次调研考试化学试题宁夏贺兰县景博中学2019-2020学年高二上学期第二次月考化学试题(已下线)1.1.1 化学反应的焓变(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)
9 . 反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(1)该反应是___________ 反应(填“吸热”、“放热”)。
(2) 在反应体系中加入催化剂,化学反应速率增大,E1、E2和ΔH的变化是:E1________ ,E2_______ ,ΔH _______ (填“增大”、“减小”或“不变”)
(3) 当反应达到平衡时,其他条件不变,升高温度,A的转化率______ (填“增大”、“减小”或“不变”)。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2) 在反应体系中加入催化剂,化学反应速率增大,E1、E2和ΔH的变化是:E1
(3) 当反应达到平衡时,其他条件不变,升高温度,A的转化率
您最近半年使用:0次



