1 . 下列热化学方程式中, 能正确表示物质的燃烧热的是
能正确表示物质的燃烧热的是
 能正确表示物质的燃烧热的是
能正确表示物质的燃烧热的是A.  kJ⋅mol kJ⋅mol |
B.  kJ·mol kJ·mol |
C.  kJ⋅mol kJ⋅mol |
D.  kJ·mol kJ·mol |
您最近半年使用:0次
名校
解题方法
2 . 我国含硫天然气资源丰富,甲烷与硫化氢重整制氢和天然气脱硫具有重要的现实意义。甲烷与硫化氢重整制氢反应为 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: 在
在_____ 下可自发进行。
A.高温 B.低温
在恒压条件下,起始时按 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数 的影响如图所示:
的影响如图所示: 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是_____ 。
(3)已知每1克 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_____ 。
 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: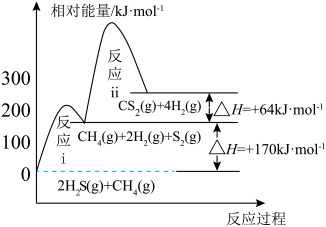
 在
在A.高温 B.低温
在恒压条件下,起始时按
 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数 的影响如图所示:
的影响如图所示: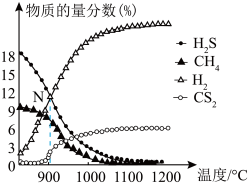
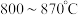 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是(3)已知每1克
 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为
您最近半年使用:0次
名校
解题方法
3 . 目前,处理烟气中 常采用两种方法:碱液吸收法和还原法。
常采用两种方法:碱液吸收法和还原法。
I.碱液吸收法
已知常温下:
第一步:用过量的浓氨水吸收 ,并在空气中氧化;
,并在空气中氧化;
第二步:加入石灰水,发生反应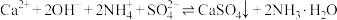 K。
K。
(1)25℃时,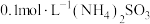 溶液的pH
溶液的pH___________ 7(填“>”“<”或“=”),并说明理由:___________ 。在该溶液中: ___________
___________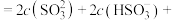 ___________。
___________。___________
(2)0.1mol/L下列溶液中,溶液中 由大到小的顺序是
由大到小的顺序是___________ 。
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
(3)第一步氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH___________ (填“升高”“不变”或“降低”)。
(4)计算第二步中反应的K=___________ 。
(5)测定一定浓度的 溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
(6)用过量的 溶液吸收
溶液吸收 的离子方程式:
的离子方程式:___________ 。
Ⅱ.水煤气还原法
已知:①
 ;
;
②
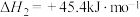 ;
;
③CO的燃烧热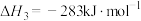 。
。
(7)表示液态硫的燃烧热的热化学方程式为___________ 。
(8)反应②中,正反应活化能
___________ (填“>”“<”或“=”) 。
。
(9)在一定压强下,发生反应①。平衡时 的转化率
的转化率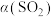 与投料比的比值
与投料比的比值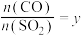 、温度T的关系如图所示。比较平衡时CO的转化率
、温度T的关系如图所示。比较平衡时CO的转化率 :N
:N___________ M(填“>”“<”或“=”,下同)。逆反应速率N___________ P。 、2molCO和
、2molCO和 发生反应①、②,第5min时达到平衡,测得混合气体中
发生反应①、②,第5min时达到平衡,测得混合气体中 、
、 的物质的量分别为1.6mol、1.8mol。
的物质的量分别为1.6mol、1.8mol。
①该温度下,反应②的平衡常数K为___________ 。(填数值)
②其他条件不变,在第7min时缩小容器体积,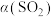
___________ (填“增大”“减小”或“不变”)。
 常采用两种方法:碱液吸收法和还原法。
常采用两种方法:碱液吸收法和还原法。I.碱液吸收法
已知常温下:
 |  |  |  |
 | 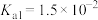  |  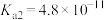 | 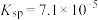 |
 ,并在空气中氧化;
,并在空气中氧化;第二步:加入石灰水,发生反应
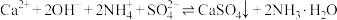 K。
K。(1)25℃时,
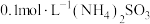 溶液的pH
溶液的pH ___________
___________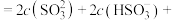 ___________。
___________。(2)0.1mol/L下列溶液中,溶液中
 由大到小的顺序是
由大到小的顺序是①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
(3)第一步氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH(4)计算第二步中反应的K=
(5)测定一定浓度的
 溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。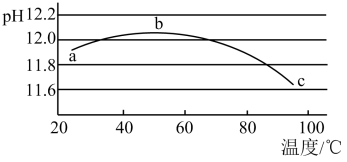
| A.c点水解程度最大 | B.水解是吸热过程 |
| C.a→b段水解平衡向右移动 | D.b点溶液中的 最大 最大 |
(6)用过量的
 溶液吸收
溶液吸收 的离子方程式:
的离子方程式:Ⅱ.水煤气还原法
已知:①

 ;
;②

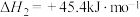 ;
;③CO的燃烧热
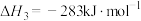 。
。(7)表示液态硫的燃烧热的热化学方程式为
(8)反应②中,正反应活化能

 。
。(9)在一定压强下,发生反应①。平衡时
 的转化率
的转化率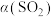 与投料比的比值
与投料比的比值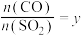 、温度T的关系如图所示。比较平衡时CO的转化率
、温度T的关系如图所示。比较平衡时CO的转化率 :N
:N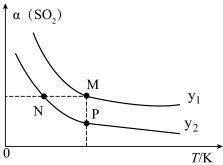
 、2molCO和
、2molCO和 发生反应①、②,第5min时达到平衡,测得混合气体中
发生反应①、②,第5min时达到平衡,测得混合气体中 、
、 的物质的量分别为1.6mol、1.8mol。
的物质的量分别为1.6mol、1.8mol。①该温度下,反应②的平衡常数K为
②其他条件不变,在第7min时缩小容器体积,
您最近半年使用:0次
解题方法
4 . 下列关于热化学反应的描述中正确的是
A. 和 和 反应的中和热 反应的中和热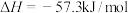 ,则 ,则 和 和 反应的中和热 反应的中和热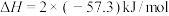 |
B.甲烷的标准燃烧热 ,则 ,则 |
C.已知: 、 、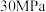 下, 下,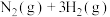 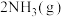 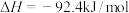 ;将 ;将 和过量的 和过量的 在此条件下充分反应,放出热量 在此条件下充分反应,放出热量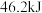 |
D. 的燃烧热是 的燃烧热是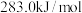 ,则 ,则 反应的 反应的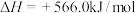 |
您最近半年使用:0次
解题方法
5 . 下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
B.由 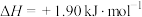 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
C.在101 kPa时,2 g  完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气摩尔燃烧焓的热化学方程式为 完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气摩尔燃烧焓的热化学方程式为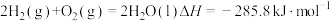 |
D.在稀溶液中, ,若将含0.5 mol ,若将含0.5 mol 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
您最近半年使用:0次
2024-03-26更新
|
148次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
名校
解题方法
6 . 硅是重要的半导体材料,构成现代电子工业的基础。磷及其化合物在工业中应用广泛,在国防和航天工业中亦有许多用途。在工业上,高纯硅可以通过下列流程制取:
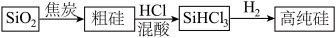
(1)基态硅原子核外电子的运动状态有___________ 种,占据的最高能层符号为___________ 。
(2)流程中由 制粗硅的反应不能说明碳的非金属性强于硅,原因是
制粗硅的反应不能说明碳的非金属性强于硅,原因是___________ 。请写出一个能说明碳的非金属性强于硅的化学方程式___________ 。
(3) 甲硅烷 是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,
是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下, 自燃放出热量
自燃放出热量 ,请写出其燃烧的热化学方程式:
,请写出其燃烧的热化学方程式:___________ 。
(4) 的热稳定性不如
的热稳定性不如 ,其原因是
,其原因是___________ 。
(5)工业上硅铁可以用于冶镁。以煅白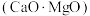 为原料与硅铁(含硅
为原料与硅铁(含硅 的硅铁合金)混合,置于密闭设备中于
的硅铁合金)混合,置于密闭设备中于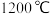 发生反应:
发生反应: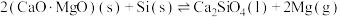 ,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:
,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:___________ 。
(6)有关碳和硅的有关化学键链能如下所示。
硅也有系列氢化物,如甲硅烷等。但硅烷在种类和数量上都远不如烷烃多,原因是___________ 。

(1)基态硅原子核外电子的运动状态有
(2)流程中由
 制粗硅的反应不能说明碳的非金属性强于硅,原因是
制粗硅的反应不能说明碳的非金属性强于硅,原因是(3) 甲硅烷
 是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,
是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下, 自燃放出热量
自燃放出热量 ,请写出其燃烧的热化学方程式:
,请写出其燃烧的热化学方程式:(4)
 的热稳定性不如
的热稳定性不如 ,其原因是
,其原因是(5)工业上硅铁可以用于冶镁。以煅白
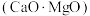 为原料与硅铁(含硅
为原料与硅铁(含硅 的硅铁合金)混合,置于密闭设备中于
的硅铁合金)混合,置于密闭设备中于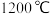 发生反应:
发生反应: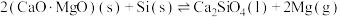 ,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:
,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:(6)有关碳和硅的有关化学键链能如下所示。
| 化学键 |  |  |  |  |  |  |
键能/ | 356 | 413 | 336 | 226 | 318 | 452 |
您最近半年使用:0次
7 . 请根据学过的知识回答下列问题:
(1)
 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程___________ 。
(2)已知: 键的键能是
键的键能是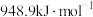 ,
, 键的键能是
键的键能是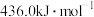 ,
, 键的键能是
键的键能是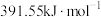 ,则
,则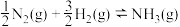

___________ 。
(3)已知:①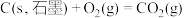

②

③

则298K时反应 的焓变:
的焓变:
___________ 。
(4)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  。
。
①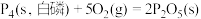

②

(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为___________ 。
(6)如图所示,某反应在不同条件下的反应历程分别为a、b。
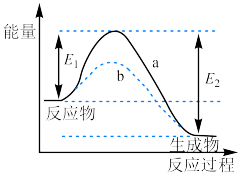
据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,反应历程a、b的反应热___________ (填“相同”或“不相同”)。
(1)

 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程(2)已知:
 键的键能是
键的键能是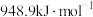 ,
, 键的键能是
键的键能是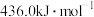 ,
, 键的键能是
键的键能是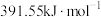 ,则
,则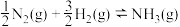

(3)已知:①
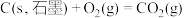

②


③


则298K时反应
 的焓变:
的焓变:
(4)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 。
。①
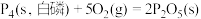

②


(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和

 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(6)如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近半年使用:0次
8 . 下列关于燃烧热和中和热的描述中正确的是
A. 溶液和溶液 溶液和溶液 反应的中和热ΔH=−57.3kJ/mol,则H2SO4溶液和Ba(OH)2溶液反应的反应热ΔH=2×(−57.3)kJ/mol 反应的中和热ΔH=−57.3kJ/mol,则H2SO4溶液和Ba(OH)2溶液反应的反应热ΔH=2×(−57.3)kJ/mol |
| B.已知2H2(g)+O2(g)=2H2O(g)ΔH=−483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
C.由C(s)+  O2(g)=CO(g)的反应热为110.5kJ/mol,可知碳的燃烧热为110.5kJ/mol O2(g)=CO(g)的反应热为110.5kJ/mol,可知碳的燃烧热为110.5kJ/mol |
| D.1molNaOH分别和1molCH3COOH、1molHNO3反应放出的热量:CH3COOH<HNO3 |
您最近半年使用:0次
名校
9 . 下列关于反应热的说法正确的是
| A.使用催化剂只改变可逆反应中正反应的活化能 |
| B.反应物的总键能小于生成物的总键能,则反应为吸热反应 |
C.已知红磷比白磷更稳定,  |
D.  ,则 ,则 燃烧热为 燃烧热为 |
您最近半年使用:0次
10 . 为了更好的解决能源问题,人们在研究如何提高燃料燃烧效率的同时,也在寻找新能源。下列说法不正确的是
| A.太阳能、地热能、核聚变能均属于新能源 |
| B.为了使燃料充分燃烧,通入的空气越多越好 |
| C.通过洁净煤技术及烟气脱硫,减轻燃煤污染,并提高煤燃烧的热利用率 |
| D.为开发氢能,可设法将太阳能聚焦,产生高温使水分解产生氢气 |
您最近半年使用:0次



