名校
1 . 工业上乙烯催化氧化制乙醛的某一反应原理为2CH2=CH2(g)+O2(g) 2CH3CHO(aq) ΔH,该反应原理可以拆解为如下三步反应:
2CH3CHO(aq) ΔH,该反应原理可以拆解为如下三步反应:
Ⅰ.CH2=CH2(g)+PdCl2(aq)+H2O(l)=CH3CHO(aq)+Pd(s)+2HCl(aq) ΔH1
Ⅱ.……
Ⅲ.4CuCl(s)+O2(g)+4HCl(aq)=4CuCl2(aq)+2H2O(l) ΔH3
若第Ⅱ步反应的反应热为ΔH2,且ΔH=2ΔH1+2ΔH2+ΔH3,则第Ⅱ步反应的热化学方程式为
 2CH3CHO(aq) ΔH,该反应原理可以拆解为如下三步反应:
2CH3CHO(aq) ΔH,该反应原理可以拆解为如下三步反应:Ⅰ.CH2=CH2(g)+PdCl2(aq)+H2O(l)=CH3CHO(aq)+Pd(s)+2HCl(aq) ΔH1
Ⅱ.……
Ⅲ.4CuCl(s)+O2(g)+4HCl(aq)=4CuCl2(aq)+2H2O(l) ΔH3
若第Ⅱ步反应的反应热为ΔH2,且ΔH=2ΔH1+2ΔH2+ΔH3,则第Ⅱ步反应的热化学方程式为
| A.PdCl2(aq)+2CuCl(s)=Pd(s)+2CuCl2(aq) ΔH2 |
| B.2Pd(s)+4CuCl2(aq)=2PdCl2(aq)+4CuCl(s) ΔH2 |
| C.Pd(s)+2CuCl2(aq)=PdCl2(aq)+2CuCl(s) ΔH2 |
| D.2PdCl2(aq)+4CuCl(s)=2Pd(s)+4CuCl2(aq) ΔH2 |
您最近一年使用:0次
2021-07-27更新
|
403次组卷
|
8卷引用:江苏省宿迁市泗阳县实验高级中学2023-2024学年高二下学期3月月考化学试题
江苏省宿迁市泗阳县实验高级中学2023-2024学年高二下学期3月月考化学试题(已下线)专题1.2 反应热的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)1.2 反应热的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)第二节 反应热的计算 第1课时 盖斯定律江苏省扬州市江都区邵伯高级中学2022-2023学年高二10月阶段性测试化学(选修)试题重庆缙云教育联盟2023-2024学年高二上学期9月月考化学试题江苏省常州市前黄高级中学2022-2023学年高二上学期第二次阶段考试化学试题江苏省盐城市大丰区新丰中学2023-2024学年高二上学期第二次学情调研化学试题(选修)
名校
解题方法
2 . 氢能是最具前景的清洁能源之一,目前水分解制氢技术及贮氢材料的开发应用都取得了很大进展。已知:2H2(g)+ O2(g)=2H2O(1)∆H=-571.6kJ·mol-1。下列说法错误的是
| A.1mol H2O(l)分解制得1molH2需要吸收571.6kJ的能量 |
| B.氢气作为新能源具有热值高、无污染、资源丰富、可再生等优点 |
| C.贮氢材料具有能大量、快速和高效率地吸收和释放氢气的特点 |
| D.利用太阳能光催化分解水制氢是一种理想的制氢手段 |
您最近一年使用:0次
2021-03-09更新
|
272次组卷
|
3卷引用:江苏省沭阳县修远中学2020-2021学年高一下学期第一次月考化学试题
江苏省沭阳县修远中学2020-2021学年高一下学期第一次月考化学试题(已下线)6.2.2 燃料燃烧释放的能量 氢燃料的应用前景(练习)-2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)江苏省淮安市涟水县第一中学2021-2022学年高一下学期第一次阶段检测化学试题
3 . 四氯化钛是乙烯聚合催化剂的重要成分,制备反应如下:
①TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)ΔH1=+175.4kJ·mol-1
②C(s)+ O2(g)=CO(g)ΔH2=-110.45kJ·mol-1
O2(g)=CO(g)ΔH2=-110.45kJ·mol-1
下列说法正确的是
①TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)ΔH1=+175.4kJ·mol-1
②C(s)+
 O2(g)=CO(g)ΔH2=-110.45kJ·mol-1
O2(g)=CO(g)ΔH2=-110.45kJ·mol-1下列说法正确的是
| A.C的燃烧热是-110.45kJ·mol-1 |
| B.若反应①中使用催化剂加快反应速率,单位时间内吸收更多热量,则ΔH1变大 |
C.反应①中的能量变化如图所示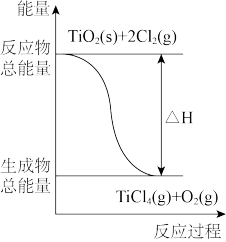 |
| D.反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g)ΔH=-45.5kJ·mol-1 |
您最近一年使用:0次
2020-07-01更新
|
391次组卷
|
6卷引用:江苏省沭阳县修远中学、泗洪县淮北中学、洪翔中学2019-2020学年高二下学期联考化学试题
名校
解题方法
4 . 肼(N2H4)是火箭发动机的燃料,它与N2O4反应生成氮气和水蒸气。已知:
①N2(g)+2O2(g)===N2O4(g)ΔH=+8.7 kJ·mol-1
②N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH=-534.0 kJ·mol-1
下列表示肼跟N2O4反应的热化学方程式正确的是
①N2(g)+2O2(g)===N2O4(g)ΔH=+8.7 kJ·mol-1
②N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH=-534.0 kJ·mol-1
下列表示肼跟N2O4反应的热化学方程式正确的是
| A.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-542.7 kJ·mol-1 |
| B.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 076.7 kJ·mol-1 |
C.N2H4(g)+ N2O4(g)=== N2O4(g)=== N2(g)+2H2O(g) ΔH=-1 076.7 kJ·mol-1 N2(g)+2H2O(g) ΔH=-1 076.7 kJ·mol-1 |
| D.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 059.3 kJ·mol-1 |
您最近一年使用:0次
2020-06-15更新
|
517次组卷
|
25卷引用:江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题
江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题(已下线)2010届河北沙河一中考前热身理综化学卷(一)(已下线)2011届黑龙江省鸡西市第一中学高三上学期期末考试(理综)化学部分(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷2015-2016学年江西省临川一中高二上第一次月考化学试卷2015-2016学年吉林大学附属中学高二上期末化学试卷吉林省乾安县第七中学2018-2019学年高一下学期第二次质量检测化学试题吉林省吉林市第五十五中学2018-2019学年高一下学期期末考试化学试题贵州省思南中学2019-2020学年高二9月月考化学试题山东省济南外国语学校三箭分校2020届高三上学期期中检测化学试题广东省湛江市第二十一中学2019-2020学年高二上学期期中考试化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第三次月考化学试题吉林省吉林市吉化第一高级中学校2019-2020学年高一下学期期末考试化学试题江西省贵溪市实验中学2020-2021学年高二上学期第一次月考化学试题陕西省汉中市洋县中学2018-2019学年高二上学期第一次月考化学试题陕西省西安市第一中学2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第1节 化学反应的热效应 课时4 反应焓变的计算江西省抚州市金溪县第一中学2019-2020学年高二上学期第二次月考化学试题广西玉林市普通中学2020-2021学年高二下学期月考化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期第一次月考化学试题江西省南城第二中学2021-2022学年高二上学期第一次月考化学试题天津市第三中学2021-2022学年高二上学期10月阶段性检测化学试题甘肃省玉门市2021-2022学年高二上学期 “研课标读教材”期中学业质量监测化学试题甘肃省玉门市2021-2022学年高二下学期 “研课标读教材”期中学业质量监测试化学试题(一)宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
5 . 氧化铁是一种重要的无机材料,化学性质稳定,催化活性高,具有良好的耐光性、耐热性和对紫外线的屏蔽性,从某种工业酸性废液(主要含Na+、Fe2+、Fe3+、Mg2+、Al3+、Cl-、 )中回收氧化铁流程如图所示:
)中回收氧化铁流程如图所示:
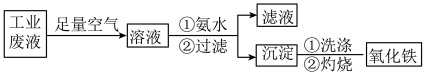
已知:常温下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33
(1)写出在该酸性废液中通入空气时发生反应的离子方程式:_________ ,指出使用空气比使用氯气好的原因是__________ 。
(2)已知Fe3+(aq)+3OH-(aq)=Fe(OH)3(s) ΔH=-Q1 kJ·mol-1,题(1)中每生成1 mol含铁微粒时,放热Q2,请你计算1 mol Fe2+全部转化为Fe(OH)3(s)的热效应ΔH=________ 。
(3)常温下,根据已知条件计算在pH=5的溶液中,理论上Fe3+在该溶液中可存在的最大浓度c(Fe3+)=____________ 。
(4)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时可能混有的杂质是________ (填化学式,下同),用________ 试剂可将其除去。
 )中回收氧化铁流程如图所示:
)中回收氧化铁流程如图所示:
已知:常温下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33
(1)写出在该酸性废液中通入空气时发生反应的离子方程式:
(2)已知Fe3+(aq)+3OH-(aq)=Fe(OH)3(s) ΔH=-Q1 kJ·mol-1,题(1)中每生成1 mol含铁微粒时,放热Q2,请你计算1 mol Fe2+全部转化为Fe(OH)3(s)的热效应ΔH=
(3)常温下,根据已知条件计算在pH=5的溶液中,理论上Fe3+在该溶液中可存在的最大浓度c(Fe3+)=
(4)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时可能混有的杂质是
您最近一年使用:0次
2020-02-21更新
|
352次组卷
|
5卷引用:江苏省沭阳县修远中学、泗洪县淮北中学、洪翔中学2019-2020学年高二下学期联考化学试题



