1 . 脱硝通常指将烟气中的氮氧化物(NOx)转化为无害的物质。
(1)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
①已知:4MH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905.5kJ·mol-1
4NO(g)+6H2O(g) △H=-905.5kJ·mol-1
N2(g)+O2(g) 2NO(g) △H=+l80kJ •mol-1
2NO(g) △H=+l80kJ •mol-1
完成该方法中主要反应的热化学方程式:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=
4N2(g)+6H2O(g) △H=__________ 。
②该方法应控制反应温度在315〜400℃之间,反应温度不宜过低也不宜过高的原因是_________________ 。
③氨氮比[ ]会直接影响该方法的脱硝率,350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如下图所示,则X是
]会直接影响该方法的脱硝率,350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如下图所示,则X是_______ (填学式)。氨氮比由0.5增加到1.0时,脱硝主要反应的平衡将向_______ 方向移动。当 >1.0时,烟气中NO浓度反而增大,主要原因是
>1.0时,烟气中NO浓度反而增大,主要原因是______ 。
(2)直接电解吸收也是脱硝的一种方法,用6%的稀硝酸吸收NOx生成HNO2(—元弱酸),再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如上右图所示。
①图中b应连接电源的______ (填“正极”或“负极”)。
②将石墨电极设置成颗粒状的目的是___________________ 。
③阳极的电极反应式为_________________ 。
(1)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
①已知:4MH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H=-905.5kJ·mol-1
4NO(g)+6H2O(g) △H=-905.5kJ·mol-1 N2(g)+O2(g)
 2NO(g) △H=+l80kJ •mol-1
2NO(g) △H=+l80kJ •mol-1完成该方法中主要反应的热化学方程式:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=
4N2(g)+6H2O(g) △H=②该方法应控制反应温度在315〜400℃之间,反应温度不宜过低也不宜过高的原因是
③氨氮比[
 ]会直接影响该方法的脱硝率,350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如下图所示,则X是
]会直接影响该方法的脱硝率,350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如下图所示,则X是 >1.0时,烟气中NO浓度反而增大,主要原因是
>1.0时,烟气中NO浓度反而增大,主要原因是
(2)直接电解吸收也是脱硝的一种方法,用6%的稀硝酸吸收NOx生成HNO2(—元弱酸),再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如上右图所示。
①图中b应连接电源的
②将石墨电极设置成颗粒状的目的是
③阳极的电极反应式为
您最近一年使用:0次
2017-04-02更新
|
262次组卷
|
2卷引用:福建省厦门市厦门英才学校2021-2022学年高二上学期期中考试化学试题
2 . (1)甲醇蒸气转化为氢气的一种原理是CH3OH和H2O反应生成CO2和H2。
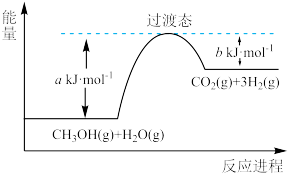
下图是该过程中能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能a的变化是_______ (填“增大”、“减小”或“不变”),反应热ΔH的变化是_______ (填“增大”、“减小”或“不变”)。请写出反应进程CH3OH(g)和H2O(g)反应的热化学方程式_______ 。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用标准状况下4.48 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为_______ ,放出的热量为_______ kJ(用含有a和b的代数式表示)。

下图是该过程中能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能a的变化是
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用标准状况下4.48 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为
您最近一年使用:0次
2016-12-09更新
|
285次组卷
|
2卷引用:福建省泉州市第六中学2022-2023学年高二上学期期中考化学试题
3 . 天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式是:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═﹣889.6kJ/mol
请回答下列问题:
(1)反应物能量总和_______ (填“大于”、“小于”或“等于”)生成物能量总和.
(2)若1mol甲烷完全燃烧生成二氧化碳和水蒸气,则放出的热量_______ (填“>”、“<”或“=”)889.6kJ.
(3)已知氢气燃烧生成液态水的热化学方程式是:2H2(g)+O2(g)═2H2O(l)△H=﹣572kJ/mol,则相同质量的甲烷和氢气,完全燃烧生成液态水,放热较多的是________ .
(4)如图所示的装置是由CH4、O2和KOH溶液组成的新型燃料电池.
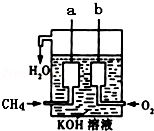
①该电池的负极是________ (填“a”或“b”)电极,该极的电极反应式是_______________ .
②电池工作一段时间后电解质溶液的pH____________ (填“增大”、“减小”或“不变”).
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═﹣889.6kJ/mol
请回答下列问题:
(1)反应物能量总和
(2)若1mol甲烷完全燃烧生成二氧化碳和水蒸气,则放出的热量
(3)已知氢气燃烧生成液态水的热化学方程式是:2H2(g)+O2(g)═2H2O(l)△H=﹣572kJ/mol,则相同质量的甲烷和氢气,完全燃烧生成液态水,放热较多的是
(4)如图所示的装置是由CH4、O2和KOH溶液组成的新型燃料电池.

①该电池的负极是
②电池工作一段时间后电解质溶液的pH
您最近一年使用:0次
12-13高二上·福建泉州·期末
4 . (1)已知:2SO2(g)+ O2 (g)  2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-1
2NO(g)+ O2 (g) 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1
则反应NO2(g)+ SO2 (g) SO3 (g) +NO(g)的△H =
SO3 (g) +NO(g)的△H =_______ kJ·mol-1
一定条件下,将NO2与SO2按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_______ 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d。每消耗1molSO3的同时生成1molNO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+ 2H2 (g) CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H _______ 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_______ 。
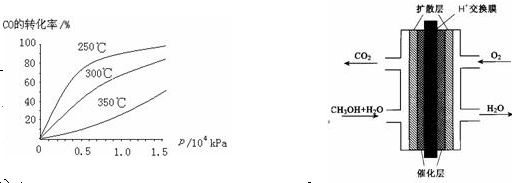
(3)甲醇(CH3OH)燃料电池的结构示意图如右上。甲醇进入_______ 极(填“正”或“负”),正极发生的电极反应为_______ 。
(4)101 kPa时,若16 gCH3OH完全燃烧生成液态水,放出热量为363.25 kJ/mol,则甲醇燃烧的热化学方程式为_______ 。
 2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-12NO(g)+ O2 (g)
 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1则反应NO2(g)+ SO2 (g)
 SO3 (g) +NO(g)的△H =
SO3 (g) +NO(g)的△H =一定条件下,将NO2与SO2按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d。每消耗1molSO3的同时生成1molNO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+ 2H2 (g)
 CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H 
(3)甲醇(CH3OH)燃料电池的结构示意图如右上。甲醇进入
(4)101 kPa时,若16 gCH3OH完全燃烧生成液态水,放出热量为363.25 kJ/mol,则甲醇燃烧的热化学方程式为
您最近一年使用:0次



