名校
解题方法
1 . 将TiO2转化为TiCl4是工业冶炼金属钛的主要反应之一。
已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140.5 kJ∙mol−1
C(s,石墨)+ O2(g)=CO(g) ΔH=−110.5 kJ∙mol−1
O2(g)=CO(g) ΔH=−110.5 kJ∙mol−1
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(l)+2CO(g)的ΔH是
已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140.5 kJ∙mol−1
C(s,石墨)+
 O2(g)=CO(g) ΔH=−110.5 kJ∙mol−1
O2(g)=CO(g) ΔH=−110.5 kJ∙mol−1则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(l)+2CO(g)的ΔH是
| A.+80.5 kJ∙mol−1 | B.+30.0 kJ∙mol−1 | C.−30.0 kJ∙mol−1 | D.−80.5 kJ∙mol−1 |
您最近一年使用:0次
2023-02-23更新
|
647次组卷
|
19卷引用:广东省惠州市2020-2021学年高二上学期期末考试化学试题
广东省惠州市2020-2021学年高二上学期期末考试化学试题广东省惠州市2020-2021学年高二上学期期末质量监测化学试题广东省梅州市大埔县田家炳实验中学2021-2022学年高二上学期第一次段考(月考)化学试题天津市第三中学2021-2022学年高二上学期10月阶段性检测化学试题山东省济宁市微山县第二中学2021-2022学年高二上学期第一学段考试化学试题海南省临高县新盈中学2021-2022学年高二上学期(1-4班)期中考试化学试题江苏省南通市海门市包场高级中学2020-2021学年高二上学期学情检测化学试题(选修)福建省南安市侨光中学2020-2021学年高二上学期第二次阶段考化学试题辽宁省重点高中沈阳市联合体2021-2022高一下学期期中考试化学试题福建省连城县第一中学2022-2023学年高二上学期月考(一)化学试题福建省三明第一中学2022-2023学年高二上学期第一次月考化学试题新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题湖北省黄冈市麻城第二中学2021-2022学年高一下学期4月月考化学试题广东省阳江市高新区2022-2023学年高二上学期1月期末考试化学试题广东省深圳市罗湖高级中学2022-2023学年高一下学期4月期中考试化学试题内蒙古通辽市重点学校2022-2023学年高一下学期3月质量检测化学试题(已下线)专题02 盖斯定律、反应热的计算【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)黑龙江省 牡丹江市第二高级中学2023-2024学年高三上学期12月月考化学试题新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第一次月考化学试题
名校
2 . 氢气选择性催化还原(H2-SCR)是目前消除NO的理想方法,备受研究者关注。
H2-SCR法的主反应:2NO(g)+2H2(g) N2(g)+2H2O(g) ΔH1
N2(g)+2H2O(g) ΔH1
副反应:2NO(g)+H2(g) N2O(g)+H2O(g) ΔH2<0
N2O(g)+H2O(g) ΔH2<0
回答下列问题:
(1)已知:H2(g)+ O2(g)
O2(g)  H2O(g) ΔH=-241.5 kJ/mol
H2O(g) ΔH=-241.5 kJ/mol
N2(g)+O2(g) 2NO(g) ΔH=+180.5 kJ/mol
2NO(g) ΔH=+180.5 kJ/mol
①ΔH1=___________ kJ/mol
②提高主反应选择性的最佳措施是___________ 。
A.降低温度 B.增大压强 C.增大c(H2) D.使用合适的催化剂
(2)H2-SCR在Pt-HY催化剂表面的反应机理如下图

已知在HY载体表面发生反应的NO、O2物质的量之比为4:1,补充并配平下列化学方程式:NH +NO+O2=N2+H2O+
+NO+O2=N2+H2O+___________ ,反应中每生成1mol N2,转移的电子的物质的量为___________
(3)T℃, 时,恒容容器中发生上述反应,平衡体系中N2物质的量分数为10%,平衡压强与起始压强之比为3.6:4,则NO的有效去除率(转化为N2)为
时,恒容容器中发生上述反应,平衡体系中N2物质的量分数为10%,平衡压强与起始压强之比为3.6:4,则NO的有效去除率(转化为N2)为___________ 。
(4)一定条件下,恒温恒容容器中充入c(NO)=2.0mol·L-1、c(H2)=4.0mol·L-1,只发生反应2NO(g)+2H2(g) N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:
N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:
①下列说法正确的是___________
a.若容器内气体的密度恒定,反应达到平衡状态
B.若容器内各气体浓度恒定,反应达到平衡状态
C.若容器内压强恒定,反应达到平衡状态
D.若容器内N2和H2O的物质的量之比为1:2,反应达到平衡状态
②假设容器的体积为1L,则该条件下反应的平衡常数K=___________ 。(列出计算表达式,不要求计算结果)
H2-SCR法的主反应:2NO(g)+2H2(g)
 N2(g)+2H2O(g) ΔH1
N2(g)+2H2O(g) ΔH1副反应:2NO(g)+H2(g)
 N2O(g)+H2O(g) ΔH2<0
N2O(g)+H2O(g) ΔH2<0回答下列问题:
(1)已知:H2(g)+
 O2(g)
O2(g)  H2O(g) ΔH=-241.5 kJ/mol
H2O(g) ΔH=-241.5 kJ/molN2(g)+O2(g)
 2NO(g) ΔH=+180.5 kJ/mol
2NO(g) ΔH=+180.5 kJ/mol①ΔH1=
②提高主反应选择性的最佳措施是
A.降低温度 B.增大压强 C.增大c(H2) D.使用合适的催化剂
(2)H2-SCR在Pt-HY催化剂表面的反应机理如下图

已知在HY载体表面发生反应的NO、O2物质的量之比为4:1,补充并配平下列化学方程式:NH
 +NO+O2=N2+H2O+
+NO+O2=N2+H2O+(3)T℃,
 时,恒容容器中发生上述反应,平衡体系中N2物质的量分数为10%,平衡压强与起始压强之比为3.6:4,则NO的有效去除率(转化为N2)为
时,恒容容器中发生上述反应,平衡体系中N2物质的量分数为10%,平衡压强与起始压强之比为3.6:4,则NO的有效去除率(转化为N2)为(4)一定条件下,恒温恒容容器中充入c(NO)=2.0mol·L-1、c(H2)=4.0mol·L-1,只发生反应2NO(g)+2H2(g)
 N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:
N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:| t/min | 0 | 10 | 20 | 30 | 40 |
| p/mPa | 24 | 22.6 | 21.6 | 21 | 21 |
①下列说法正确的是
a.若容器内气体的密度恒定,反应达到平衡状态
B.若容器内各气体浓度恒定,反应达到平衡状态
C.若容器内压强恒定,反应达到平衡状态
D.若容器内N2和H2O的物质的量之比为1:2,反应达到平衡状态
②假设容器的体积为1L,则该条件下反应的平衡常数K=
您最近一年使用:0次
2021-11-03更新
|
424次组卷
|
3卷引用:广东省惠州市惠阳高级中学实验学校2021-2022学年高三上学期月考化学试题
广东省惠州市惠阳高级中学实验学校2021-2022学年高三上学期月考化学试题广东省汕头市金山中学2021-2022学年高三上学期期中考试试题(已下线)第15周 周测卷-备战2022年高考化学周测与晚练(新高考专用)
3 . 2020年世界环境日的宣传主题为“关爱自然,刻不容缓”。防治大气污染、水体污染等是世界各国保护环境的最重要课题。
I.利用高效催化剂可以处理汽车尾气中的NO和CO,发生反应
(1)已知几种化学键的键能数据如下:
则上述反应的
_______  。
。
(2)在 恒容密闭容器中充入
恒容密闭容器中充入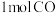 和
和 ,测得
,测得 的转化率与温度、时间的关系如图所示:
的转化率与温度、时间的关系如图所示:

① 温度下,
温度下,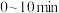 内用
内用 表示的平均反应速率
表示的平均反应速率
_______  ;
; 温度下,上述反应的平衡常数
温度下,上述反应的平衡常数
_______  。
。
② 温度下,向平衡后的容器内再加入
温度下,向平衡后的容器内再加入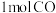 和
和 ,则再次达平衡时NO的转化率
,则再次达平衡时NO的转化率_______ (填“增大”“减小”或“不变”)。
II. 催化还原NO是重要的烟气脱硝技术,研究发现在以
催化还原NO是重要的烟气脱硝技术,研究发现在以 为主的催化剂上可能发生的反应过程如图。
为主的催化剂上可能发生的反应过程如图。

(3)写出脱硝过程的总反应的化学方程式_______ 。
(4)催化氧化法去除NO是在一定条件下,用 消除NO污染,其反应原理为:
消除NO污染,其反应原理为:
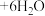 。不同温度条件下,
。不同温度条件下, 为
为 时,得到NO脱除率曲线如图所示。脱除NO的最佳温度是
时,得到NO脱除率曲线如图所示。脱除NO的最佳温度是_______ 。在温度超过100℃时NO脱除率骤然下降的原因可能是_______ 。

I.利用高效催化剂可以处理汽车尾气中的NO和CO,发生反应

(1)已知几种化学键的键能数据如下:
| 化学键 | C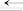 O O | NO中的共价键 | N≡N | C=O |
键能( ) ) | 1076 | 630 | 946 | 799 |

 。
。(2)在
 恒容密闭容器中充入
恒容密闭容器中充入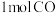 和
和 ,测得
,测得 的转化率与温度、时间的关系如图所示:
的转化率与温度、时间的关系如图所示:
①
 温度下,
温度下,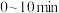 内用
内用 表示的平均反应速率
表示的平均反应速率
 ;
; 温度下,上述反应的平衡常数
温度下,上述反应的平衡常数
 。
。②
 温度下,向平衡后的容器内再加入
温度下,向平衡后的容器内再加入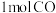 和
和 ,则再次达平衡时NO的转化率
,则再次达平衡时NO的转化率II.
 催化还原NO是重要的烟气脱硝技术,研究发现在以
催化还原NO是重要的烟气脱硝技术,研究发现在以 为主的催化剂上可能发生的反应过程如图。
为主的催化剂上可能发生的反应过程如图。
(3)写出脱硝过程的总反应的化学方程式
(4)催化氧化法去除NO是在一定条件下,用
 消除NO污染,其反应原理为:
消除NO污染,其反应原理为:
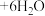 。不同温度条件下,
。不同温度条件下, 为
为 时,得到NO脱除率曲线如图所示。脱除NO的最佳温度是
时,得到NO脱除率曲线如图所示。脱除NO的最佳温度是
您最近一年使用:0次
名校
解题方法
4 . 氮元素是生命体核酸与蛋白质必不可少的组成元素,氮及其化合物在国民经济中占有重要地位。
(1)氨催化氧化制得硝酸的同时,排放的氮氧化物也是环境的主要污染物之一。
已知:





则反应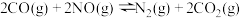

_______ 。
(2)在容积均为2 L的三个恒容密闭容器中分别通入1 mol CO和1 mol NO,发生反应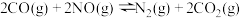 ,a、b、c三组实验的反应温度分别记为Ta、Tb、Tc。恒温恒容条件下反应各体系压强的变化曲线如图所示。
,a、b、c三组实验的反应温度分别记为Ta、Tb、Tc。恒温恒容条件下反应各体系压强的变化曲线如图所示。

①三组实验对应温度的大小关系是_______ (用Ta、Tb、Tc表示),0~20 min内,实验b中v(CO2)=_______  。
。
②实验a条件下,反应的平衡常数K=_______  。
。
(3)工业用铂丝网作催化剂,温度控制在780~840℃,将NH3转化为NO,反应方程式为 。回答下列问题:
。回答下列问题:
①NH3催化氧化速率 ,k为常数。当氧气浓度为
,k为常数。当氧气浓度为 时,c(NH3)与速率的关系如表所示,则a=
时,c(NH3)与速率的关系如表所示,则a=_______ 。
②其他反应条件相同时,测得不同温度下相同时间内NH3的转化率如图所示。则A点对应的反应速率v(正)_______ (填“>”、“<”或“=”)v(逆),A、C点对应条件下,反应平衡常数较大的是_______ (填“A”或“C”),理由是_______ 。

(1)氨催化氧化制得硝酸的同时,排放的氮氧化物也是环境的主要污染物之一。
已知:






则反应
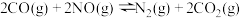

(2)在容积均为2 L的三个恒容密闭容器中分别通入1 mol CO和1 mol NO,发生反应
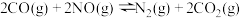 ,a、b、c三组实验的反应温度分别记为Ta、Tb、Tc。恒温恒容条件下反应各体系压强的变化曲线如图所示。
,a、b、c三组实验的反应温度分别记为Ta、Tb、Tc。恒温恒容条件下反应各体系压强的变化曲线如图所示。
①三组实验对应温度的大小关系是
 。
。②实验a条件下,反应的平衡常数K=
 。
。(3)工业用铂丝网作催化剂,温度控制在780~840℃,将NH3转化为NO,反应方程式为
 。回答下列问题:
。回答下列问题:①NH3催化氧化速率
 ,k为常数。当氧气浓度为
,k为常数。当氧气浓度为 时,c(NH3)与速率的关系如表所示,则a=
时,c(NH3)与速率的关系如表所示,则a= | 0.8 | 1.6 | 3.2 | 6.4 |
 | 10.2 | 81.6 | 652.8 | 5222.4 |

您最近一年使用:0次
2021-04-09更新
|
1915次组卷
|
10卷引用:广东省惠州市第一中学2021-2022学年高二上学期第二次考试化学试题
广东省惠州市第一中学2021-2022学年高二上学期第二次考试化学试题广东省惠州市第一中学2021-2022学年高二上学期期中考试化学试题山东省百所名校2021届高三下学期4月份(第三次)联考化学试题广东部分学校2021届高三4月模拟考试化学试题(已下线)难点5 化学反应速率与化学平衡图表分析-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第18题 化学反应原理综合题-备战2021年高考化学临考题号押题(山东卷)(已下线)第17周 晚练题-备战2022年高考化学周测与晚练(新高考专用)吉林省长春外国语学校2021-2022学年高二上学期期末考试化学试题(已下线)2022年全国甲卷高考真题变式题(非选择题)(已下线)2022年全国乙卷高考变式题(非选择题)
解题方法
5 . 二氧化碳和氨的利用是我国能源领域的一个重要战略方向,目前我国科学家在以下方面已经取得重大成果。
Ⅰ.(1)①图1是由 制取C的太阳能工艺。已知过程1中
制取C的太阳能工艺。已知过程1中 与
与 反应时
反应时 ,则
,则 的化学式为
的化学式为___________ 。
②过程1生成 的反应热为
的反应热为 ;过程2产生
;过程2产生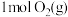 的反应热为
的反应热为 。则制取C的反应
。则制取C的反应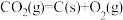 的
的 为
为___________ 。

Ⅱ.以 和
和 为原料合成尿素的化学方程式为
为原料合成尿素的化学方程式为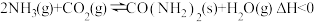 。
。
(2)合成的粗尿素中含有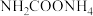 杂质。通过控制温度和压强,可将
杂质。通过控制温度和压强,可将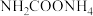 分解为
分解为 和
和 。研究温度和压强对
。研究温度和压强对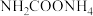 分解率的影响,结果如下:
分解率的影响,结果如下:

若X代表压强,则温度:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)工业上含尿素的废水需经处理后才能排放。如图为一种电化学降解尿素的装置示意图,该过程中,尿素降解的产物之一为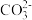 :
:
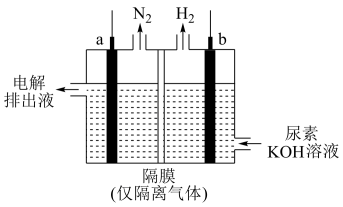
写出尿素被降解的电极反应式:___________ 。
Ⅲ.在200℃时,向 带气压计的恒容密闭容器中通入
带气压计的恒容密闭容器中通入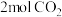 和
和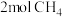 发生反应
发生反应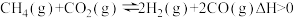 ,测得初始压强为
,测得初始压强为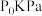 ,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。
,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。

(4)该反应过程中从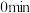 到
到 压强变小原因是
压强变小原因是___________ 。
(5)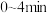 内,反应的平均反应速率
内,反应的平均反应速率
___________ 。
(6)用平衡分压代替平衡浓度表示的化学平衡常数
___________ 。[气体分压 气体总压
气体总压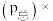 气体体积分数]
气体体积分数]
Ⅰ.(1)①图1是由
 制取C的太阳能工艺。已知过程1中
制取C的太阳能工艺。已知过程1中 与
与 反应时
反应时 ,则
,则 的化学式为
的化学式为②过程1生成
 的反应热为
的反应热为 ;过程2产生
;过程2产生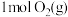 的反应热为
的反应热为 。则制取C的反应
。则制取C的反应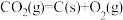 的
的 为
为
Ⅱ.以
 和
和 为原料合成尿素的化学方程式为
为原料合成尿素的化学方程式为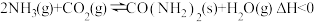 。
。(2)合成的粗尿素中含有
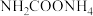 杂质。通过控制温度和压强,可将
杂质。通过控制温度和压强,可将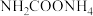 分解为
分解为 和
和 。研究温度和压强对
。研究温度和压强对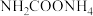 分解率的影响,结果如下:
分解率的影响,结果如下:
若X代表压强,则温度:

 (填“>”或“<”)。
(填“>”或“<”)。(3)工业上含尿素的废水需经处理后才能排放。如图为一种电化学降解尿素的装置示意图,该过程中,尿素降解的产物之一为
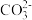 :
:
写出尿素被降解的电极反应式:
Ⅲ.在200℃时,向
 带气压计的恒容密闭容器中通入
带气压计的恒容密闭容器中通入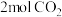 和
和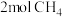 发生反应
发生反应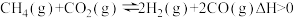 ,测得初始压强为
,测得初始压强为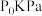 ,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。
,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。
(4)该反应过程中从
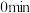 到
到 压强变小原因是
压强变小原因是(5)
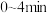 内,反应的平均反应速率
内,反应的平均反应速率
(6)用平衡分压代替平衡浓度表示的化学平衡常数

 气体总压
气体总压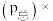 气体体积分数]
气体体积分数]
您最近一年使用:0次
名校
解题方法
6 . 绿水青山是习总书记构建美丽中国的伟大设想,研究碳、氮、硫等废气的处理对建设美丽中国具有重要意义。
(1)用CO2可以生产燃料甲醇。
已知: △H=-a kJ/mol
△H=-a kJ/mol
 △H=-b kJ/mol
△H=-b kJ/mol
则表示 燃烧的热化学方程式为
燃烧的热化学方程式为_______ 。
(2)某温度 下,将6 mol CO2和8 molH2充入一容积为2 L的密闭容器中发生
下,将6 mol CO2和8 molH2充入一容积为2 L的密闭容器中发生 △H<0反应,测得H2的物质的量随时间变化如图中实线所示。
△H<0反应,测得H2的物质的量随时间变化如图中实线所示。

请回答下列问题:
①前 分钟内,H2的平均反应速率为
分钟内,H2的平均反应速率为_______  (保留两位小数)。
(保留两位小数)。
②下列表述能表示该反应已达平衡的是_______ (填序号)。
a.容器内压强不再改变 b.容器内气体的密度不再改变
c.容器内气体的平均摩尔质量不再改变 d.容器内各物质的物质的量相等
③在温度 时,该反应的化学平衡常数为
时,该反应的化学平衡常数为_______ 。
④仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,改变条件的方式可能是_______ 。
(3)二氧化硫一空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。

在该燃料电池中,负极的电极方程式为_______ 。
(1)用CO2可以生产燃料甲醇。
已知:
 △H=-a kJ/mol
△H=-a kJ/mol △H=-b kJ/mol
△H=-b kJ/mol 则表示
 燃烧的热化学方程式为
燃烧的热化学方程式为(2)某温度
 下,将6 mol CO2和8 molH2充入一容积为2 L的密闭容器中发生
下,将6 mol CO2和8 molH2充入一容积为2 L的密闭容器中发生 △H<0反应,测得H2的物质的量随时间变化如图中实线所示。
△H<0反应,测得H2的物质的量随时间变化如图中实线所示。
请回答下列问题:
①前
 分钟内,H2的平均反应速率为
分钟内,H2的平均反应速率为 (保留两位小数)。
(保留两位小数)。②下列表述能表示该反应已达平衡的是
a.容器内压强不再改变 b.容器内气体的密度不再改变
c.容器内气体的平均摩尔质量不再改变 d.容器内各物质的物质的量相等
③在温度
 时,该反应的化学平衡常数为
时,该反应的化学平衡常数为④仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,改变条件的方式可能是
(3)二氧化硫一空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。

在该燃料电池中,负极的电极方程式为
您最近一年使用:0次
2021-01-30更新
|
262次组卷
|
4卷引用:广东省惠州市2020-2021学年高二上学期期末考试化学试题
7 . 合成氨是目前最有效工业固氮的方法,解决数亿人口生存问题。回答下列问题:
(1)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。

由图可知合成氨反应 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的∆H=
NH3(g)的∆H=___ kJ·mol-1。该历程中反应速率最慢的步骤的化学方程式为___ 。
(2)工业合成氨反应为:N2(g)+3H2(g) 2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
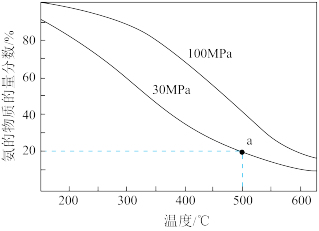
①500℃时,反应平衡常数Kp(30MPa)___ Kp(100MPa)。(填“<”、“=”、“>”)
②500℃、30MPa时,氢气的平衡转化率为___ (保留2位有效数字),Kp=___ (MPa)-2(列出计算式)。
(3)科学家利用电解法在常温常压下实现合成氨,工作时阴极区的微观示意如图,其中电解液为溶解有三氟甲磺酸锂和乙醇的惰性有机溶剂。
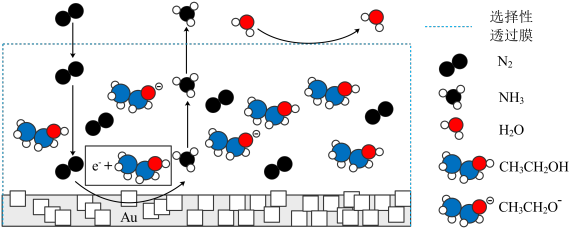
①阴极区生成NH3的电极方程式为___ 。
②下列说法正确的是___ (填标号)。
A.三氟甲磺酸锂的作用是增强导电性
B.该装置用金(Au)作催化剂目的是降低N2的键能
C.选择性透过膜可允许N2和NH3通过,防止H2O进入装置
(1)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。

由图可知合成氨反应
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的∆H=
NH3(g)的∆H=(2)工业合成氨反应为:N2(g)+3H2(g)
 2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
①500℃时,反应平衡常数Kp(30MPa)
②500℃、30MPa时,氢气的平衡转化率为
(3)科学家利用电解法在常温常压下实现合成氨,工作时阴极区的微观示意如图,其中电解液为溶解有三氟甲磺酸锂和乙醇的惰性有机溶剂。

①阴极区生成NH3的电极方程式为
②下列说法正确的是
A.三氟甲磺酸锂的作用是增强导电性
B.该装置用金(Au)作催化剂目的是降低N2的键能
C.选择性透过膜可允许N2和NH3通过,防止H2O进入装置
您最近一年使用:0次
2020-03-30更新
|
918次组卷
|
4卷引用:广东省惠州市惠城区2021--2022学年高三上学期8月开学摸底化学试题
广东省惠州市惠城区2021--2022学年高三上学期8月开学摸底化学试题陕西省西北工业大学附中2020-2021学年高二下学期期中考试化学试题广东省广州市2020届高三年级3月阶段训练(全国I卷)理综化学试题(已下线)01 化学反应原理综合题型集训之催化剂、活化能与反应历程(解析)-备战2023年高考化学大题逐空突破系列(全国通用)



