名校
1 . 下列有关化学实验说法正确的是


| A.铁片上电镀锌时,通常把铁片做阳极 |
| B.如图验证热效应的氢氧化钡晶体与氯化铵晶体反应操作中,通常小木板上要洒少量水 |
| C.反应热测量时,量筒中的氢氧化钠溶液要缓慢倒入盛有盐酸的简易量热计中 |
| D.为了证明HClO是弱酸,可用广泛pH试纸测常温下NaClO溶液的pH |
您最近一年使用:0次
2022-01-11更新
|
211次组卷
|
2卷引用:山东省滕州市第一中学2022-2023学年高二上学期1月期末考试化学试题
2 . 化学能与热能、电能等可以相互转化.关于化学能与其他能量相互转化的说法正确的是( )
A. 将化学能转变为电能 将化学能转变为电能 |
B.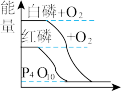 白磷比红磷稳定 白磷比红磷稳定 |
C.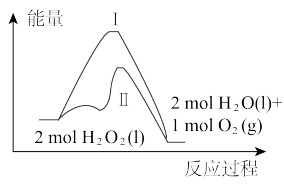 发生的反应为放热反应 发生的反应为放热反应 |
D. 证明在其他条件相同时,按途径Ⅰ发生反应与按途径Ⅱ发生反应,并产生相等质量氧气时放出的热量不相等 证明在其他条件相同时,按途径Ⅰ发生反应与按途径Ⅱ发生反应,并产生相等质量氧气时放出的热量不相等 |
您最近一年使用:0次
名校
3 . 下列叙述正确的是
| A.华为自主研发的“麒麟”芯片与太阳能电池感光板所用材料均为二氧化硅 |
B.同温同压下氢气和氯气反应生成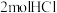 ,光照和点燃条件下反应的焓变不同 ,光照和点燃条件下反应的焓变不同 |
C. 比 比 还原性强,证明硅的非金属性比碳弱 还原性强,证明硅的非金属性比碳弱 |
| D.某化学反应中,反应物化学键中储存的总能量比反应产物化学键中储存的总能量低,则该反应是放热反应。 |
您最近一年使用:0次
名校
4 . 甲酸 又名蚁酸,是一种常见的弱酸,常温下甲酸的电离平衡常数
又名蚁酸,是一种常见的弱酸,常温下甲酸的电离平衡常数 (已知
(已知 )。
)。
(1)设计实验证明甲酸为弱酸,下列实验设计合理的是_______ (填选项字母)。
A.将甲酸溶液滴入 溶液中,观察是否有气泡生成
溶液中,观察是否有气泡生成
B.向体积相同、 相同的盐酸和甲酸溶液中加入足量
相同的盐酸和甲酸溶液中加入足量 ,比较溶解
,比较溶解 的质量
的质量
C.取一定浓度的甲酸钠溶液,测其
(2) 的甲酸钠
的甲酸钠 溶液和
溶液和 的甲酸溶液等体积混合可配成一种缓冲溶液。
的甲酸溶液等体积混合可配成一种缓冲溶液。
① 的水解平衡常数
的水解平衡常数
_______ 。
②该混合溶液的 约为
约为_______ 。
③该混合溶液中
_______ (填“>”“=”或“<”)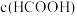 。
。
(3)催化甲酸分解的一种反应机理和相对能量的变化情况如图所示。

①已知催化剂“I”带一个正电荷,反应过程中的中间产物也带一个正电荷的是_______ (填“II”“III”或“IV”)。
②由反应进程可知甲酸分解的
_______ (填“>”“=”或“<”)0,该历程中的决速步骤为_______ (填选项字母),历程中最大能垒(活化能)
_______  。
。
a.I转化为II的过程 b.II转化为III的过程
c.III转化为IV的过程 d.IV转化为I的过程
 又名蚁酸,是一种常见的弱酸,常温下甲酸的电离平衡常数
又名蚁酸,是一种常见的弱酸,常温下甲酸的电离平衡常数 (已知
(已知 )。
)。(1)设计实验证明甲酸为弱酸,下列实验设计合理的是
A.将甲酸溶液滴入
 溶液中,观察是否有气泡生成
溶液中,观察是否有气泡生成B.向体积相同、
 相同的盐酸和甲酸溶液中加入足量
相同的盐酸和甲酸溶液中加入足量 ,比较溶解
,比较溶解 的质量
的质量C.取一定浓度的甲酸钠溶液,测其

(2)
 的甲酸钠
的甲酸钠 溶液和
溶液和 的甲酸溶液等体积混合可配成一种缓冲溶液。
的甲酸溶液等体积混合可配成一种缓冲溶液。①
 的水解平衡常数
的水解平衡常数
②该混合溶液的
 约为
约为③该混合溶液中

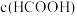 。
。(3)催化甲酸分解的一种反应机理和相对能量的变化情况如图所示。

①已知催化剂“I”带一个正电荷,反应过程中的中间产物也带一个正电荷的是
②由反应进程可知甲酸分解的


 。
。a.I转化为II的过程 b.II转化为III的过程
c.III转化为IV的过程 d.IV转化为I的过程
您最近一年使用:0次
2023-01-05更新
|
373次组卷
|
3卷引用:山东省滕州市第一中学2022-2023学年高二上学期1月期末考试化学试题
名校
解题方法
5 . 为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
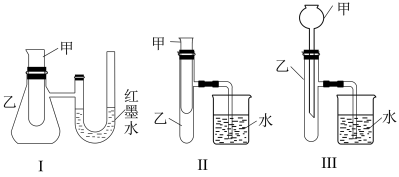
(1)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,根据所学知识推测该反应属于_______ (填“吸热”或“放热”)反应,预测U形管中可观察到的现象是_______ 。
(2)选择装置II进行探究固体M在甲中溶于水的热效应。
①若M为 ,则实验过程中烧杯中可观察到的现象是
,则实验过程中烧杯中可观察到的现象是_______ 。
②若M为NaOH,则实验过程中烧杯中可观察到的现象为_______ 。
(3)上述3个装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是_______ (填序号)。理由是_______ 。
(4)至少有两种实验方法能证明过氧化钠与水的反应(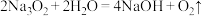 )是放热反应。
)是放热反应。
方法①:选择上述装置_______ (填“I”、“II”或“III”)进行实验。
方法②:取适量过氧化钠粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到_______ ,则说明该反应是放热反应。

(1)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,根据所学知识推测该反应属于
(2)选择装置II进行探究固体M在甲中溶于水的热效应。
①若M为
 ,则实验过程中烧杯中可观察到的现象是
,则实验过程中烧杯中可观察到的现象是②若M为NaOH,则实验过程中烧杯中可观察到的现象为
(3)上述3个装置中,不能用来证明“锌和稀硫酸反应是吸热反应还是放热反应”的是
(4)至少有两种实验方法能证明过氧化钠与水的反应(
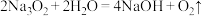 )是放热反应。
)是放热反应。方法①:选择上述装置
方法②:取适量过氧化钠粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到
您最近一年使用:0次
2022-11-21更新
|
280次组卷
|
2卷引用:山东省滨州市沾化区、阳信县2022-2023学年高一下学期期中联考化学(B)试题
6 . 研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
(1)反应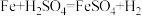 的能量变化如图1所示。
的能量变化如图1所示。
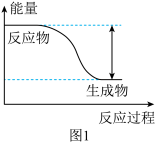
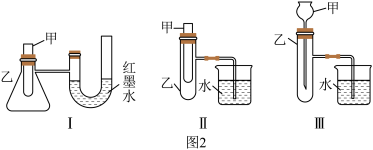
①该反应为_______ (填“吸热”或“放热”)反应。
②图2的3个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是_______ 。
(2)现有纯铁片、纯铜片、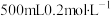 的硫酸溶液、导线和
的硫酸溶液、导线和 量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且 量筒中已充满了水。
量筒中已充满了水。
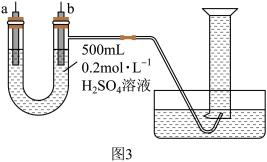
①若a、b极不用导线相连,则b极材料为_______ (填“纯铁片”或“纯铜片”)。
②将a、b极(a极为“纯铁片”,b极为“纯铜片”)用导线相连,则电子在导线上的流动方向为从_______ 到(填“a极”或“b极”,下同)_______ ;此时a极的电极反应式为_______ 。
③根据上述实验所得结论为_______ 。
(1)反应
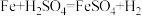 的能量变化如图1所示。
的能量变化如图1所示。
①该反应为
②图2的3个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是

(2)现有纯铁片、纯铜片、
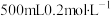 的硫酸溶液、导线和
的硫酸溶液、导线和 量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且 量筒中已充满了水。
量筒中已充满了水。
①若a、b极不用导线相连,则b极材料为
②将a、b极(a极为“纯铁片”,b极为“纯铜片”)用导线相连,则电子在导线上的流动方向为从
③根据上述实验所得结论为
您最近一年使用:0次
名校
7 . 化学反应过程既是物质的转化过程,也是化学能与热能,电能等其他形式能量的转化过程。请根据要求回答下列与能量转化有关的问题:
I.利用如图所示装置测定中和热,取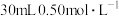 稀硫酸与
稀硫酸与 溶液进行实验,实验数据如表。
溶液进行实验,实验数据如表。
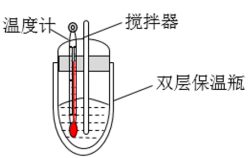
回答下列问题:
(1)若近似认为 稀硫酸与
稀硫酸与 溶液的密度均为
溶液的密度均为 (忽略溶液混合后体积变化),反应所得溶液的比热容
(忽略溶液混合后体积变化),反应所得溶液的比热容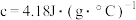 ,则实验测定中和热的数值为
,则实验测定中和热的数值为_______  (保留1位小数)。
(保留1位小数)。
(2)上述实验结果与中和热的标准数值 有偏差,产生偏差的原因不可能是因为_____。
有偏差,产生偏差的原因不可能是因为_____。
(3)如图三个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是_______ 。
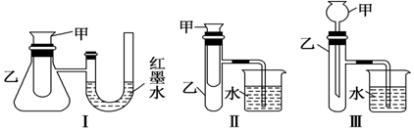
II.
(4)请用下图所示仪器装置设计一个包括:电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。
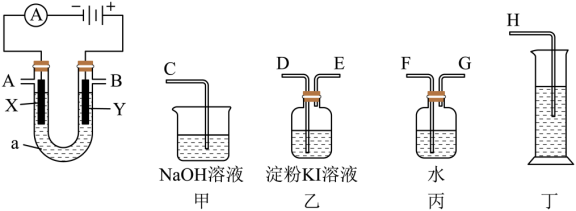
①所选仪器连接时,各接口的顺序是___________ (填各接口的字母代号):
A接______、_____接_____;B接_____、______接______;
②体现氯气的氧化性的实验现象为:_______ ,电解一段时间后,用丁测得气体体积为280mL(标准状况下);需加入_______ g(结果保留一位小数)的_______ 可使溶液复原。
| 温度 实验次数 | 起始温度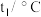 | 终止温度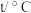 | ||
 |  | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.2 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.3 |
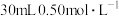 稀硫酸与
稀硫酸与 溶液进行实验,实验数据如表。
溶液进行实验,实验数据如表。
回答下列问题:
(1)若近似认为
 稀硫酸与
稀硫酸与 溶液的密度均为
溶液的密度均为 (忽略溶液混合后体积变化),反应所得溶液的比热容
(忽略溶液混合后体积变化),反应所得溶液的比热容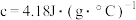 ,则实验测定中和热的数值为
,则实验测定中和热的数值为 (保留1位小数)。
(保留1位小数)。(2)上述实验结果与中和热的标准数值
 有偏差,产生偏差的原因不可能是因为_____。
有偏差,产生偏差的原因不可能是因为_____。| A.实验装置保温、隔热效果差 |
| B.用量筒量取NaOH溶液的体积时仰视读数 |
| C.分多次把NaOH溶液倒入内筒中 |
| D.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度 |

II.
(4)请用下图所示仪器装置设计一个包括:电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。

①所选仪器连接时,各接口的顺序是
A接______、_____接_____;B接_____、______接______;
②体现氯气的氧化性的实验现象为:
您最近一年使用:0次
名校
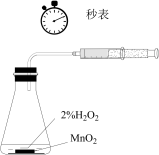
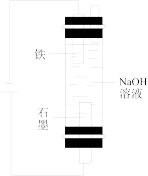
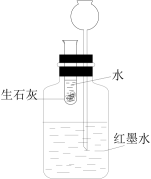
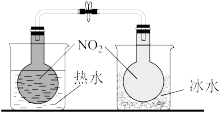
8 . 利用下列实验装置无法实现实验目的的是
 |  |  |  |
| ① | ② | ③ | ④ |
| A.用装置①测量2%双氧水分解生成O2的化学反应速率 |
B.用装置②制备 并能较长时间观察其颜色 并能较长时间观察其颜色 |
| C.用装置③证明生石灰与水反应是放热反应 |
| D.用装置④探究温度对化学平衡的影响 |
您最近一年使用:0次
2021-11-18更新
|
226次组卷
|
3卷引用:山东省青岛市4区市2021-2022学年高二上学期期中考试化学试题
9 . 下列实验操作不能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向1mL2mol·L-1FeCl3溶液中加入1mL1mol·L-1KI溶液,萃取分液后向水层滴入KSCN溶液,观察溶液颜色变化 | 探究Fe3+与I-的反应是否可逆 |
| B | 向烧杯中加入70g研细的Ca(OH)2晶体和50gNH4Cl晶体,并将烧杯放在滴有水的玻璃片上,用玻璃棒迅速搅拌,观察实验现象 | 证明吸热反应不一定需要加热才能进行 |
| C | 向某溶液中滴加K3[Fe(CN)6]溶液,观察是否产生蓝色沉淀 | 证明某溶液中有Fe2+,无Fe3+ |
| D | 相同条件下,用20mL1.0mol·L-1醋酸溶液和50mL1.0mol·L-1盐酸分别做导电性实验,观察对应灯泡明暗程度 | 证明醋酸是弱电解质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 综合利用研究发现,硼镁铁矿(主要成分为 ,含有SiO2、FeO、Fe2O3等杂质)可以制备硼酸、铁红和碳酸镁等常用化工试剂,工艺流程图如下:
,含有SiO2、FeO、Fe2O3等杂质)可以制备硼酸、铁红和碳酸镁等常用化工试剂,工艺流程图如下:
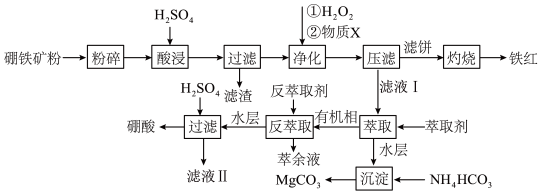
回答下列问题:
(1)硼镁矿粉碎的目的是 发生的离子反应是
发生的离子反应是
(2)为提高产品纯度,“净化”时用的试剂X为
(3)过滤所得碳酸镁需冷水洗涤后再进行干燥证明碳酸镁固体洗涤干净的具体操作为
(4)不同条件下硼酸的萃取率图象如下:
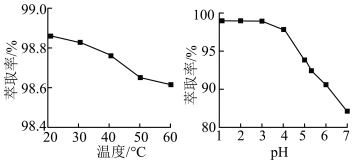
萃取过程为
您最近一年使用:0次
2021-05-23更新
|
404次组卷
|
3卷引用:山东省济南市2021届高三第三次摸底考试化学试题



