解题方法
1 . 化学物质在汽车的动力、安全等方面有着极为重要的作用。
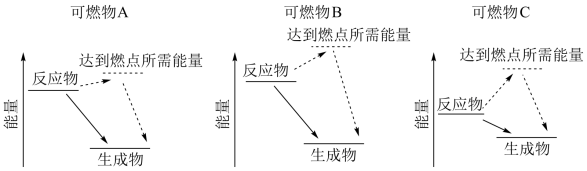
(1)某同学根据所查阅的资料,绘制了三种可燃物在空气中发生燃烧反应的能量变化示意图。根据示意图,你认为可燃物_______ (填“A”、“B”或“C”)更适合用作车用燃料。(已知:燃点是指在规定的条件下,应用外部热源使物质表面起火并持续燃烧一定时间所需的最低温度,燃点较低时存在安全隐患。)
(2)汽车尾气中含有 、
、 等污染物。其中
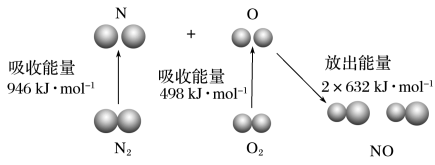
等污染物。其中 生成过程的能量变化如图,由该图数据计算可得,该反应为
生成过程的能量变化如图,由该图数据计算可得,该反应为_______ (填“吸热”或“放热”)反应。
(3)通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 的含量,其工作原理如图所示:
的含量,其工作原理如图所示:
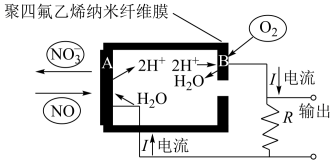
①A电极发生的是_______ 反应(填“氧化”或“还原”)。
②B电极反应为_______ 。
(4)电动汽车普遍使用锂离子电池。某锂离子电池反应为 。
。
①当有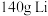 消耗时,电路中转移电子数目为
消耗时,电路中转移电子数目为_______ 。
②根据①的计算思路,分析 做电极优于
做电极优于 的原因是
的原因是_______ 。
(5)安全性是汽车发展需要解决的重要问题。汽车受到强烈撞击时,预置在安全气囊内的化学药剂发生反应产生大量气体,气囊迅速弹出。某种产气药剂主要含有 、
、 、
、 、
、 ,已知
,已知 在猛烈撞击时分解产生两种单质,并放出大量的热。
在猛烈撞击时分解产生两种单质,并放出大量的热。
①药剂中 做冷却剂原因是
做冷却剂原因是_______ 。
②根据产气药剂的组成,在设计气囊中所运用的化学反应时,需要考虑的角度有_______ (填标号)。
A.固体反应物的颜色 B.气体产物的毒性 C.反应的快慢 D.反应的能量变化
(1)某同学根据所查阅的资料,绘制了三种可燃物在空气中发生燃烧反应的能量变化示意图。根据示意图,你认为可燃物

(2)汽车尾气中含有
 、
、 等污染物。其中
等污染物。其中 生成过程的能量变化如图,由该图数据计算可得,该反应为
生成过程的能量变化如图,由该图数据计算可得,该反应为
(3)通过
 传感器可监测汽车尾气中
传感器可监测汽车尾气中 的含量,其工作原理如图所示:
的含量,其工作原理如图所示:
①A电极发生的是
②B电极反应为
(4)电动汽车普遍使用锂离子电池。某锂离子电池反应为
 。
。①当有
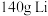 消耗时,电路中转移电子数目为
消耗时,电路中转移电子数目为②根据①的计算思路,分析
 做电极优于
做电极优于 的原因是
的原因是(5)安全性是汽车发展需要解决的重要问题。汽车受到强烈撞击时,预置在安全气囊内的化学药剂发生反应产生大量气体,气囊迅速弹出。某种产气药剂主要含有
 、
、 、
、 、
、 ,已知
,已知 在猛烈撞击时分解产生两种单质,并放出大量的热。
在猛烈撞击时分解产生两种单质,并放出大量的热。①药剂中
 做冷却剂原因是
做冷却剂原因是②根据产气药剂的组成,在设计气囊中所运用的化学反应时,需要考虑的角度有
A.固体反应物的颜色 B.气体产物的毒性 C.反应的快慢 D.反应的能量变化
您最近一年使用:0次
名校
解题方法
2 . 化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d.铜溶于浓硝酸 e.氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)H2O2分解时的能量变化关系如图所示,则H2O2分解反应为___________ 反应 (选填:吸热、放热)。
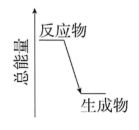
查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和___________ 。
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置:
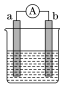
①当电极a为镁,电极b为铝,电解质溶液为氢氧化钠溶液时,该电池的负极为___________ (填名称)。
②燃料电池的工作原理是将燃料和氧化剂(O2)反应所产生的化学能直接转化为电能。现设计一燃料电池,电极a通入氢气燃料,采用氢氧化钠溶液为电解液,b极的电极反应式为___________ 。
③质量相同的铜棒和铁棒用导线连接后插入CuSO4溶液中,一段时间后,取出洗净、干燥、称量,二者质量差为12 g,则导线中通过的电子的数目为___________ 。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d.铜溶于浓硝酸 e.氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)H2O2分解时的能量变化关系如图所示,则H2O2分解反应为

查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置:

①当电极a为镁,电极b为铝,电解质溶液为氢氧化钠溶液时,该电池的负极为
②燃料电池的工作原理是将燃料和氧化剂(O2)反应所产生的化学能直接转化为电能。现设计一燃料电池,电极a通入氢气燃料,采用氢氧化钠溶液为电解液,b极的电极反应式为
③质量相同的铜棒和铁棒用导线连接后插入CuSO4溶液中,一段时间后,取出洗净、干燥、称量,二者质量差为12 g,则导线中通过的电子的数目为
您最近一年使用:0次
2021-05-11更新
|
269次组卷
|
2卷引用:山东省济宁市任城区2020-2021学年高一下学期期中考试化学试题
解题方法
3 . 2022年3月23日,“天宫课堂”第二课中王亚平老师用结构为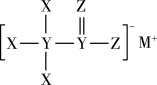 的物质制作出“冰球”,其中X、Y、Z、M是原子序数依次增大的短周期主族元素,M的焰色试验中火焰呈黄色。下列说法错误的是
的物质制作出“冰球”,其中X、Y、Z、M是原子序数依次增大的短周期主族元素,M的焰色试验中火焰呈黄色。下列说法错误的是
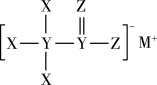 的物质制作出“冰球”,其中X、Y、Z、M是原子序数依次增大的短周期主族元素,M的焰色试验中火焰呈黄色。下列说法错误的是
的物质制作出“冰球”,其中X、Y、Z、M是原子序数依次增大的短周期主族元素,M的焰色试验中火焰呈黄色。下列说法错误的是| A.该物质中含有离子键、极性共价键和非极性共价键 |
| B.最简单氢化物的稳定性:Z<Y |
| C.Z的两种常见同素异形体均有氧化性 |
| D.X、Y、Z、M形成的无机盐与柠檬酸反应是放热反应 |
您最近一年使用:0次
4 . NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图1;研究发现在催化剂上可能发生的反应过程如图2。下列说法不正确的是
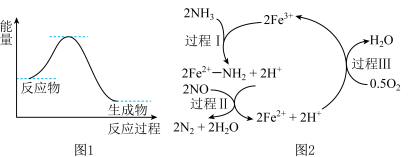

| A.NH3催化还原NO为放热反应 |
| B.过程I中NH3断裂极性键,需要吸收能量,Fe3+体现了氧化性 |
C.过程III的离子方程式: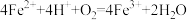 |
| D.反应过程中,反应物为NH3、O2、NO,Fe3+、Fe2+为中间产物 |
您最近一年使用:0次
2021-09-26更新
|
982次组卷
|
16卷引用:山东省“学情空间”区域教研共同体2022-2023学年高三上学期10月检测化学试题
山东省“学情空间”区域教研共同体2022-2023学年高三上学期10月检测化学试题浙江省“精诚联盟”2021-2022学年高二上学期返校考试化学试题江西省抚州市临川一中、临川一中实验学校2022届高三第一次月考化学试题(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)吉林省长春市北师大附属学校2021-2022学年高三上学期第一次月考化学试题天津市红桥区2021-2022学年高三上学期期中考试化学试题(已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)浙江省金华市第六中学2022-2023学年高二上学期开学考试化学试题四川省成都市郫都区2021-2022学年高二上学期期中考试化学试题湖南省宁乡市四校联考2022-2023学年高二上学期10月月考化学试题湖北省襄阳市第三中学2021-2022学年高一下学期3月月考化学试题四川省凉山州西昌市第二中学2021-2022学年高二上学期期末检测化学试题浙江省名校协作体2023-2024学年高二上学期开学适应性考试化学试题吉林省通化市梅河口市第五中学2022-2023学年高三上学期10月期中考试化学试题湖南省常德市第一中学2023-2024学年高二上学期入学考试化学试题上海市控江中学2023-2024学年高二上学期10月阶段测验化学试题
解题方法
5 . 化学知识无处不在,下列活动内容不能用对应的化学知识解释的是
| 选项 | 活动内容 | 化学知识 |
| A | 硫酸铜可以用来检验酒精中是否还有少量水 | 硫酸铜结合水会变成蓝色晶体 |
| B | 在葡萄酒酿制过程中加入少量SO2 | SO2具有杀菌、抗氧化等作用 |
| C | 冷敷袋在日常生活中有降温、保鲜和镇疼等用途 | 袋中盛装的硝酸铵和水发生吸热反应 |
| D | “84消毒液”稀释后拖地 | 利用NaClO的氧化性消毒杀菌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . Ⅰ.完成下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。
①已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ 。
a.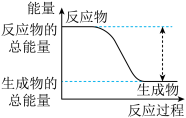 b.
b. 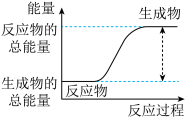
②从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量_______ kJ。
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
Ⅱ.完成下列问题
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原 电池, 则负极所用电极材料为_______ 。
(4)H2和 O2组合形成的燃料电池的结构如图(电解液是稀硫酸):
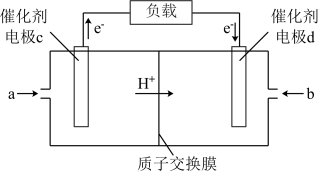
电极 d 的电极反应式为_______ 。
(5)氨氧燃料电池具有很大的发展潜力,其工作原理如图 3 所示。a电极上的反应式为_______ 。
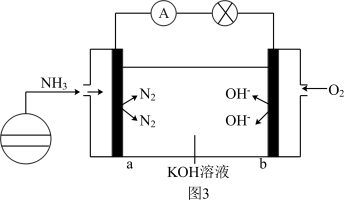
(6)高铁电池是一种新型可充电电池。高铁电池的总反应式为: 3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为
3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为_______ 。
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。
①已知该反应为放热反应,下图能正确表示该反应中能量变化的是
a.
 b.
b. 
②从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H-H | O=O | H-O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出热量
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
Ⅱ.完成下列问题
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原 电池, 则负极所用电极材料为
(4)H2和 O2组合形成的燃料电池的结构如图(电解液是稀硫酸):

电极 d 的电极反应式为
(5)氨氧燃料电池具有很大的发展潜力,其工作原理如图 3 所示。a电极上的反应式为

(6)高铁电池是一种新型可充电电池。高铁电池的总反应式为: 3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为
3Zn(OH)2+2Fe(OH)3+4KOH。已知负极反应式为 Zn-2e-+2OH-=Zn(OH)2,则正极反应为
您最近一年使用:0次
名校
7 . 废水对自然环境有严重的破坏作用,水污染治理刻不容缓,BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法不正确的是( )
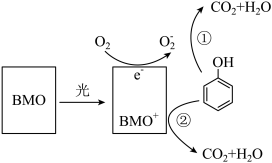

| A.该过程中O2-e-=O2- |
| B.①和②中BMO+和O-都表现较强氧化性 |
| C.催化剂BMO能降低反应的反应热和活化能 |
| D.该过程为放热反应 |
您最近一年使用:0次
2020-04-04更新
|
201次组卷
|
3卷引用:山东省青岛市莱西第一中学2020届高三下学期质量检测化学试题
山东省青岛市莱西第一中学2020届高三下学期质量检测化学试题山东省淄博市高青县第一中学2021-2022学年高二10月月考化学试题(已下线)小题必刷07 氧化还原反应概念及应用——2021年高考化学一轮复习小题必刷(通用版)
名校
解题方法
8 . 2021年10月16日6时56分,神舟十三号载人飞船与空间站组合体完成自主快速交会对接。中国空间站开启有人长期驻留时代。空间站的水气整合系统利用“萨巴蒂尔反应”,将 转化为
转化为 和水蒸气,配合
和水蒸气,配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:
I.萨巴蒂尔反应为:

(1)在某一恒容密闭容器中加入 、
、 ,其分压分别为
,其分压分别为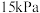 、
、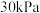 ,加入催化剂并加热使其发生萨巴蒂尔反应。研究表明
,加入催化剂并加热使其发生萨巴蒂尔反应。研究表明 的反应速率
的反应速率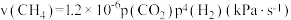 ,某时刻测得
,某时刻测得 的分压为
的分压为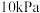 ,则该时刻
,则该时刻
______ 。
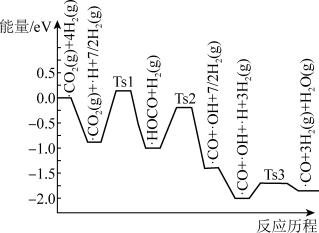
(2)研究发现萨巴蒂尔反应的历程,前三步历程如图所示。其中吸附在 催化剂表面用“.”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
催化剂表面用“.”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会______ (填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为______ 。
II.某研究团队经实验证明, 在一定条件下与
在一定条件下与 发生氧再生反应:
发生氧再生反应:
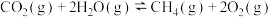
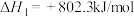
(3)氧再生反应可以通过酸性条件下半导体光催化转化实现;反应机理如图所示:
i.光催化 转化为
转化为 的阴极方程式为
的阴极方程式为______ 。
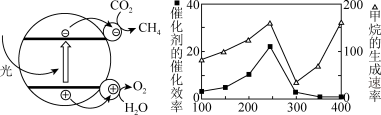
ii.催化剂的催化效率和 的生成速率随温度的变化关系如图所示。
的生成速率随温度的变化关系如图所示。 到
到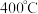 之间,
之间, 生成速率加快的原因是
生成速率加快的原因是______ 。
 转化为
转化为 和水蒸气,配合
和水蒸气,配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:I.萨巴蒂尔反应为:


(1)在某一恒容密闭容器中加入
 、
、 ,其分压分别为
,其分压分别为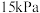 、
、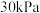 ,加入催化剂并加热使其发生萨巴蒂尔反应。研究表明
,加入催化剂并加热使其发生萨巴蒂尔反应。研究表明 的反应速率
的反应速率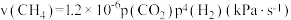 ,某时刻测得
,某时刻测得 的分压为
的分压为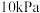 ,则该时刻
,则该时刻
(2)研究发现萨巴蒂尔反应的历程,前三步历程如图所示。其中吸附在
 催化剂表面用“.”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
催化剂表面用“.”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
II.某研究团队经实验证明,
 在一定条件下与
在一定条件下与 发生氧再生反应:
发生氧再生反应: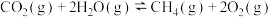
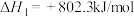
(3)氧再生反应可以通过酸性条件下半导体光催化转化实现;反应机理如图所示:

i.光催化
 转化为
转化为 的阴极方程式为
的阴极方程式为ii.催化剂的催化效率和
 的生成速率随温度的变化关系如图所示。
的生成速率随温度的变化关系如图所示。 到
到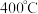 之间,
之间, 生成速率加快的原因是
生成速率加快的原因是
您最近一年使用:0次



