1 . ①H2O(l)=H2(g)+ O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是___________ 。(填序号)
(2)H2的燃烧热为___________ 。
(3)燃烧10gH2生成液态水,放出的热量为___________ 。
 O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10gH2生成液态水,放出的热量为
您最近半年使用:0次
2 . 在25℃、101 kPa下,1g液态甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式:___________ 。
您最近半年使用:0次
3 . 已知: 、
、 、
、 的燃烧热分别为
的燃烧热分别为 、
、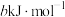 和
和 (a、b、c都大于0)。则反应
(a、b、c都大于0)。则反应 的
的 为
为
 、
、 、
、 的燃烧热分别为
的燃烧热分别为 、
、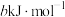 和
和 (a、b、c都大于0)。则反应
(a、b、c都大于0)。则反应 的
的 为
为A. | B.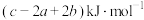 |
C.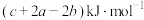 | D.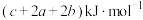 |
您最近半年使用:0次
4 . 下列关于热化学反应的描述正确的是
| A.HCl和NaOH反应的反应热ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3) kJ·mol-1 |
| B.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol-1 |
| C.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+566.0 kJ·mol-1 |
D.已知:500 ℃、30 MPa下,N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1;将3 mol H2和过量的N2在此条件下充分反应,会放出92.4 kJ热量 2NH3(g) ΔH=-92.4 kJ·mol-1;将3 mol H2和过量的N2在此条件下充分反应,会放出92.4 kJ热量 |
您最近半年使用:0次
5 . 填空
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:_____ 。反应III为_____ (选填“吸热”或“放热”)反应。
(2)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为_____ 。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____ 。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
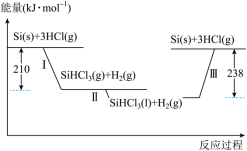
(2)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近半年使用:0次
名校
6 . 请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为___________ (填“吸热”或“放热”)反应,其中ΔH=___________ (用含有a、b的关系式表示)。___________ 114.6kJ(填“大于”、“等于”或“小于”)。
(3)在25℃,101kPa下,16g的N2H4(g)完全燃烧生成氮气和液态水时放热316kJ,则表示N2H4(g)燃烧热的热化学方程式为___________ 。
(4)甲醇(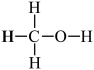 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=___________ 。
(1)如图表示某反应的能量变化关系,则此反应为
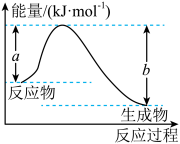
(3)在25℃,101kPa下,16g的N2H4(g)完全燃烧生成氮气和液态水时放热316kJ,则表示N2H4(g)燃烧热的热化学方程式为
(4)甲醇(
 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
您最近半年使用:0次
名校
7 . 已知 是一种高效清洁的火箭燃料。
是一种高效清洁的火箭燃料。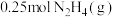 完全燃烧生成
完全燃烧生成 和
和 时,放出
时,放出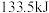 热量。则下列热化学方程式书写正确的是
热量。则下列热化学方程式书写正确的是
 是一种高效清洁的火箭燃料。
是一种高效清洁的火箭燃料。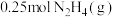 完全燃烧生成
完全燃烧生成 和
和 时,放出
时,放出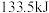 热量。则下列热化学方程式书写正确的是
热量。则下列热化学方程式书写正确的是A. |
B.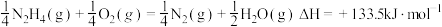 |
C.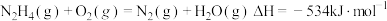 |
D. |
您最近半年使用:0次
名校
8 . “肼合成酶”以其中的 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼
转化为肼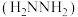 ,其反应历程如下所示。
,其反应历程如下所示。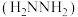 的燃烧热为
的燃烧热为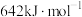 。
。
下列说法正确的是
 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼
转化为肼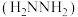 ,其反应历程如下所示。
,其反应历程如下所示。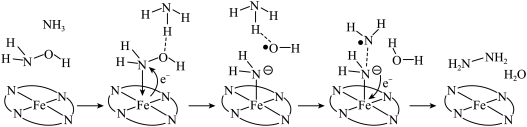
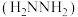 的燃烧热为
的燃烧热为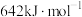 。
。下列说法正确的是
A.反应过程中 元素的化合价发生了变化 元素的化合价发生了变化 |
B.催化中心的 提供孤电子对,N提供空轨道 提供孤电子对,N提供空轨道 |
| C.反应涉及极性键与非极性键的断裂和生成 |
D.肼燃烧热的热化学方程式为: 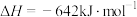 |
您最近半年使用:0次
2024-05-04更新
|
90次组卷
|
2卷引用:广西南宁三中2023-2024学年高二下学期3月阶段性学业测试化学试卷
解题方法
9 . 积极发展清洁能源,推动经济社会绿色低碳转型,已经成为国际社会应对全球气候变化的普遍共识。已知:
①某些常见化学键的键能(指常温常压下,气态分子中 化学键解离成气态原子所吸收的能量)数据如下:
化学键解离成气态原子所吸收的能量)数据如下:
②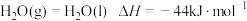 ;
;
③在 和
和 下,
下, 的燃烧热
的燃烧热 。
。
(1)氢能是理想的绿色能源。已知 。
。
①断开1molH—〇需要吸收___________  能量。
能量。
②与天然气相比,氢能的优点是___________ (任写1点)。
(2)CH3OH是一种重要的清洁燃料, 在
在 和
和 下完全燃烧生成
下完全燃烧生成 和
和 时,放出
时,放出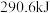 热量。
热量。
①表示 (1)燃烧热的热化学方程式为
(1)燃烧热的热化学方程式为___________ ,该反应中反应物的总键能___________ (填“大于”“小于”或“等于”)生成物的总键能。
②由 催化加氢可制备
催化加氢可制备 ,则
,则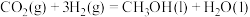

___________  ,若生成气态水,则
,若生成气态水,则
___________ (填“大于”“小于”或“等于”)该计算值。
(3)在 和
和 下,
下, 和
和 的混合气体
的混合气体 完全燃烧生成
完全燃烧生成 和
和 时,放出
时,放出 热量,则该混合气体中
热量,则该混合气体中 的物质的量分数为
的物质的量分数为___________  。
。
①某些常见化学键的键能(指常温常压下,气态分子中
 化学键解离成气态原子所吸收的能量)数据如下:
化学键解离成气态原子所吸收的能量)数据如下:| 化学键 |  |  |
键能 | 436 | 496 |
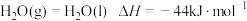 ;
;③在
 和
和 下,
下, 的燃烧热
的燃烧热 。
。(1)氢能是理想的绿色能源。已知
 。
。①断开1molH—〇需要吸收
 能量。
能量。②与天然气相比,氢能的优点是
(2)CH3OH是一种重要的清洁燃料,
 在
在 和
和 下完全燃烧生成
下完全燃烧生成 和
和 时,放出
时,放出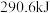 热量。
热量。①表示
 (1)燃烧热的热化学方程式为
(1)燃烧热的热化学方程式为②由
 催化加氢可制备
催化加氢可制备 ,则
,则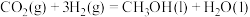

 ,若生成气态水,则
,若生成气态水,则
(3)在
 和
和 下,
下, 和
和 的混合气体
的混合气体 完全燃烧生成
完全燃烧生成 和
和 时,放出
时,放出 热量,则该混合气体中
热量,则该混合气体中 的物质的量分数为
的物质的量分数为 。
。
您最近半年使用:0次
10 . 下列化学反应的表示正确的是
A.尿素和NaClO溶液在碱性条件下反应: |
B.过量氨水和硫酸铜溶液反应: |
C.1-溴丙烷与氢氧化钠水溶液共热: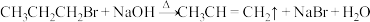 |
D.常温下N2H4为液体,具有很高的燃烧热(622.08 kJ⋅mol-1),肼燃烧的热化学方程式: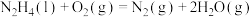 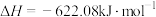 |
您最近半年使用:0次



