名校
解题方法
1 . 根据如下能量关系示意图,下列说法正确的是
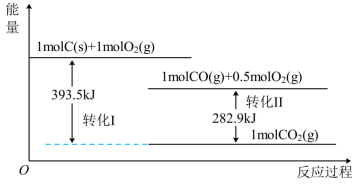
A.1mol 与1mol 与1mol  的能量之和为393.5kJ 的能量之和为393.5kJ |
| B.CO比CO2的能量高 |
C.C的燃烧热的热化学方程式为:C(s)+ O2(g)=CO(g) △H=110.6kJ·mol-1 O2(g)=CO(g) △H=110.6kJ·mol-1 |
D.CO气体燃烧的热化学方程式为: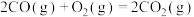  |
您最近一年使用:0次
2024-03-29更新
|
216次组卷
|
2卷引用:浙江省湖州市第二中学2023-2024学年高一下学期3月月考化学试卷
解题方法
2 . 下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
B.由 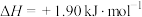 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
C.在101 kPa时,2 g  完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气摩尔燃烧焓的热化学方程式为 完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气摩尔燃烧焓的热化学方程式为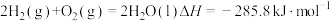 |
D.在稀溶液中, ,若将含0.5 mol ,若将含0.5 mol 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
您最近一年使用:0次
2024-03-26更新
|
152次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
解题方法
3 . 下列反应式正确的是
A.表示 燃烧热的热化学方程式: 燃烧热的热化学方程式:  |
B.碱性锌锰电池的负极反应式: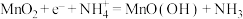 |
C.惰性电极电解NaOH溶液的阳极反应式: |
D. 与 与 溶液反应产生沉淀和气体的离子方程式: 溶液反应产生沉淀和气体的离子方程式: |
您最近一年使用:0次
4 . 已知下列两个热化学方程式:①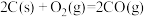
 ,②
,②
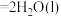
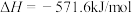 。下列结论正确的是
。下列结论正确的是
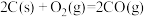
 ,②
,②
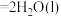
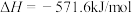 。下列结论正确的是
。下列结论正确的是| A.反应①为吸热反应 |
B.碳的燃烧热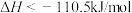 |
C.由②可知氢气的燃烧热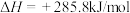 |
D.已知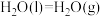 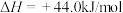 ,则 ,则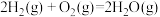  |
您最近一年使用:0次
解题方法
5 . 下列有关热化学方程式的说法正确的是
A.甲烷的标准燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为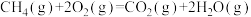  |
B.500℃、30MPa下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为: ,放热19.3kJ,其热化学反应方程式为:  |
C.已知稀溶液中 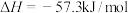 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
D.CO(g)的燃烧热是283.0kJ/mol,则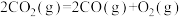 反应的 反应的 |
您最近一年使用:0次
名校
解题方法
6 . 硅是重要的半导体材料,构成现代电子工业的基础。磷及其化合物在工业中应用广泛,在国防和航天工业中亦有许多用途。在工业上,高纯硅可以通过下列流程制取:
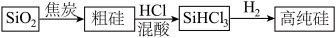
(1)基态硅原子核外电子的运动状态有___________ 种,占据的最高能层符号为___________ 。
(2)流程中由 制粗硅的反应不能说明碳的非金属性强于硅,原因是
制粗硅的反应不能说明碳的非金属性强于硅,原因是___________ 。请写出一个能说明碳的非金属性强于硅的化学方程式___________ 。
(3) 甲硅烷 是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,
是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下, 自燃放出热量
自燃放出热量 ,请写出其燃烧的热化学方程式:
,请写出其燃烧的热化学方程式:___________ 。
(4) 的热稳定性不如
的热稳定性不如 ,其原因是
,其原因是___________ 。
(5)工业上硅铁可以用于冶镁。以煅白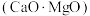 为原料与硅铁(含硅
为原料与硅铁(含硅 的硅铁合金)混合,置于密闭设备中于
的硅铁合金)混合,置于密闭设备中于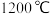 发生反应:
发生反应: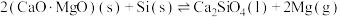 ,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:
,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:___________ 。
(6)有关碳和硅的有关化学键链能如下所示。
硅也有系列氢化物,如甲硅烷等。但硅烷在种类和数量上都远不如烷烃多,原因是___________ 。

(1)基态硅原子核外电子的运动状态有
(2)流程中由
 制粗硅的反应不能说明碳的非金属性强于硅,原因是
制粗硅的反应不能说明碳的非金属性强于硅,原因是(3) 甲硅烷
 是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,
是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下, 自燃放出热量
自燃放出热量 ,请写出其燃烧的热化学方程式:
,请写出其燃烧的热化学方程式:(4)
 的热稳定性不如
的热稳定性不如 ,其原因是
,其原因是(5)工业上硅铁可以用于冶镁。以煅白
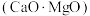 为原料与硅铁(含硅
为原料与硅铁(含硅 的硅铁合金)混合,置于密闭设备中于
的硅铁合金)混合,置于密闭设备中于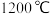 发生反应:
发生反应: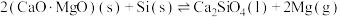 ,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:
,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:(6)有关碳和硅的有关化学键链能如下所示。
| 化学键 |  |  |  |  |  |  |
键能/ | 356 | 413 | 336 | 226 | 318 | 452 |
您最近一年使用:0次
名校
解题方法
7 .  元素可形成多种含氧酸,其中次磷酸
元素可形成多种含氧酸,其中次磷酸 为一元弱酸,
为一元弱酸, 为三元中强酸。雌黄
为三元中强酸。雌黄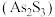 和
和 在盐酸中反应转化为雄黄
在盐酸中反应转化为雄黄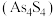 和
和 (沸点
(沸点 并放出
并放出 气体。下列化学反应表示正确的是
气体。下列化学反应表示正确的是
 元素可形成多种含氧酸,其中次磷酸
元素可形成多种含氧酸,其中次磷酸 为一元弱酸,
为一元弱酸, 为三元中强酸。雌黄
为三元中强酸。雌黄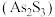 和
和 在盐酸中反应转化为雄黄
在盐酸中反应转化为雄黄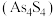 和
和 (沸点
(沸点 并放出
并放出 气体。下列化学反应表示正确的是
气体。下列化学反应表示正确的是A. 制 制 的离子方程式: 的离子方程式: |
B.次磷酸与足量 溶液反应: 溶液反应: |
C.肼燃烧的热化学方程式: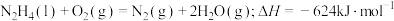 |
D.雌黄制备雄黄的化学方程式: |
您最近一年使用:0次
8 . 研究电解质在水溶液中的平衡能了解它的存在形式。已知部分弱酸的电离常数如下表:
(1)①常温下,pH相同的三种溶液HF、H2CO3、H2S,物质的量浓度最小的是_______ 。
②将少量H2S通入Na2CO3溶液,反应的离子方程式是_______ 。
③0.1mol·L-1的HF溶液,其电离百分数为8%,则该溶液的pH=_______ (已知lg2=0.3)
(2)25℃时,向足量的NaCN溶液中通入少量CO2,所发生反应的离子方程式为_______ 。
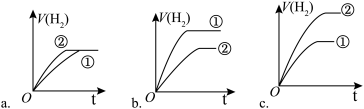
(3)pH相同、体积相同的盐酸和氢氟酸两种溶液盐酸分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示氢氟酸)
(4)烟气中的SO2可引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过程中,溶液中H2SO3、 、
、 三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=
三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=_______ 。

(5)25℃,101KPa时,1g氢气完全燃烧生成液态水,放出142.9kJ热量,请写出氢气燃烧热的热化学方程式_______ (结果取整数)。
| 化学式 | HF | H2CO3 | H2S | HCN |
| 电离平衡常数K(25℃) | 7.2×10-4 | Ka1=4.4×10-7 Ka2=9.1×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-11 | K=4.9×10-10 |
(1)①常温下,pH相同的三种溶液HF、H2CO3、H2S,物质的量浓度最小的是
②将少量H2S通入Na2CO3溶液,反应的离子方程式是
③0.1mol·L-1的HF溶液,其电离百分数为8%,则该溶液的pH=
(2)25℃时,向足量的NaCN溶液中通入少量CO2,所发生反应的离子方程式为
(3)pH相同、体积相同的盐酸和氢氟酸两种溶液盐酸分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

(4)烟气中的SO2可引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过程中,溶液中H2SO3、
 、
、 三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=
三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=
(5)25℃,101KPa时,1g氢气完全燃烧生成液态水,放出142.9kJ热量,请写出氢气燃烧热的热化学方程式
您最近一年使用:0次
解题方法
9 . 下列说法正确的是
A.已知:  ,每进行1mol该反应,有890.3kJ热能转化为化学能 ,每进行1mol该反应,有890.3kJ热能转化为化学能 |
B.若在一定条件下, 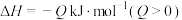 ,则黑磷的稳定性更好 ,则黑磷的稳定性更好 |
C.由 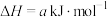 知, 知, 的燃烧热 的燃烧热 |
D.一定条件下,若向某密闭容器中充入1mol  和1 mol 和1 mol  ,充分反应后放出b kJ热量,则 ,充分反应后放出b kJ热量,则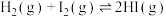 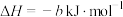 |
您最近一年使用:0次
10 . 2007年10月24日我国自主研发的第一颗月球探测卫星“嫦娥一号”的成功发射“嫦娥一号”三级火箭所用的燃料是高性能、高纯度的液氢燃料和液氧氧化剂,氢气不仅是一种高能燃料,也是一种可再生的绿色能源。
(1)氢气的燃烧热为285.8kJ/mol,写出其燃烧热的热化学方程式:_______ 。
(2)实验测得1mol 与1mol
与1mol 完全反应放出184.6kJ的热量,又知1mol
完全反应放出184.6kJ的热量,又知1mol 分子中化学键断裂时需要吸收436kJ的能量,1mol
分子中化学键断裂时需要吸收436kJ的能量,1mol 分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收
分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收_______ 的能量。
(3) 可转化为甲醇:
可转化为甲醇:
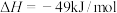

①在一恒温恒容密闭容器中充入1mol 和3mol
和3mol 进行上述反应。测得
进行上述反应。测得 和
和 浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为
浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为_______ ; 的转化率为
的转化率为_______ 。
②拟据下列v-t图象,填写下列空白:

下列时刻所改变的外界条件是
_______ ;
_______ ;
_______ ;反应速率最快的时间段为_______ 。
(1)氢气的燃烧热为285.8kJ/mol,写出其燃烧热的热化学方程式:
(2)实验测得1mol
 与1mol
与1mol 完全反应放出184.6kJ的热量,又知1mol
完全反应放出184.6kJ的热量,又知1mol 分子中化学键断裂时需要吸收436kJ的能量,1mol
分子中化学键断裂时需要吸收436kJ的能量,1mol 分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收
分子中化学键断裂需要吸收243kJ的能量。则1molHCl分子中化学键断裂时需要吸收(3)
 可转化为甲醇:
可转化为甲醇:
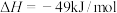

①在一恒温恒容密闭容器中充入1mol
 和3mol
和3mol 进行上述反应。测得
进行上述反应。测得 和
和 浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为
浓度随时间变化如图所示。问答:0~10min内,氢气的平均反应速率为 的转化率为
的转化率为②拟据下列v-t图象,填写下列空白:

下列时刻所改变的外界条件是



您最近一年使用:0次



