名校
解题方法
1 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气器材的消毒,可由乙酸与 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: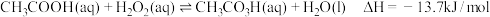
(1)市售过氧乙酸的浓度一般不超过21%,原因是___________ 。
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
(3)取质量相等的冰醋酸和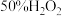 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
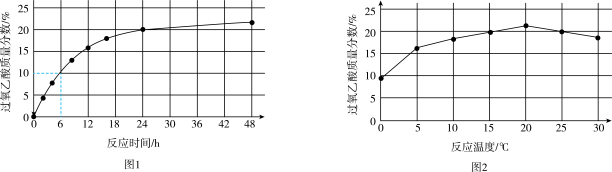
①实验1中,若反应混合液的总质量为 ,依据图1数据计算,在
,依据图1数据计算,在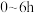 间,
间,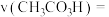
___________ 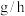 。(用含m的代数式表示)
。(用含m的代数式表示)
②综合图1、图2分析,与 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是___________ (写出2条)。
(4)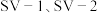 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
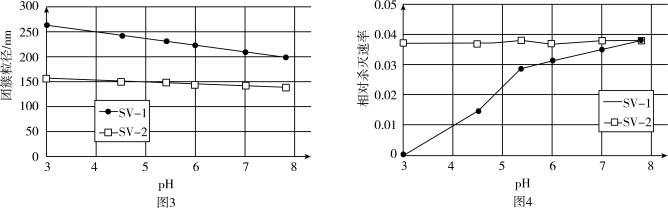
依据图3、图4分析,过氧乙酸对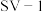 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是___________ 。
 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: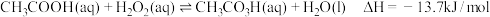
(1)市售过氧乙酸的浓度一般不超过21%,原因是
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
| A.降低温度 | B.增加 用量(溶液体积不变) 用量(溶液体积不变) |
| C.加水稀释溶液 | D.增加乙酸的用量(溶液体积不变) |
(3)取质量相等的冰醋酸和
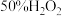 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。实验1:在
 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。

①实验1中,若反应混合液的总质量为
 ,依据图1数据计算,在
,依据图1数据计算,在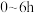 间,
间,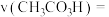
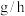 。(用含m的代数式表示)
。(用含m的代数式表示)②综合图1、图2分析,与
 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是(4)
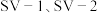 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
依据图3、图4分析,过氧乙酸对
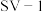 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是
您最近一年使用:0次
名校
2 . 丙酮(  )碘化反应为:
)碘化反应为: +I2
+I2
 +H++I-。兴趣小组在20 ℃时研究了该反应的反应速率。他们在反应开始前加入淀粉溶液,通过观察淀粉溶液褪色时间 t 来度量反应速率的大小。实验数据如下:
+H++I-。兴趣小组在20 ℃时研究了该反应的反应速率。他们在反应开始前加入淀粉溶液,通过观察淀粉溶液褪色时间 t 来度量反应速率的大小。实验数据如下:
下列根据实验数据做出的推理不合理的是
 )碘化反应为:
)碘化反应为: +I2
+I2
 +H++I-。兴趣小组在20 ℃时研究了该反应的反应速率。他们在反应开始前加入淀粉溶液,通过观察淀粉溶液褪色时间 t 来度量反应速率的大小。实验数据如下:
+H++I-。兴趣小组在20 ℃时研究了该反应的反应速率。他们在反应开始前加入淀粉溶液,通过观察淀粉溶液褪色时间 t 来度量反应速率的大小。实验数据如下:| 实验编号 | c(丙酮) / mol·L−1 | c(I2) / mol·L−1 | c(H+) / mol·L−1 | t / s |
| ① | 2 | 0.002 | 0.5 | 40 |
| ② | 1 | 0.002 | 0.5 | 80 |
| ③ | 2 | 0.001 | 0.5 | 40 |
| ④ | 2 | 0.002 | 0.25 | 80 |
| A.实验①中,v(I2)=5×10-5 mol·L−1·s−1 |
| B.由实验①③可知,c(I2)越大,反应速率越快 |
| C.由实验①④可知,c(H+)越大,反应速率越快 |
| D.若c(丙酮)、c(I2)、c(H+)分别为1mol·L−1、0.002 mol·L−1、1mol·L−1,则 t=40 s |
您最近一年使用:0次
名校
3 . 一定温度下,容积为2L的密闭容器中发生反应:A(g)+B(g) C(g)+2D(g) △H>0,容器中部分物质的含量见下表(t2>t1),下列说法正确的是
C(g)+2D(g) △H>0,容器中部分物质的含量见下表(t2>t1),下列说法正确的是
 C(g)+2D(g) △H>0,容器中部分物质的含量见下表(t2>t1),下列说法正确的是
C(g)+2D(g) △H>0,容器中部分物质的含量见下表(t2>t1),下列说法正确的是| 反应时间/min | n(A)/mol | n(B)/mol | n(C)/mol | n(D)/mol |
| 0 | 1.2 | 0.6 | 0 | 0 |
| t1 | 0.8 | |||
| t2 | 0.2 | 0.8 |
| A.升高温度和减小压强都能使此反应的化学平衡常数增大 |
| B.tlmin内,D的平均化学反应速率为v(D)=0.8/t1mol(L·min)-1 |
| C.达到化学平衡状态时,A的转化率为66.7% |
| D.该温度下,反应的化学平衡常数K=0.8 |
您最近一年使用:0次
名校
解题方法
4 . 使反应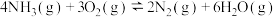 在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.6 mol。此反应的平均速率可表示为
在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.6 mol。此反应的平均速率可表示为
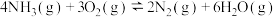 在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.6 mol。此反应的平均速率可表示为
在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.6 mol。此反应的平均速率可表示为A.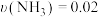 mol(L·s) mol(L·s) | B.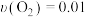 mol/(L·s) mol/(L·s) |
C.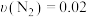 mol/(L·s) mol/(L·s) | D.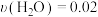 mol/(L·s) mol/(L·s) |
您最近一年使用:0次
名校
解题方法
5 . 在恒容密闭容器中通入X并发生反应:2X(g)=Y(g),T1、T2温度下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是


| A.该反应进行到M点放出的热量大于进行到W点放出的热量 |
| B.T2温度下,在0- t1,时间内,v(Y)=a-b/t1mol·L-1min-1 |
| C.该反应的ΔH<0 |
| D.M点时向容器内充入一定量惰性气体,平衡向正反应方向移动 |
您最近一年使用:0次
2023-12-27更新
|
114次组卷
|
2卷引用:北京市中关村中学2021-2022学年高二上学期期中考试化学试题
名校
6 . 在5L密闭容器中进行反应2SO2(g)+O2(g) 2SO3(g),30秒后,SO3的物质的量增加了0.3mol。下列叙述不正确的是
2SO3(g),30秒后,SO3的物质的量增加了0.3mol。下列叙述不正确的是
 2SO3(g),30秒后,SO3的物质的量增加了0.3mol。下列叙述不正确的是
2SO3(g),30秒后,SO3的物质的量增加了0.3mol。下列叙述不正确的是| A.v(SO3)=0.002 mol·L-1.s-1 |
| B.v(O2)=0.001 mol·L-1.s-1 |
| C.当容器内气体密度不再变化时,反应达到平衡 |
| D.当容器内的SO3的浓度不再增加时,反应达到平衡 |
您最近一年使用:0次
名校
7 . 1 L密闭容器中进行反应: ,2 min内N2的物质的量由2 mol减小到0.8 mol,则用N2的浓度变化表示的化学反应速率[
,2 min内N2的物质的量由2 mol减小到0.8 mol,则用N2的浓度变化表示的化学反应速率[ ]为
]为
 ,2 min内N2的物质的量由2 mol减小到0.8 mol,则用N2的浓度变化表示的化学反应速率[
,2 min内N2的物质的量由2 mol减小到0.8 mol,则用N2的浓度变化表示的化学反应速率[ ]为
]为| A.0.4 | B.1.0 | C.1.2 | D.0.6 |
您最近一年使用:0次
2023-12-18更新
|
95次组卷
|
2卷引用:北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题
名校
解题方法
8 . 一定条件下,在2L密闭容器中发生反应: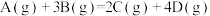 ,测得5min内,A的物质的量减小了10mol,则5min内该反应的化学反应速率是
,测得5min内,A的物质的量减小了10mol,则5min内该反应的化学反应速率是
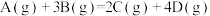 ,测得5min内,A的物质的量减小了10mol,则5min内该反应的化学反应速率是
,测得5min内,A的物质的量减小了10mol,则5min内该反应的化学反应速率是A.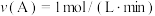 | B.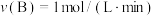 |
C.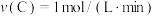 | D.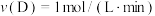 |
您最近一年使用:0次
9 . 在2L的密闭容器中通入 和
和 ,使其发生反应
,使其发生反应 。在10s内用
。在10s内用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为 ,则这10s内消耗的
,则这10s内消耗的 的物质的量是
的物质的量是
 和
和 ,使其发生反应
,使其发生反应 。在10s内用
。在10s内用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为 ,则这10s内消耗的
,则这10s内消耗的 的物质的量是
的物质的量是| A.0.8mol | B.0.4mol | C.0.2mol | D.1.6mol |
您最近一年使用:0次
名校
解题方法
10 . 在 反应中,表示该反应速率最快的是
反应中,表示该反应速率最快的是
 反应中,表示该反应速率最快的是
反应中,表示该反应速率最快的是A.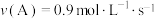 | B. |
C. | D. |
您最近一年使用:0次



