2024·广东深圳·二模
1 . 一定温度下,向恒容密闭容器中投入E和M发生如下反应:E(g)+M(g) F(g)
F(g) G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是
G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是
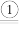 F(g)
F(g) G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是
G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是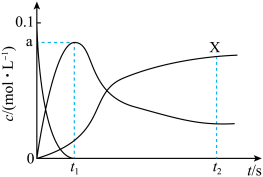
A.X为c(F)随 的变化曲线 的变化曲线 | B.0~t1内,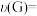 = = mol•L-1•s-1 mol•L-1•s-1 |
| C.反应的活化能:①>② | D.t2时,扩大容器的体积,n(F)减小 |
您最近一年使用:0次
名校
解题方法
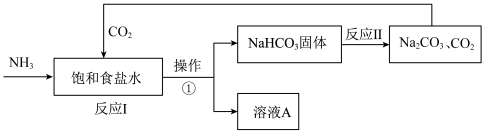
2 . 侯氏制碱法是我国化学工程专家侯德榜将氨碱法和合成氨法两种工艺联合起来生产纯碱的方法。主要过程如图所示(部分物质已略去):
(1)纯碱的化学式为___________ (填“ ”或“
”或“ ”);
”);
(2)操作①的名称是___________ (填“蒸发”或“过滤”);
(3)上述实验过程中可以循环使用的物质是___________ (填化学式);
(4)工业上可以用氨生产尿素,其方程式为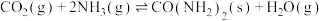 ,一定温度下,将1 mol
,一定温度下,将1 mol  和2 mol
和2 mol  充入体积为1L的密闭容器中,5 min后测得
充入体积为1L的密闭容器中,5 min后测得 的物质的量为0.6 mol,则:
的物质的量为0.6 mol,则:
①对上述反应,若适当升高温度,化学反应速率会___________ (填“增大”或“减小”);
②用 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为___________ mol/(L·min)。
(1)纯碱的化学式为
 ”或“
”或“ ”);
”);(2)操作①的名称是
(3)上述实验过程中可以循环使用的物质是
(4)工业上可以用氨生产尿素,其方程式为
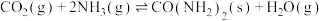 ,一定温度下,将1 mol
,一定温度下,将1 mol  和2 mol
和2 mol  充入体积为1L的密闭容器中,5 min后测得
充入体积为1L的密闭容器中,5 min后测得 的物质的量为0.6 mol,则:
的物质的量为0.6 mol,则:①对上述反应,若适当升高温度,化学反应速率会
②用
 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为
您最近一年使用:0次
7日内更新
|
141次组卷
|
2卷引用:江苏省南京师范大学附属中学2024届高三下学期5月模拟化学试题
3 . 请根据有关知识,填写下列空白:
(1)拆开1molH-H键,1molN-H键,1molN N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3
N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3___________ 热量(填“吸收”或“放出”)___________ kJ;事实上,反应的热量总小于理论值,理由是___________ 。
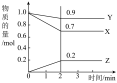
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:___________ 。
②从开始到10s用Z表示该反应的速率为___________ 。
③下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.X、Y、Z的反应速率之比为1:1:2
B.在混合气体中X的体积分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的压强不随时间的变化而变化
④为加快该反应的反应速率,可采取的措施是___________ 。
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
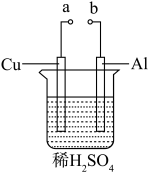
(3)某兴趣小组为研究原电池原理,设计如图装置。___________ ,Al极发生___________ 填(“氧化”或“还原”)反应,溶液pH___________ (填“增大”、“减小”或“不变”)。当负极金属溶解5.4g时,通过导线的电子物质的量___________ 。
(1)拆开1molH-H键,1molN-H键,1molN
 N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3
N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

②从开始到10s用Z表示该反应的速率为
③下列叙述中能说明上述反应达到平衡状态的是
A.X、Y、Z的反应速率之比为1:1:2
B.在混合气体中X的体积分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的压强不随时间的变化而变化
④为加快该反应的反应速率,可采取的措施是
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
(3)某兴趣小组为研究原电池原理,设计如图装置。
您最近一年使用:0次
名校
4 . 某温度下,在1L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示。由图中数据分析:____________ 。反应开始至2min,Z的平均反应速率为:______________ 。
您最近一年使用:0次
名校
解题方法
5 . 对于反应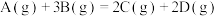 ,下列表示中反应速率最大的是
,下列表示中反应速率最大的是
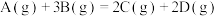 ,下列表示中反应速率最大的是
,下列表示中反应速率最大的是A.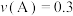 mol⋅L mol⋅L ⋅s ⋅s | B.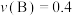 mol⋅L mol⋅L ⋅s ⋅s |
C. mol⋅L mol⋅L ⋅s ⋅s | D.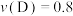 mol⋅L mol⋅L ⋅min ⋅min |
您最近一年使用:0次
2024-04-27更新
|
317次组卷
|
6卷引用:江苏省扬州中学2022-2023学年高一下学期3月月考化学试题
江苏省扬州中学2022-2023学年高一下学期3月月考化学试题江苏省盐城市大丰高级中学2023-2024学年高一下学期(普通班强化班)第一次阶段性考试化学试卷 江苏省盐城市五校联考2023-2024学年高一下学期3月月考化学试题(已下线)第05讲 化学反应的速率与限度-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)(已下线)6.2.1化学反应的速率课后作业提高篇(已下线)专题06 化学反应的速率与限度(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
6 . 在2L恒容密闭容器中,充入0.6molX气体和0.4molY气体,发生如下反应: ,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为
,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为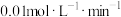 ,则:上述反应的化学方程式中Z的化学计量数n的值是
,则:上述反应的化学方程式中Z的化学计量数n的值是
 ,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为
,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为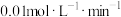 ,则:上述反应的化学方程式中Z的化学计量数n的值是
,则:上述反应的化学方程式中Z的化学计量数n的值是| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
名校
解题方法
7 . 在2L密闭容器中,800℃时,反应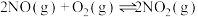 体系中,
体系中, 随时间的变化如下表所示。
随时间的变化如下表所示。
(1)图中,A点处
______  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。 变化的曲线是
变化的曲线是______ ,用 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
______ 。
(3)下列能使该反应的反应速率增大的是______ 。
a.及时分离出 气体 b.适当升高温度
气体 b.适当升高温度
c.增大 的浓度 d.选择高效的催化剂
的浓度 d.选择高效的催化剂
(4)下列能说明该反应已经达到平衡状态的是______ (填字母,下同)。
a. b.容器内压强保持不变
b.容器内压强保持不变
c. d.容器内的密度保持不变
d.容器内的密度保持不变
e.气体的总质量保持不变 f. 和
和 的物质的量之比为
的物质的量之比为
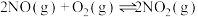 体系中,
体系中, 随时间的变化如下表所示。
随时间的变化如下表所示。| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)图中,A点处

 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
 变化的曲线是
变化的曲线是 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
(3)下列能使该反应的反应速率增大的是
a.及时分离出
 气体 b.适当升高温度
气体 b.适当升高温度c.增大
 的浓度 d.选择高效的催化剂
的浓度 d.选择高效的催化剂(4)下列能说明该反应已经达到平衡状态的是
a.
 b.容器内压强保持不变
b.容器内压强保持不变c.
 d.容器内的密度保持不变
d.容器内的密度保持不变e.气体的总质量保持不变 f.
 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
8 . 在2L恒容密闭容器中,充入0.6molX气体和0.4molY气体,发生如下反应: ,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为
,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为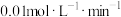 ,则:上述反应在5min末时,已消耗掉Y的物质的量分数是
,则:上述反应在5min末时,已消耗掉Y的物质的量分数是
 ,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为
,5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为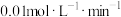 ,则:上述反应在5min末时,已消耗掉Y的物质的量分数是
,则:上述反应在5min末时,已消耗掉Y的物质的量分数是| A.20% | B.25% | C.33% | D.50% |
您最近一年使用:0次
解题方法
9 . 向一个固定体积的密闭容器充入2molA和1molB,发生如下反应:2A(g)+B(g) 3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。
3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。
(1)用A表示2分钟内平均反应速率为_______ 。
(2)容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为_______ (填“吸热”或“放热”)反应。
(3)增大B的转化率,可采取的措施是_______ (用序号填空)
① 加入A ② 升高温度 ③ 加压 ④ 再加入1.6molA+0.8molB ⑤ 将C分离出容器
(4)若在一体积可变的容器中,该反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如下图,a点改变的条件可能是_______ ;若升高温度时,请将反应速率变化情况画在c-d处_______ 。

 3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。
3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。(1)用A表示2分钟内平均反应速率为
(2)容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为
(3)增大B的转化率,可采取的措施是
① 加入A ② 升高温度 ③ 加压 ④ 再加入1.6molA+0.8molB ⑤ 将C分离出容器
(4)若在一体积可变的容器中,该反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如下图,a点改变的条件可能是

您最近一年使用:0次
10 . 已知: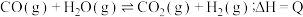 ,其平衡常数随温度变化如下表所示。
,其平衡常数随温度变化如下表所示。
(1)上述反应的化学平衡常数表达式为
___________ 。
(2) 时,向体积为
时,向体积为 反应器中通入一定量的
反应器中通入一定量的 和
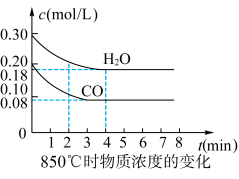
和 ,发生上述反应,
,发生上述反应, 和
和 浓度变化如图所示,则
浓度变化如图所示,则 时,平均反应速率
时,平均反应速率
___________ 。
(3)若在 时进行,且
时进行,且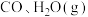 的起始浓度均为
的起始浓度均为 ,该条件下,
,该条件下, 的最大转化率为
的最大转化率为___________
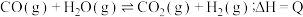 ,其平衡常数随温度变化如下表所示。
,其平衡常数随温度变化如下表所示。温度 | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为

(2)
 时,向体积为
时,向体积为 反应器中通入一定量的
反应器中通入一定量的 和
和 ,发生上述反应,
,发生上述反应, 和
和 浓度变化如图所示,则
浓度变化如图所示,则 时,平均反应速率
时,平均反应速率

(3)若在
 时进行,且
时进行,且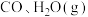 的起始浓度均为
的起始浓度均为 ,该条件下,
,该条件下, 的最大转化率为
的最大转化率为
您最近一年使用:0次



