解题方法
1 . 一定温度下,在 的密闭容器中,
的密闭容器中, 两种气体的物质的量随时间变化的曲线如图所示:
两种气体的物质的量随时间变化的曲线如图所示:_______ 。
(2)反应达到最大限度的时间是______  ,该时间内的平均反应速率
,该时间内的平均反应速率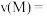
______ 。
(3)判断该反应达到平衡状态的依据是_______。
(4)能加快反应速率的措施是_______。
(5)反应进行到4min时,N的转化率为_______ 。
 的密闭容器中,
的密闭容器中, 两种气体的物质的量随时间变化的曲线如图所示:
两种气体的物质的量随时间变化的曲线如图所示: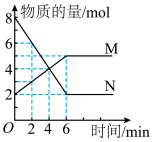
(2)反应达到最大限度的时间是
 ,该时间内的平均反应速率
,该时间内的平均反应速率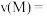
(3)判断该反应达到平衡状态的依据是_______。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
D.该条件下,单位时间内消耗 的同时,消耗 的同时,消耗 |
(4)能加快反应速率的措施是_______。
| A.升高温度 |
B.容器容积不变,充入惰性气体 |
C.容器压强不变,充入惰性气体 |
| D.使用催化剂 |
(5)反应进行到4min时,N的转化率为
您最近一年使用:0次
2 . 请根据有关知识,填写下列空白:
(1)拆开1molH-H键,1molN-H键,1molN N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3
N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3___________ 热量(填“吸收”或“放出”)___________ kJ;事实上,反应的热量总小于理论值,理由是___________ 。
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:___________ 。
②从开始到10s用Z表示该反应的速率为___________ 。
③下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.X、Y、Z的反应速率之比为1:1:2
B.在混合气体中X的体积分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的压强不随时间的变化而变化
④为加快该反应的反应速率,可采取的措施是___________ 。
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
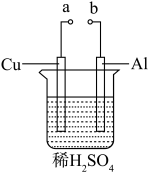
(3)某兴趣小组为研究原电池原理,设计如图装置。___________ ,Al极发生___________ 填(“氧化”或“还原”)反应,溶液pH___________ (填“增大”、“减小”或“不变”)。当负极金属溶解5.4g时,通过导线的电子物质的量___________ 。
(1)拆开1molH-H键,1molN-H键,1molN
 N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3
N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

②从开始到10s用Z表示该反应的速率为
③下列叙述中能说明上述反应达到平衡状态的是
A.X、Y、Z的反应速率之比为1:1:2
B.在混合气体中X的体积分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的压强不随时间的变化而变化
④为加快该反应的反应速率,可采取的措施是
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
(3)某兴趣小组为研究原电池原理,设计如图装置。
您最近一年使用:0次
名校
3 . 一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质量的变化如图所示。下列推断合理的是
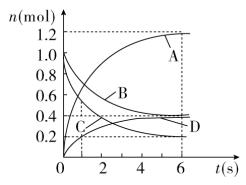
A.该反应的化学方程式为: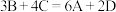 |
B.反应进行到1s时, |
| C.反应进行到6s时,B的平均反应速率为0.05 mol/(L·s) |
| D.反应进行到6s时,各物质的反应速率相等 |
您最近一年使用:0次
解题方法
4 . NH3(含6个H-N)是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
注:拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能
可逆反应N2(g)+3H2(g) 2NH(g) ∆H=
2NH(g) ∆H=___________ kJ•mol-1。
(2)在一定条件下,体积固定的体系中,建立如图所示的N2+3H2 2NH3平衡体系。
2NH3平衡体系。___________ (填“曲线A”、“曲线B”或“曲线C”)。
②0~tomin时,用H2表示化学反应速率是___________ mol•L•min-1。
③下列能说明该反应达到平衡的是___________ 。
A.混合气体的压强不再变化 B.c(H2)=c(NH3)
C.混合气体的质量不再变化 D.NH3的体积分数不再变化
(3)潜艇的液氨-液氧燃料电池示意图如图所示:___________ ,其中电极b是该电池的___________ 。
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
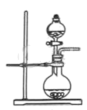
(4)火箭燃料N2H4具有强还原性,可用氨水与NaClO溶液反应制取,反应装置如图所示,其中分液漏斗中溶液是___________ 。
(1)已知:
| 共价键 | H-H | N≡N | N-H |
| 键能/kJ•mol-1 | 436 | 946 | 391 |
可逆反应N2(g)+3H2(g)
 2NH(g) ∆H=
2NH(g) ∆H=(2)在一定条件下,体积固定的体系中,建立如图所示的N2+3H2
 2NH3平衡体系。
2NH3平衡体系。
②0~tomin时,用H2表示化学反应速率是
③下列能说明该反应达到平衡的是
A.混合气体的压强不再变化 B.c(H2)=c(NH3)
C.混合气体的质量不再变化 D.NH3的体积分数不再变化
(3)潜艇的液氨-液氧燃料电池示意图如图所示:

②电解质溶液中OH-离子向
(4)火箭燃料N2H4具有强还原性,可用氨水与NaClO溶液反应制取,反应装置如图所示,其中分液漏斗中溶液是
您最近一年使用:0次
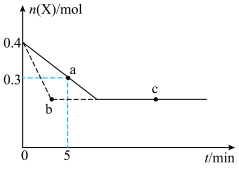
5 . 在恒温2L密闭容器中通入气体X并发生反应:2X(g) Y(g) ∆H<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
Y(g) ∆H<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
 Y(g) ∆H<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
Y(g) ∆H<0,X的物质的量n(x)随时间t变化的曲线如图所示(图中的两曲线分别代表有无催化剂的情形),下列叙述正确的是
| A.虚线表示未使用催化剂的情形 |
| B.b、c两点表明反应在相应条件下达到了最大限度 |
| C.反应进行到a点时放出的热量大于反应进行到b点时放出的热量 |
| D.反应从开始到a点的平均反应速率可表示为v(Y)=0.01mol/(L•min) |
您最近一年使用:0次
6 . 往1L的恒容绝热容器中充入1.5mol气体N,容器内各成分的物质的量随时间变化的曲线如图。已知反应物和生成物均为气体。下列说法正确的是
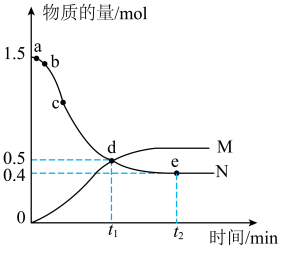
| A.ab段平均反应速率大于bc段平均反应速率 |
| B.d点时,反应达到平衡状态 |
C.总反应方程式为 |
| D.反应达到平衡时,M的体积分数约为58% |
您最近一年使用:0次
名校
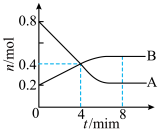
7 . 某温度时,在2L容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。___________ 。
(2)反应开始至4min,A的平均反应速率为___________ ;8 min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(3)4 min时,反应是否达到化学平衡?___________ (填“是”或“否”)
(2)反应开始至4min,A的平均反应速率为
(3)4 min时,反应是否达到化学平衡?
您最近一年使用:0次
8 . 一定温度下,在1L恒容密闭容器中投入2mol氨基甲酸铵( ),发生反应
),发生反应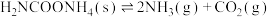 ,实验测得数据如下表所示。下列说法错误
,实验测得数据如下表所示。下列说法错误
 ),发生反应
),发生反应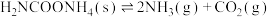 ,实验测得数据如下表所示。下列说法错误
,实验测得数据如下表所示。下列说法错误时间段/min |
|
0-1 | 0.8 |
0-2 | 0.6 |
0-3 | 0.4 |
A.2min时,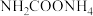 的转化率为30% 的转化率为30% |
B.2min时,体系中存在 |
C.30s时, 的浓度大于0.4 的浓度大于0.4 |
| D.混合气体的密度不变时,说明此反应达到了平衡状态 |
您最近一年使用:0次
解题方法
9 . 在体积为2L的绝热、恒容密闭容器中投入2mol  和1mol
和1mol  ,发生反应:
,发生反应:
 如图所示是部分反应物和生成物随时间的变化曲线。下列说法正确的是
如图所示是部分反应物和生成物随时间的变化曲线。下列说法正确的是
 和1mol
和1mol  ,发生反应:
,发生反应:
 如图所示是部分反应物和生成物随时间的变化曲线。下列说法正确的是
如图所示是部分反应物和生成物随时间的变化曲线。下列说法正确的是
| A.A.10min时,正反应速率等于逆反应速率 |
B.反应开始至10min, 的平均反应速率为 的平均反应速率为 |
C.使用催化剂增大反应速率,可实现 的完全转化 的完全转化 |
| D.某时刻,体系的温度不再发生变化说明该反应达到化学平衡状态 |
您最近一年使用:0次
10 . 化学工业为世界能源消费生产了多种能源物质。
(1)在常温常压下,H2和C3H8的混合气体共3mol完全燃烧生成CO2和液态水放出2792kJ的热量。
已知: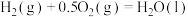
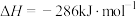
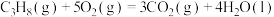
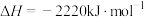
则该混合气体中,H2和C3H8的体积比为___________ 。
(2)一种利用太阳能将甲烷重整制氢原理的示意图如下:___________ 。
②NiO·Fe2O3在整个反应过程中的作用是___________ 。
③反应每消耗1molCH4,理论上可生成标准状况下H2的体积为___________ 。
(3)在催化剂光照条件下,CO2和H2O可转化为CH3OH,该反应的化学方程式为: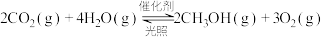 。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得
。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得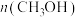 随时间的变化如下表所示:
随时间的变化如下表所示:
①用H2O(g)表示0~3min内该反应的平均反应速率为___________ 。
②第4分钟时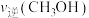
___________ (填“大于”“小于”或“等于”)第3分钟时 。
。
③能说明该反应已达到平衡状态的是___________ 。
A. B.
B.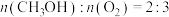
C.容器内密度保持不变 D.容器内压强保持不变
④上述反应达到平衡时二氧化碳的转化率为___________ 。
(1)在常温常压下,H2和C3H8的混合气体共3mol完全燃烧生成CO2和液态水放出2792kJ的热量。
已知:
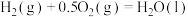
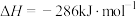
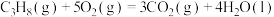
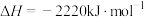
则该混合气体中,H2和C3H8的体积比为
(2)一种利用太阳能将甲烷重整制氢原理的示意图如下:
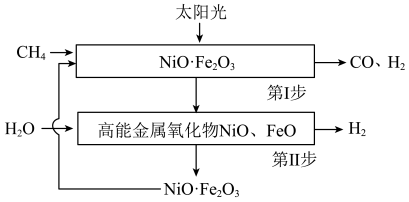
②NiO·Fe2O3在整个反应过程中的作用是
③反应每消耗1molCH4,理论上可生成标准状况下H2的体积为
(3)在催化剂光照条件下,CO2和H2O可转化为CH3OH,该反应的化学方程式为:
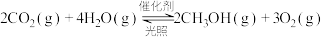 。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得
。一定条件下,在2L恒容密闭容器中充入0.50molCO2和1.00mol水蒸气进行上述反应,测得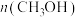 随时间的变化如下表所示:
随时间的变化如下表所示:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
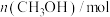 | 0.00 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
②第4分钟时
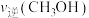
 。
。③能说明该反应已达到平衡状态的是
A.
 B.
B.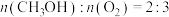
C.容器内密度保持不变 D.容器内压强保持不变
④上述反应达到平衡时二氧化碳的转化率为
您最近一年使用:0次