1 . 已知双环戊二烯解聚成环戊二烯的反应为
 。若将3 mol双环戊二烯通入2L恒容密闭容器中,测得
。若将3 mol双环戊二烯通入2L恒容密闭容器中,测得 ℃和
℃和 ℃下n(双环戊二烯或环戊二烯)随时间的变化如图所示,
℃下n(双环戊二烯或环戊二烯)随时间的变化如图所示, ℃时反应到a点恰好达到平衡。下列有关说法错误的是
℃时反应到a点恰好达到平衡。下列有关说法错误的是

| A. T1>T2 |
B. ℃时,0~2h内的平均反应速率:v(环戊二烯) ℃时,0~2h内的平均反应速率:v(环戊二烯)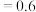 mol⋅L mol⋅L ⋅h ⋅h |
C. ℃时,当容器内的气体压强为起始的1.5倍时:v(正) ℃时,当容器内的气体压强为起始的1.5倍时:v(正)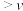 (逆) (逆) |
D. ℃时,反应恰好达到平衡时:44.8 mol ℃时,反应恰好达到平衡时:44.8 mol (环戊二烯) (环戊二烯)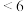 mol mol |
您最近一年使用:0次
名校
2 . 在1373K、100kPa反应条件下,H2S可以发生热解反应: △H>0。对于
△H>0。对于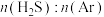 分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是
分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是
 △H>0。对于
△H>0。对于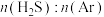 分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是
分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示。下列说法错误的是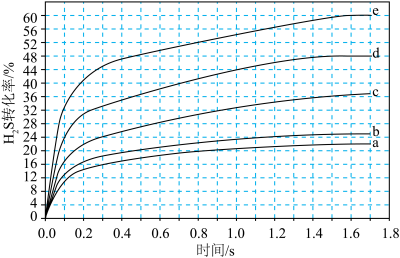
| A.H2S热分解反应的正反应活化能大于逆反应活化能 |
B.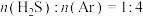 时,在0~0.9s之间,H2S分压的平均变化率为35.6 时,在0~0.9s之间,H2S分压的平均变化率为35.6 |
| C.生成a mol S2,同时形成4a mol H-S键,说明反应已达平衡 |
| D.等温等压下加入惰性气体越多,H2S平衡转化率会提高 |
您最近一年使用:0次
3 . 利用天然气制乙炔,反应原理如下:
①

②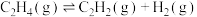

在1L恒容密闭反应器中充入适量的 ,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
①


②
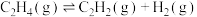

在1L恒容密闭反应器中充入适量的
 ,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
| A.M点正反应速率小于逆反应速率 | B.反应前30min以乙烯生成为主 |
| C.若60min后升温,乙曲线上移,甲曲线下移 | D.0~40min内 平均速率为2. 平均速率为2.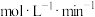 |
您最近一年使用:0次
4 . SiHCl3被应用于制造多晶硅及硅烷偶联剂等领域。50℃时将nmolSiHCl3置于密闭容器中发生如下反应: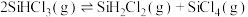 ,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
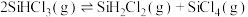 ,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是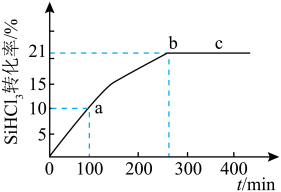
| A.SiH2Cl2和SiCl4均为由极性键构成的非极性分子 |
B.0~100min内,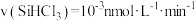 |
C.50℃时该反应的平衡常数 |
| D.b-c段平均速率大于a-b段平均速率 |
您最近一年使用:0次
5 . 一定温度下,向2.0 L恒容密闭容器中充入一定量的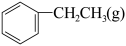 ,在催化剂作用下发生脱氢反应:
,在催化剂作用下发生脱氢反应: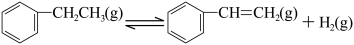
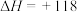 kJ·mol
kJ·mol ,测得乙苯脱氢反应时间与容器中气体总压强的关系如图所示:
,测得乙苯脱氢反应时间与容器中气体总压强的关系如图所示:

| A.乙苯脱氢反应在相对较高温度下能自发进行 |
B.0~4h内平均反应速率可用压强变化表示为v( ) )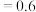 kPa⋅h kPa⋅h |
| C.若向平衡体系中再通入适量的乙苯气体,平衡正向移动 |
| D.若在平衡时扩大容器的容积使体系压强恢复至起始压强,再次达到平衡时乙苯的体积分数减小 |
您最近一年使用:0次
6 . 某温度下,在1 L恒容密闭容器中3.0 mol A发生反应 ,有关数据如下:
,有关数据如下:
下列说法错误的是
 ,有关数据如下:
,有关数据如下:| 时间段/min | 产物C的平均生成速率/mol·L-1·min-1 |
| 0~2 | 0.20 |
| 0~4 | 0.15 |
| 0~6 | 0.10 |
| A.当容器内压强不再变化时,反应达到平衡状态 |
| B.2 min时,加入0.2 mol C,此时平衡逆向移动 |
| C.该温度下的平衡常数K=0.108 |
| D.5 min时,A的物质的量为2.1 mol |
您最近一年使用:0次
解题方法
7 . 在恒温恒容密闭容器中充入一定量W(g),发生如下反应:反应②和③的速率方程分别为 和
和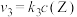 ,其中
,其中 、
、 分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
下列说法正确的是
 和
和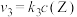 ,其中
,其中 、
、 分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
 | 0 | 1 | 2 | 3 | 4 | 5 | …… |
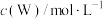 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 | …… |
A.0~4min内, |
| B.若增大容器容积,平衡时W的转化率增大 |
C.若 ,平衡时 ,平衡时 |
| D.达到平衡后,再充入一定量的W(g),混合气体的平均摩尔质量增大 |
您最近一年使用:0次
8 . 一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应A(g)+B(g) 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
 2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是
2C(g)+D(s),t1时达到平衡,在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示,下列说法正确的是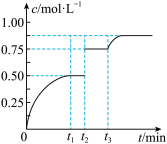
| A.若t1=2min,则v(D)=0.125mol/(L·min) |
| B.t2时刻改变的条件是增加等物质的量的A和B |
| C.t1时刻后向体系中再充入A、B、C各1mol,则v正>v逆 |
| D.若t3时刻改变的条件是升温,则该反应是放热反应 |
您最近一年使用:0次
解题方法
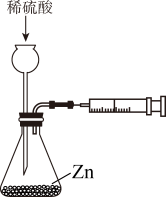
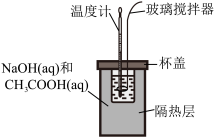
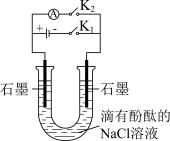
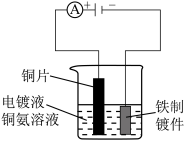
9 . 使用下列装置进行实验,能达到实验目的的是
| A | B | C | D |
| |
|
|
| 测定化学反应速率 | 测定中和反应反应热 | 制作简单氢氧燃料电池 | 在铁质镀件表面镀铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 汽车尾气的排放会对环境造成污染。利用高效催化剂处理汽车尾气中的NO与CO的反应为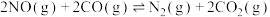
 。一定温度下,在1L恒容密闭容器中加入1mol CO和1mol NO发生上述反应,部分物质的体积分数(
。一定温度下,在1L恒容密闭容器中加入1mol CO和1mol NO发生上述反应,部分物质的体积分数( )随时间(t)的变化如图所示。下列说法正确的是
)随时间(t)的变化如图所示。下列说法正确的是
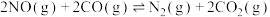
 。一定温度下,在1L恒容密闭容器中加入1mol CO和1mol NO发生上述反应,部分物质的体积分数(
。一定温度下,在1L恒容密闭容器中加入1mol CO和1mol NO发生上述反应,部分物质的体积分数( )随时间(t)的变化如图所示。下列说法正确的是
)随时间(t)的变化如图所示。下列说法正确的是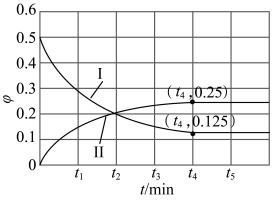
A.曲线Ⅱ表示的是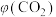 随时间的变化 随时间的变化 |
B. min时,反应达到化学平衡状态 min时,反应达到化学平衡状态 |
| C.增大压强,该平衡右移,平衡常数增大 |
D.0~t4时间段内的平均反应速率为: |
您最近一年使用:0次