1 . 用 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:
(1)利用 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为_____ 。
写出 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:_____ 。
(3)一定条件下,向某恒容密闭容器中充入2
 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。_____ 。
② K时,该反应的平衡常数
K时,该反应的平衡常数
_____ (列出计算式即可,不必化简。以分压代替浓度,分压=总压×物质的量分数)。
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:
该反应速率的通式为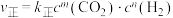 ,
,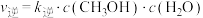 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
_____ 、
_____ 。实验发现,当实验1中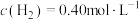 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的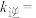
_____ 。
 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:(1)利用
 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为
| 共价键 |  |  |  |  |  |
键能/( ) ) | 464 | 358 | 799 | 432 | 411 |
 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:(3)一定条件下,向某恒容密闭容器中充入2

 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。
②
 K时,该反应的平衡常数
K时,该反应的平衡常数
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入
 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:| 实验 | 起始浓度/( ) ) | 初始速率/( ) ) | |
 |  | ||
| 1 | 0.25 | 1.00 | 0.45 |
| 2 | 0.25 | 2.00 | 3.60 |
| 3 | 2.00 | 1.00 | 3.6 |
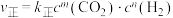 ,
,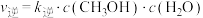 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中

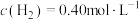 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的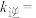
您最近半年使用:0次
解题方法
2 . 反应 ,经 2 min 后,B 的浓度减少了 0.6 mol·L-1。对此反应速率的正确表示是
,经 2 min 后,B 的浓度减少了 0.6 mol·L-1。对此反应速率的正确表示是
 ,经 2 min 后,B 的浓度减少了 0.6 mol·L-1。对此反应速率的正确表示是
,经 2 min 后,B 的浓度减少了 0.6 mol·L-1。对此反应速率的正确表示是| A.用 A 表示的反应速率是 0.4 mol·L-1·min-1 |
| B.在 2 min 末时的反应速率,用反应物 B 来表示是 0.3 mol·L-1·min-1 |
| C.分别用 B、C、D 表示反应的速率,其比值是 3∶2∶1 |
| D.在这 2 min 内用 B 和 C 表示的反应速率的值都是相同的 |
您最近半年使用:0次
解题方法
3 . 在2L密闭容器中发生铝与稀硫酸的反应,已知5 s末硫酸的物质的量消耗了0.6 mol,若不考虑反应过程中溶液体积的变化,则5 s内生成硫酸铝的平均反应速率是
| A.1.2 mol/(L·min) | B.1.8 mol/(L·min) | C.0.06 mol/(L·s) | D.0.04 mol/(L·s) |
您最近半年使用:0次
名校
解题方法
4 . 某研究团队以NO和H2为原料,在Fe基催化下有效地合成NH3.回答下列问题:
已知:①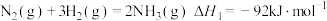
②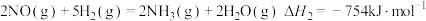
(1)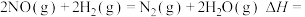
___________  。
。
(2)在一定温度下,向一恒容密闭容器中充入0.2molNO(g)和0.5molH2(g),只发生反应②,达到平衡时生成1.7gNH3(g)。下列叙述正确的是___________ (填标号)。
A.当容器内总压强不变时,该反应达到平衡
B.达到平衡时,反应体系放出的热量为37.7kJ
C.平衡后再充入0.2molNO(g)和0.5molH2(g),NO平衡转化率减小
(3)研究发现, 分两步进行:
分两步进行:
第1步: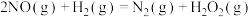 (慢反应);
(慢反应);
第2步:___________ (补充)(快反应)。
加入催化剂,主要是降低第___________ (填“1”或“2”)步反应活化能。
(4) 的反应速率方程式为
的反应速率方程式为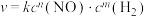 (其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
(其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
根据上述数据计算:m=___________ ,n=___________ ,c=___________ 。
(5)在一密闭反应器中充入2molNO(g)和5molH2(g),在催化剂10Fe﹣8Cu/TiO2作用下发生反应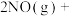
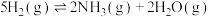 ,
, ,实验测得NO转化率和NH3选择性与温度的关系如图所示。
,实验测得NO转化率和NH3选择性与温度的关系如图所示。

温度高于350℃时,NO转化率增大,但NH3选择性降低,主要原因是___________ 。a点时生成NH3的物质的量为___________ (结果保留3位有效数字)。
(6)某温度下,保持总压强为100kPa,向反应器中充入2molNO(g)和6molH2(g),只发生反应:(a)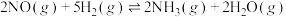 ,(b)
,(b) ,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
___________  (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
已知:①
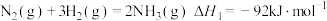
②
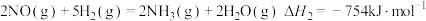
(1)
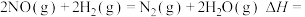
 。
。(2)在一定温度下,向一恒容密闭容器中充入0.2molNO(g)和0.5molH2(g),只发生反应②,达到平衡时生成1.7gNH3(g)。下列叙述正确的是
A.当容器内总压强不变时,该反应达到平衡
B.达到平衡时,反应体系放出的热量为37.7kJ
C.平衡后再充入0.2molNO(g)和0.5molH2(g),NO平衡转化率减小
(3)研究发现,
 分两步进行:
分两步进行:第1步:
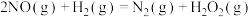 (慢反应);
(慢反应);第2步:
加入催化剂,主要是降低第
(4)
 的反应速率方程式为
的反应速率方程式为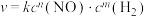 (其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
(其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:| 序号 | 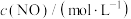 | 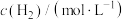 | 速率 |
| I | 0.1 | 0.1 | v |
| II | 0.2 | 0.1 | 4v |
| III | 0.2 | 0.2 | 8v |
| IV | c | 0.4 | 36v |
(5)在一密闭反应器中充入2molNO(g)和5molH2(g),在催化剂10Fe﹣8Cu/TiO2作用下发生反应
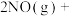
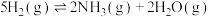 ,
, ,实验测得NO转化率和NH3选择性与温度的关系如图所示。
,实验测得NO转化率和NH3选择性与温度的关系如图所示。
温度高于350℃时,NO转化率增大,但NH3选择性降低,主要原因是
(6)某温度下,保持总压强为100kPa,向反应器中充入2molNO(g)和6molH2(g),只发生反应:(a)
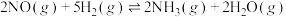 ,(b)
,(b) ,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
 (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
您最近半年使用:0次
2024-01-19更新
|
154次组卷
|
3卷引用:2024届青海省协作联考高三上学期一模理综试题
名校
5 . 在某一化学反应中,生成物 的浓度在
的浓度在 内从
内从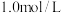 变成
变成 ,则
,则 内用生成物
内用生成物 表示的化学反应速率是
表示的化学反应速率是
 的浓度在
的浓度在 内从
内从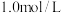 变成
变成 ,则
,则 内用生成物
内用生成物 表示的化学反应速率是
表示的化学反应速率是A.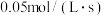 | B.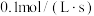 |
C.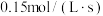 | D.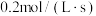 |
您最近半年使用:0次
2023-08-07更新
|
55次组卷
|
2卷引用: 青海省西宁市2022-2023学年高一下学期期末考试化学试题
名校
解题方法
6 . 在300℃时,将6molAB2压入一个盛有催化剂的10L密闭容器中进行反应: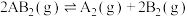 ,已知2min时,容器中剩余2molAB2,回答下列问题:
,已知2min时,容器中剩余2molAB2,回答下列问题:
(1)2min时AB2的物质的量浓度是___________ 。
(2)2min内平均反应速率:v(A2)=___________ 。
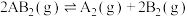 ,已知2min时,容器中剩余2molAB2,回答下列问题:
,已知2min时,容器中剩余2molAB2,回答下列问题:(1)2min时AB2的物质的量浓度是
(2)2min内平均反应速率:v(A2)=
您最近半年使用:0次
名校
解题方法
7 . 从能量的变化和反应的快慢等角度研究反应: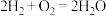 。
。
(1)为了加快反应速率,可以采取的措施有___________(填序号,下同)。
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是___________ 。
A.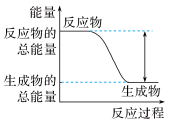 B.
B.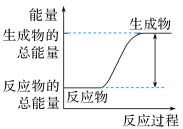
(3)在25℃、101kPa的条件下。
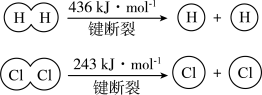
①由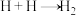 ,当生成1molH2时,要
,当生成1molH2时,要___________ (填“吸收”或“放出”)436kJ的能量;由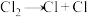 ,当断裂1molCl2中的共价键时,要
,当断裂1molCl2中的共价键时,要___________ (填“吸收”或“放出”)243kJ的能量。
②对于反应 ,测得生成2molHCl(g)时,反应过程中放出183kJ的热量,则断开1molH—Cl键所需的能量是
,测得生成2molHCl(g)时,反应过程中放出183kJ的热量,则断开1molH—Cl键所需的能量是___________ kJ。
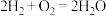 。
。(1)为了加快反应速率,可以采取的措施有___________(填序号,下同)。
| A.使用催化剂 | B.适当提高氧气的浓度 |
| C.适当提高反应的温度 | D.适当降低反应的温度 |
A.
 B.
B.
(3)在25℃、101kPa的条件下。

①由
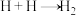 ,当生成1molH2时,要
,当生成1molH2时,要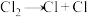 ,当断裂1molCl2中的共价键时,要
,当断裂1molCl2中的共价键时,要②对于反应
 ,测得生成2molHCl(g)时,反应过程中放出183kJ的热量,则断开1molH—Cl键所需的能量是
,测得生成2molHCl(g)时,反应过程中放出183kJ的热量,则断开1molH—Cl键所需的能量是
您最近半年使用:0次
8 . 化石燃料的综合利用既能减少污染,又能提高资源利用率。回答下列问题:
(1)煤的气化是将煤转化为气体燃料,其中重要的一步反应是高温下焦炭与水蒸气反应制备水煤气(CO、H2),该反应的化学方程式为___________ 。
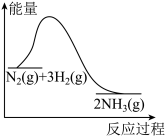
(2)合成氨工业是煤化工产业链中非常重要的一步。合成氨反应过程中的能量变化如图所示,则该反应为___________ (填“吸热”或“放热”)反应。
(3)实验室模拟工业合成氨,向2L恒容密闭容器内充入1molN2反应过程和3molH2,在一定条件下发生反应。若经过5min后,测得容器内NH3的物质的量为1mol,则这段时间内,v(N2)=___________ ,此时容器内H2的物质的量浓度为___________ 。
(4)天然气的主要成分是CH4.在酸性介质中,利用反应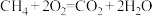 可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示(其中质子交换膜只允许H+通过):
可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示(其中质子交换膜只允许H+通过):
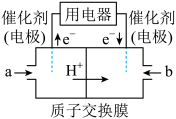
通入b气体的电极名称为___________ ,通入a气体的电极上反应式为___________ 。
(1)煤的气化是将煤转化为气体燃料,其中重要的一步反应是高温下焦炭与水蒸气反应制备水煤气(CO、H2),该反应的化学方程式为
(2)合成氨工业是煤化工产业链中非常重要的一步。合成氨反应过程中的能量变化如图所示,则该反应为

(3)实验室模拟工业合成氨,向2L恒容密闭容器内充入1molN2反应过程和3molH2,在一定条件下发生反应。若经过5min后,测得容器内NH3的物质的量为1mol,则这段时间内,v(N2)=
(4)天然气的主要成分是CH4.在酸性介质中,利用反应
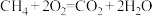 可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示(其中质子交换膜只允许H+通过):
可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示(其中质子交换膜只允许H+通过):
通入b气体的电极名称为
您最近半年使用:0次
2023-07-16更新
|
54次组卷
|
2卷引用:青海省西宁市大通回族土族自治县2022-2023学年高一下学期期末考试化学试题
名校
9 . H2S的转化是资源利用和环境保护的重要研究课题。回答下列问题:
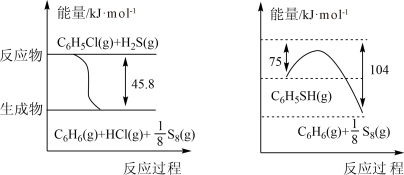
(1)苯硫酚(C6H5SH)是一种重要的有机合成中间体,工业上常用氯苯(C6H5Cl)和硫化氢(H2S)来制备苯硫酚。已知下列两个反应的能量关系如图所示,则C6H5Cl与H2S反应生成C6H5SH的热化学方程式为_______ 。
(2)H2S与CO2在高温下反应制得的羰基硫(COS)可用于合成除草剂。在610K时,将0.40molH2S与0.10molCO2充入2.5L的空钢瓶中,发生反应:H2S(g)+CO2(g)⇌COS(g)+H2O(g)ΔH=+35kJ/mol,反应达平衡后水蒸气的物质的量分数为0.02。
①在610K时,反应经2min达到平衡,则0~2min的平均反应速率v(H2S)=_______ 。
②实验测得上述反应的速率方程为:v正=k正·c(H2S)·c(CO2),v逆=k逆·c(COS)·c(H2O),k正、k逆分别为正、逆反应速率常数,速率常数k随温度升高而增大。则达到平衡后,仅升高温度,k正增大的倍数_______ (填“>”“<”或“=”)k逆增大的倍数。
③该条件下,容器中反应达到化学平衡状态的依据是_______ (填字母)。
A.容器内混合气体密度不再变化 B.v正(H2S)=v逆(COS)
C.容器内的压强不再变化 D.H2S与CO2的质量之比不变
(3)工业上可以通过硫化氢分解制得H2和硫蒸气。在密闭容器中充入一定量H2S气体,反应原理:2H2S(g)⇌2H2(g)+S2(g),H2S气体的平衡转化率与温度、压强的关系如图所示。
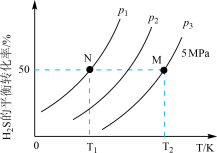
①图中压强(P1、P2、P3)的大小顺序为_______ ,理由是_______ 。
②如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有_______ 。
③在温度T2、P3=5MPa条件下,该反应的平衡常数Kp=_______ MPa(已知:用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)苯硫酚(C6H5SH)是一种重要的有机合成中间体,工业上常用氯苯(C6H5Cl)和硫化氢(H2S)来制备苯硫酚。已知下列两个反应的能量关系如图所示,则C6H5Cl与H2S反应生成C6H5SH的热化学方程式为

(2)H2S与CO2在高温下反应制得的羰基硫(COS)可用于合成除草剂。在610K时,将0.40molH2S与0.10molCO2充入2.5L的空钢瓶中,发生反应:H2S(g)+CO2(g)⇌COS(g)+H2O(g)ΔH=+35kJ/mol,反应达平衡后水蒸气的物质的量分数为0.02。
①在610K时,反应经2min达到平衡,则0~2min的平均反应速率v(H2S)=
②实验测得上述反应的速率方程为:v正=k正·c(H2S)·c(CO2),v逆=k逆·c(COS)·c(H2O),k正、k逆分别为正、逆反应速率常数,速率常数k随温度升高而增大。则达到平衡后,仅升高温度,k正增大的倍数
③该条件下,容器中反应达到化学平衡状态的依据是
A.容器内混合气体密度不再变化 B.v正(H2S)=v逆(COS)
C.容器内的压强不再变化 D.H2S与CO2的质量之比不变
(3)工业上可以通过硫化氢分解制得H2和硫蒸气。在密闭容器中充入一定量H2S气体,反应原理:2H2S(g)⇌2H2(g)+S2(g),H2S气体的平衡转化率与温度、压强的关系如图所示。

①图中压强(P1、P2、P3)的大小顺序为
②如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有
③在温度T2、P3=5MPa条件下,该反应的平衡常数Kp=
您最近半年使用:0次
2023-06-19更新
|
335次组卷
|
4卷引用:青海省西宁市大通回族土族自治县2023-2024学年高三上学期期中考试理综试题
10 . 合成氨是人工固氮的主要手段,对人类生存、社会进步和经济发展都有着重大意义。
(1)下列物质间能量的变化与合成氨的能量变化(如图所示)相符的是___________(填标号)。
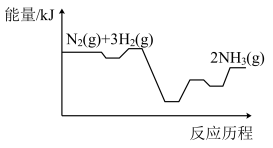
(2)一定温度下,在2L的某恒容密闭容器中,通入0.1mol 和0.3mol
和0.3mol ,发生反应
,发生反应
 ,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的
,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的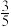 ,则:
,则:
①反应达到平衡时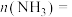
___________ mol。
②0~5min内,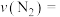
___________  。
。
③为了加快该反应的速率,除加入合适的催化剂,升高温度外,还可采取的措施为___________ (写一种即可)。
(3)利用反应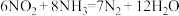 为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
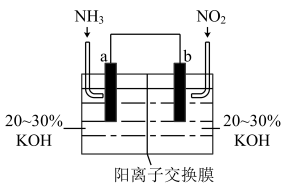
①电池工作时,电解质溶液中的 穿过阳离子交换膜向
穿过阳离子交换膜向___________ (填“a”或“b”)电极移动。
②b电极上的电极反应式为___________ 。
③电池工作一段时间后,左侧工作室溶液的pH___________ (填“变大”、“变小”或“不变”)。
(1)下列物质间能量的变化与合成氨的能量变化(如图所示)相符的是___________(填标号)。

| A.盐酸与碳酸氢钠的反应 | B.氢氧化钡与氯化铵的反应 |
| C.铝片与稀硫酸的反应 | D.氢气与氯气的反应 |
 和0.3mol
和0.3mol ,发生反应
,发生反应
 ,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的
,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的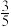 ,则:
,则:①反应达到平衡时
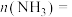
②0~5min内,
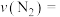
 。
。③为了加快该反应的速率,除加入合适的催化剂,升高温度外,还可采取的措施为
(3)利用反应
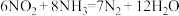 为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
①电池工作时,电解质溶液中的
 穿过阳离子交换膜向
穿过阳离子交换膜向②b电极上的电极反应式为
③电池工作一段时间后,左侧工作室溶液的pH
您最近半年使用:0次



