名校
解题方法
1 . 下列实验能达到预期目的是
| 实验内容 | 实验目的 | |
| A | 将 的 的 溶液和 溶液和 的 的 溶液等体积混合,充分反应后,取少许混合液滴加 溶液等体积混合,充分反应后,取少许混合液滴加 溶液 溶液 | 验证 与 与 的反应有一定限度 的反应有一定限度 |
| B | 装有二氧化氮和四氧化二氮混合气体的装置,一球放入热水中,一球放入冰水混合物中 | 探究温度对化学反应速率的影响 |
| C | 相同条件下,向一支试管中加入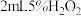 和 和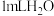 ,向另一支试管中加入 ,向另一支试管中加入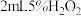 和 和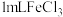 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 探究 对 对 分解速率的影响 分解速率的影响 |
| D | 向2支盛有 不同浓度 不同浓度 溶液的试管中,同时加入 溶液的试管中,同时加入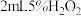 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-15更新
|
247次组卷
|
3卷引用:山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题
2 . 过硫酸钠(Na2S2O8)也叫高硫酸钠、过二硫酸钠,是白色晶状粉末,易溶于水,加热至65℃就会发生分解,用作漂白剂、氧化剂、乳液聚合促进剂。某化学小组对Na2S2O8制备和性质进行探究。
I.实验室制备Na2S2O8
【查阅资料】工业制备过硫酸钠的反应原理:
主反应:(NH4)2S2O8+2NaOH Na2S2O8+2NH3↑+2H2O
Na2S2O8+2NH3↑+2H2O
副反应:2NH3+3Na2S2O8+6NaOH 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
设计如图实验装置:

(1)恒压滴液漏斗的优点是___ 。
(2)装置a中反应产生的气体需要持续通入装置c的目的是___ ;装置b、d的作用分别是___ 、___ 。
(3)反应完毕,将三颈圆底烧瓶中的溶液减压浓缩、结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是___ 。
II.探究Na2S2O8的性质
(1)酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,该方法可用于检验Mn2+,所得溶液除去Ag+后加入BaCl2溶液可以产生白色沉淀。
①用酸性Na2S2O8溶液检验Mn2+时的实验现象为___ 。
②该反应的离子方程式为____ 。
(2)过硫酸钠溶液与铜反应只生成两种盐且反应先慢后快,某同学推测反应先慢后快的原因可能是生成的Cu2+对反应起催化作用,设计实验方案检验该推测是否正确___ 。(供选择试剂:Cu、Na2S2O8溶液、Na2SO4溶液、CuSO4溶液、Cu(NO3)2溶液、CuCl2溶液、蒸馏水)
I.实验室制备Na2S2O8
【查阅资料】工业制备过硫酸钠的反应原理:
主反应:(NH4)2S2O8+2NaOH
 Na2S2O8+2NH3↑+2H2O
Na2S2O8+2NH3↑+2H2O副反应:2NH3+3Na2S2O8+6NaOH
 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2设计如图实验装置:

(1)恒压滴液漏斗的优点是
(2)装置a中反应产生的气体需要持续通入装置c的目的是
(3)反应完毕,将三颈圆底烧瓶中的溶液减压浓缩、结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是
II.探究Na2S2O8的性质
(1)酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,该方法可用于检验Mn2+,所得溶液除去Ag+后加入BaCl2溶液可以产生白色沉淀。
①用酸性Na2S2O8溶液检验Mn2+时的实验现象为
②该反应的离子方程式为
(2)过硫酸钠溶液与铜反应只生成两种盐且反应先慢后快,某同学推测反应先慢后快的原因可能是生成的Cu2+对反应起催化作用,设计实验方案检验该推测是否正确
您最近一年使用:0次
3 . 下列实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 相同温度下,向两支盛有相同体积、相同浓度双氧水的试管中,分别滴入等量相同浓度的CuSO4溶液和FeCl3溶液 | 探究 、 、 对H2O2分解速率的影响 对H2O2分解速率的影响 |
| B | 将铁片和铜片用导线连接,插入浓HNO3中 | 比较铁和铜的失电子能力 |
| C | 向鸡蛋清溶液中加入CuSO4溶液,观察现象:然后加入蒸馏水振荡,观察现象 | 探究蛋白质的变性是否可逆 |
| D | 向淀粉的水解液中加入新制Cu(OH)2悬浊液,加热 | 检验淀粉是否水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



