解题方法
1 . 能量以多种不同的形式存在,并能相互转化。
I.化学反应伴随能量变化。
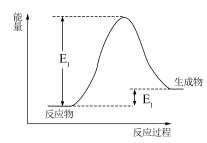
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,___________ 代表反应活化能(填“E1”或“E2”)。
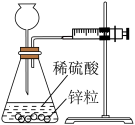
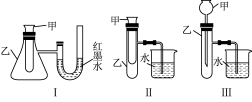
(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是___________ (填序号)。
(3)NH4HCO3和CH3COOH反应的离子方程式为___________ 。
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用 、
、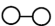 、
、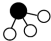 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
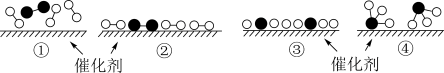
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。
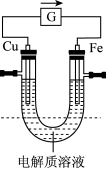
(5)电解质溶液为FeCl3时,图中箭头的方向表示___________ (填“电子”或“电流”)的流向,铁片上的电极反应式为___________ 。
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。
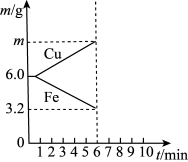
①X可以是___________ (填字母)。
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为___________ g。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,

(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是

(3)NH4HCO3和CH3COOH反应的离子方程式为
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用
 、
、 、
、 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)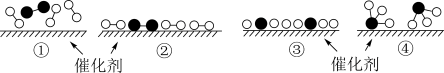
| A.反应过程存在非极性共价键的断裂和形成 |
| B.催化剂仅起到吸附N2和H2的作用,对化学反应速率没有影响 |
| C.②→③过程吸热 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。

(5)电解质溶液为FeCl3时,图中箭头的方向表示
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。

①X可以是
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为
您最近一年使用:0次
名校
2 . 下列装置与设计不能达到实验目的的是
选项 | A | B |
装置与设计 |
|
|
目的 | 测定锌与稀硫酸反应生成氢气的速率 | 探究催化剂对反应速率的影响 |
选项 | C | D |
装置与设计 |
|
|
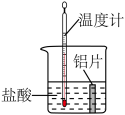
目的 | 证明铝片与盐酸的反应为放热反应 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
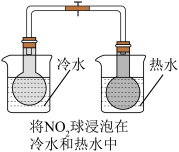
| A | 将盛有NO2气体的玻璃球放入热水浴中 | 探究2NO2(g) N2O4(g)的热效应 N2O4(g)的热效应 |
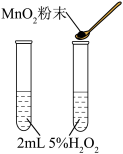
| B | 向各盛有5mLH2O2溶液的两支试管中分别滴入2滴0.1mol/L的FeCl3溶液和0.1mol/L的CuSO4溶液 | 比较Fe3+与Cu2+对H2O2分解的催化效果 |
| C | 向盛有淀粉溶液的试管中加入少量稀硫酸,加热,再滴加几滴银氨溶液,水浴加热 | 证明淀粉已发生水解 |
| D | 向5mL0.1mol/LAgNO3溶液中滴加几滴0.1mol/L NaCl溶液,再滴加几滴0.1mol/LKI溶液 | 验证Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 实验一:已知 ,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
设计如下(所取溶液体积均为10mL)。
(1)其他条件不变时,探究温度对化学反应速率的影响,应选择实验_____ (填实验编号);若同时选择实验①、实验②、实验③,测定混合液变浑浊的时间,可探究_____ 对化学反应速率的影响。
实验二:已知 ,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。
,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。
(2)表中
_____ ,
_____ 。
(3)利用实验1中数据计算,若用KMnO4溶液的浓度变化表示的反应速率为:
_____ 。
(4)在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大。针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大。从影响化学反应速率的因素看,你猜想还可能是_____ 的影响。
(5)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入_____(填字母)。
 ,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计如下(所取溶液体积均为10mL)。
| 实验编号 | 实验温度/℃ |  |  |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
实验二:已知
 ,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。
,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 3mol/L稀硫酸 | 0.05mol/LKMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 |  | 2.7 |
| 3 | 1.0 |  | 2.0 | 3.0 | 3.9 |


(3)利用实验1中数据计算,若用KMnO4溶液的浓度变化表示的反应速率为:

(4)在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大。针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大。从影响化学反应速率的因素看,你猜想还可能是
(5)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入_____(填字母)。
| A.硫酸钾 | B.硫酸锰 | C.氯化锰 | D.水 |
您最近一年使用:0次
2023-10-27更新
|
54次组卷
|
3卷引用:广东省东莞市东华高级中学2023-2024学年高二上学期期中联考化学试卷
名校
解题方法
5 . 小组同学探究影响 分解反应速率的因素。
分解反应速率的因素。
(1)在 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为_______________ 。
【实验方案】
(2)对比实验①和实验②,目的是探究______ 对 分解反应速率的影响。
分解反应速率的影响。
(3)对比实验②和实验③,目的是_____ 对 分解反应速率的影响,则实验③中x的值是
分解反应速率的影响,则实验③中x的值是_____ 。
(4)如果实验②中 时共收集到气体的体积为
时共收集到气体的体积为 (已折算成标准状况下),则用过氧化氢表示的
(已折算成标准状况下),则用过氧化氢表示的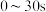 的平均反应速率为
的平均反应速率为__________  。
。
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如图所示。
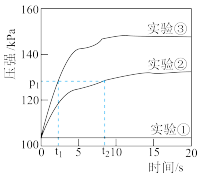
(5)上述实验中, 分解速率最快的是
分解速率最快的是_______ (填序号 );
(6)图中能证明 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是__________ 。
 分解反应速率的因素。
分解反应速率的因素。(1)在
 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为【实验方案】
| 实验编号 |  溶液 溶液 | 蒸馏水 | 催化剂 | 温度 | |
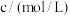 |  |  | |||
| ① | 3 | 10 | 20 | 无催化剂 | 20 |
| ② | 3 | 10 | 20 | 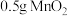 固体 固体 | 20 |
| ③ | 3 | 15 | x | 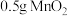 固体 固体 | 20 |
(2)对比实验①和实验②,目的是探究
 分解反应速率的影响。
分解反应速率的影响。(3)对比实验②和实验③,目的是
 分解反应速率的影响,则实验③中x的值是
分解反应速率的影响,则实验③中x的值是(4)如果实验②中
 时共收集到气体的体积为
时共收集到气体的体积为 (已折算成标准状况下),则用过氧化氢表示的
(已折算成标准状况下),则用过氧化氢表示的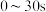 的平均反应速率为
的平均反应速率为 。
。【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如图所示。

(5)上述实验中,
 分解速率最快的是
分解速率最快的是(6)图中能证明
 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是
您最近一年使用:0次
名校
解题方法
6 . 下图有关实验或操作能达到实验目的的是


A.①证明 |
| B.②装置蒸发氯化铝溶液制备无水氯化铝 |
C.③装置可判断 反应的热效应 反应的热效应 |
| D.④验证氯化铁对过氧化氢的分解有催化作用 |
您最近一年使用:0次
名校
7 . (一)某同学探究外界条件对 分解速率的影响
分解速率的影响
实验所用试剂: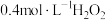 溶液、蒸馏水、
溶液、蒸馏水、 粉末、
粉末、 粉。
粉。
(1)实验1、2的目的是其他条件相同时,研究___________ 对 分解速率的影响。
分解速率的影响。
(2)表中a处所用试剂为___________ 。对比实验3、4可得出的结论是___________ 。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。b处取用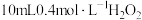 溶液,还应添加的试剂及用量为
溶液,还应添加的试剂及用量为___________ 。
(二)在2L的密闭容器中, 和
和 在催化剂和
在催化剂和 的条件下发生的反应。
的条件下发生的反应。 和
和 的物质的量随时间变化的关系曲线如图所示。
的物质的量随时间变化的关系曲线如图所示。
回答下列问题。

(4) ,以
,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是___________  。
。
(5)反应达到化学平衡状态的依据是___________ 。
a.单位时间内消耗 ,同时生成
,同时生成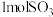
b. 的浓度与
的浓度与 浓度均不再变化
浓度均不再变化
c.正、逆反应速率相等且不等于零
d. 的浓度与
的浓度与 浓度相等
浓度相等
(6)对于 与
与 生成
生成 的反应,在
的反应,在 过量时,
过量时, 也不能完全转化为
也不能完全转化为 。对此现象,某小组同学提出三个观点:
。对此现象,某小组同学提出三个观点:
查阅资料得到以下两条事实:
其中可以证明观点一不正确的事实是(填①或填②,下同)___________ ,可以证明观点三不正确的事实是;___________ ;符合观点二的事实是①②
 分解速率的影响
分解速率的影响实验所用试剂:
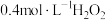 溶液、蒸馏水、
溶液、蒸馏水、 粉末、
粉末、 粉。
粉。| 实验序号 |  浓度 浓度 | V( 溶液)(mL) 溶液)(mL) | 温度 | 催化剂 | 收集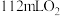 所需时间(s) 所需时间(s) |
| 1 | 0.4 | 20 | 室温 | 无 | 几乎无气体产生 |
| 2 | 0.4 | 20 | 50℃水浴 | 296 | 296 |
| 3 | 0.4 | 20 | 室温 | 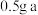 | 45 |
| 4 | 0.4 | 20 | 室温 | 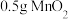 粉末 粉末 | 100 |
| 5 | 0.4 |  | 室温 | 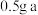 |  |
 分解速率的影响。
分解速率的影响。(2)表中a处所用试剂为
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。b处取用
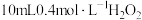 溶液,还应添加的试剂及用量为
溶液,还应添加的试剂及用量为(二)在2L的密闭容器中,
 和
和 在催化剂和
在催化剂和 的条件下发生的反应。
的条件下发生的反应。 和
和 的物质的量随时间变化的关系曲线如图所示。
的物质的量随时间变化的关系曲线如图所示。回答下列问题。

(4)
 ,以
,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是 。
。(5)反应达到化学平衡状态的依据是
a.单位时间内消耗
 ,同时生成
,同时生成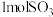
b.
 的浓度与
的浓度与 浓度均不再变化
浓度均不再变化c.正、逆反应速率相等且不等于零
d.
 的浓度与
的浓度与 浓度相等
浓度相等(6)对于
 与
与 生成
生成 的反应,在
的反应,在 过量时,
过量时, 也不能完全转化为
也不能完全转化为 。对此现象,某小组同学提出三个观点:
。对此现象,某小组同学提出三个观点:观点一:只有部分 与 与 反应 反应 |
观点二: 与 与 反应生成 反应生成 的同时, 的同时, 分解生成 分解生成 与 与 |
观点三: 全部转化为 全部转化为 后,部分 后,部分 又转化为 又转化为 |
| 事实① | 事实② |
一定条件下向密闭容器中充入 和 和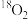 ,反应一段时间后, ,反应一段时间后,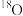 存在于 存在于 、 、 、 、 中 中 | 反应过程中, 的物质的量变化趋势如图所示 的物质的量变化趋势如图所示 |
您最近一年使用:0次
名校
解题方法
8 .  是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。
(一)A实验小组拟在同浓度 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。
(1)写出本实验 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:___________ 。
(2)设计实验方案:在不同 浓度下,测定
浓度下,测定___________ (要求所测得的数据能直接体现反应速率大小)。
(二)B实验小组在验证 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。
实验Ⅰ:
(3)实验Ⅰ中溶液变红的原因是___________ 。(请用离子方程式表示其原理)
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,___________ (填实验操作和现象),证明溶液中有 ,而几乎无
,而几乎无 。
。
(5)查阅资料发现,酸性溶液中 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
实验Ⅱ:

实验Ⅲ:
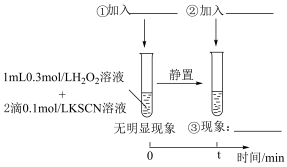
①___________ ;②___________ ;③___________ 。
(三)C实验小组猜测, 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。
(6)实验Ⅳ:
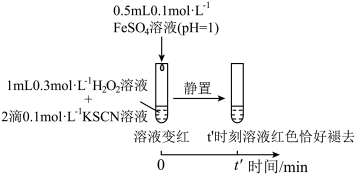
实验得知,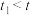 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,___________ 。
 是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。(一)A实验小组拟在同浓度
 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。(1)写出本实验
 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:(2)设计实验方案:在不同
 浓度下,测定
浓度下,测定(二)B实验小组在验证
 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。实验Ⅰ:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加 溶液,红色变浅并逐渐褪去 溶液,红色变浅并逐渐褪去 |
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,
 ,而几乎无
,而几乎无 。
。(5)查阅资料发现,酸性溶液中
 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。实验Ⅱ:

实验Ⅲ:

①
(三)C实验小组猜测,
 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。(6)实验Ⅳ:

实验得知,
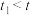 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
您最近一年使用:0次
2023-10-19更新
|
162次组卷
|
2卷引用:广东省广州市执信中学2023-2024学年高二上学期10月选考化学试题
名校
9 . 下列实验方案不能达到相应实验目的的是


| A.用装置①定量测定化学反应速率 |
B.用装置②探究 浓度对化学反应速率的影响 浓度对化学反应速率的影响 |
C.用装置③探究催化剂对 分解速率的影响 分解速率的影响 |
| D.用装置④证明铝片与盐酸的反应为放热反应 |
您最近一年使用:0次
名校
10 . 某化学小组为了探究外界条件对化学反应速率的影响,进行了如下实验。
【实验原理】

【实验内容及记录】
(1)实验原理中,1 mol KMnO4参加反应时,转移电子的物质的量为_______ mol。
(2)实验①、②探究的是_______ 对反应速率的影响,表中Vx=_______ 。
(3)由实验①、③可得出的结论是_______ 。
(4)实验①中,4.0 min内,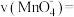
_______ mol·L ·min
·min 。
。
(5)反应过程中,反应速率随时间的变化趋势如图所示。

其中,因反应放热导致温度升高对速率影响不大,试推测t1-t2速率迅速增大的主要原因是_______ 。若用实验证明你的推测,除了表中试剂外,还需向试管中加入少量固体,该固体应为_______ (填标号)。
A.K2SO4 B.MnSO4 C.MnO2
【实验原理】

【实验内容及记录】
| 实验序号 | 温度/℃ | 试管中所加试剂及其用量/mL | 溶液紫色褪至无色时所需时间/min | |||
| 0.04 mol/L KMnO4溶液 | 0.36 mol/L稀硫酸 | 0.2 mol/L H2C2O4溶液 | H2O | |||
| ① | 20 | 1.0 | 1.0 | 2.0 | 2.0 | 4.0 |
| ② | 20 | 1.0 | 1.0 | 3.0 | Vx | 3.6 |
| ③ | 40 | 1.0 | 1.0 | 2.0 | 2.0 | 0.92 |
(2)实验①、②探究的是
(3)由实验①、③可得出的结论是
(4)实验①中,4.0 min内,
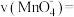
 ·min
·min 。
。(5)反应过程中,反应速率随时间的变化趋势如图所示。

其中,因反应放热导致温度升高对速率影响不大,试推测t1-t2速率迅速增大的主要原因是
A.K2SO4 B.MnSO4 C.MnO2
您最近一年使用:0次
2023-03-05更新
|
377次组卷
|
3卷引用:广东省广州市黄埔区2022-2023学年高二上学期期末考试化学试题