名校
1 . 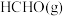 与
与 在催化剂羟基磷灰石(简写为
在催化剂羟基磷灰石(简写为 )表面催化生成
)表面催化生成 和
和 的历程示意图如下。下列说法错误的是
的历程示意图如下。下列说法错误的是

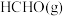 与
与 在催化剂羟基磷灰石(简写为
在催化剂羟基磷灰石(简写为 )表面催化生成
)表面催化生成 和
和 的历程示意图如下。下列说法错误的是
的历程示意图如下。下列说法错误的是
A. 和 和 分子的 分子的 模型都是四面体形 模型都是四面体形 |
| B.羟基磷灰石(HAP)的作用是加快反应速率 |
C. 与 与 分子中的中心原子的杂化轨道类型相同 分子中的中心原子的杂化轨道类型相同 |
| D.该反应过程既有极性共价键的断裂,也有非极性共价键的断裂 |
您最近一年使用:0次
2 . CO甲烷化反应为: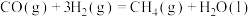 。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略),其中步骤②反应速率最慢。
。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略),其中步骤②反应速率最慢。
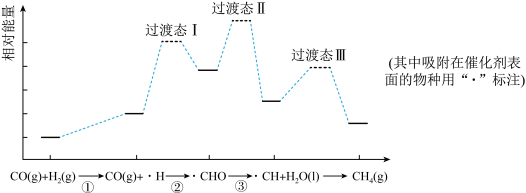
下列说法不正确 的是
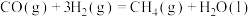 。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略),其中步骤②反应速率最慢。
。下图是使用某种催化剂时转化过程中的能量变化(部分物质省略),其中步骤②反应速率最慢。
下列说法
| A.步骤①只有极性键断裂 |
| B.步骤②速率最慢的原因可能是其活化能最高 |
| C.步骤③是吸热反应 |
| D.使用该催化剂不能有效提高CO的平衡转化率 |
您最近一年使用:0次
名校
3 . 反应物(S)转化为产物(P或P•Z)的能量与反应进程的关系如图所示
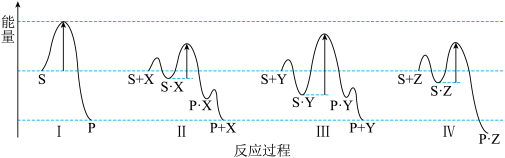
下列有关四种不同反应进程的说法正确的是

下列有关四种不同反应进程的说法正确的是
| A.进程I是吸热反应 | B.平衡时P的产率:II>I |
| C.生成P的速率:III<II | D.进程IV中,Z没有催化作用 |
您最近一年使用:0次
名校
解题方法
4 . 用钛(Ru)基催化剂催化CO2(g)和H2(g)反应生成2mol液态HCOOH放出62.4kJ热量的图示如图,下列说法正确的是
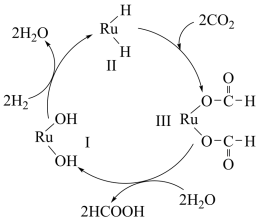

| A.图示中物质Ⅱ为该反应的催化剂 |
| B.图示中参与循环的物质只有CO2和H2 |
| C.该反应的活化能为62.4kJ•mol-1 |
| D.该反应的热化学方程式为H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ•mol-1 |
您最近一年使用:0次
名校
解题方法
5 . 在合成氨工业中,为增加NH3的日产量,下列措施与平衡移动无关的是
| A.不断将氨分离出来 |
| B.使用催化剂 |
| C.采用450℃左右的高温而不是650℃的高温 |
| D.采用10Mpa—30Mpa的压强 |
您最近一年使用:0次
2022-11-09更新
|
29次组卷
|
2卷引用:海南省海口市第四中学2023-2024学年高二上学期11月期中考试化学试题
6 .  与
与 在催化剂表面生成
在催化剂表面生成 ,反应历程及能量变化示意图如下所示,
,反应历程及能量变化示意图如下所示,不正确 的是
 与
与 在催化剂表面生成
在催化剂表面生成 ,反应历程及能量变化示意图如下所示,
,反应历程及能量变化示意图如下所示,
| A.①→②放出能量 | B.②→③形成了N-H键 |
| C.该反应为放热反应 | D.该催化剂可降低反应活化能 |
您最近一年使用:0次
2022-04-11更新
|
191次组卷
|
3卷引用:海南省海口嘉勋高级中学2022-2023学年高二上学期10月检测化学试题
名校
7 . 已知反应:2NO(g)+Br2(g)=2NOBr(g) △H=-a kJ·mol-1(a>0),其反应机理如下:
①NO(g)+Br2(g)=NOBr2(g) △H1 快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2 慢反应。
下列说法正确的是
①NO(g)+Br2(g)=NOBr2(g) △H1 快反应;
②NO(g)+NOBr2(g)=2NOBr(g) △H2 慢反应。
下列说法正确的是
| A.NOBr2是该反应的催化剂 |
| B.该反应的速率主要取决于反应① |
| C.△H=△H1+△H2 |
| D.恒容时,增大Br2(g)的浓度能增加单位体积内活化分子的百分数,有效碰撞增加,加快反应速率 |
您最近一年使用:0次
2021-11-02更新
|
330次组卷
|
2卷引用:海南省华中师范大学海南附属中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
8 . 实验小组欲通过测定单位时间内生成 的速率,探究某种影响化学反应速率的因素,设计实验方案如下:
的速率,探究某种影响化学反应速率的因素,设计实验方案如下:
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
请回答:
(1)该反应的离子方程式______________________________________________ 。
(2)该实验目的是探究_______________________________________________
(3)V=_________ 
(4)利用实验1中数据计算,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率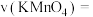
______________ mol/(L·min) 。
(5)该小组同学根据经验绘制了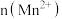 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中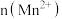 随时间变化的趋势应如图2所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
随时间变化的趋势应如图2所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①甲同学提出的假设是_______________________________________________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
③若甲同学提出的假设成立,再向试管中加入少量该固体后,应观察到的现象与实验1比较,溶液褪色所需时间比4min_________ (填“短”、“长”或“相同”)。
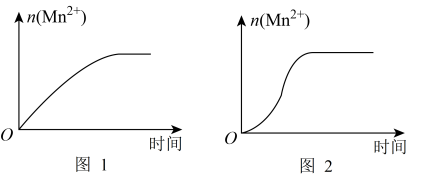
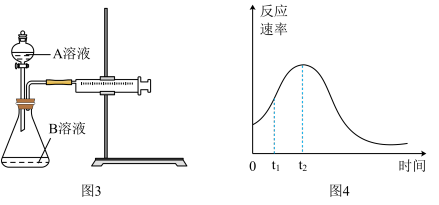
(6)乙同学用图3装置开展实验,发现反应速率总是图4,其中t1~t2时间内速率变快。乙同学认为主要原因可能存在甲提出的假设成立外,还可能有其他原因________________________ 。
 的速率,探究某种影响化学反应速率的因素,设计实验方案如下:
的速率,探究某种影响化学反应速率的因素,设计实验方案如下:【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量 | 室温下溶液颜色褪至无色所需时间 | |||
0.6 mol/L 溶液 溶液 |  |  溶液 溶液 | 3 mol/L 稀硫酸 | ||
| 1 |  |  |  |  |  |
| 2 |  |  |  |  | 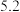 |
| 3 |  |  |  |  |  |
(1)该反应的离子方程式
(2)该实验目的是探究
(3)V=

(4)利用实验1中数据计算,用
 的浓度变化表示的反应速率
的浓度变化表示的反应速率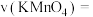
(5)该小组同学根据经验绘制了
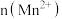 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中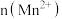 随时间变化的趋势应如图2所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
随时间变化的趋势应如图2所示.该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①甲同学提出的假设是
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量 | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 | |||
0.6mol/L 溶液 溶液 |  | 0.2mol/L KMnO4溶液 | 3mol/L 稀硫酸 | |||
| 4 |  |  |  |  | MnSO4 | t |
(6)乙同学用图3装置开展实验,发现反应速率总是图4,其中t1~t2时间内速率变快。乙同学认为主要原因可能存在甲提出的假设成立外,还可能有其他原因

您最近一年使用:0次
解题方法
9 . T ℃时,在2 L的密闭容器中,气体X、Y和Z三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是


A.容器中化学反应为X(g)+Y(g)  Z(g) Z(g) |
| B.0~10 s,X表示的平均化学反应速率为0.04 mol/(L·s) |
| C.使用催化剂只能加快0~10 s间的反应速率 |
| D.10s时Z的浓度为1.6mol/L |
您最近一年使用:0次
名校
10 . 下列说法中正确的是( )
| A.NaOH溶液与稀盐酸反应的活化能几乎为零 |
| B.活化分子之间发生的碰撞一定是有效碰撞 |
| C.升高温度和增大压强都可以提高反应体系内活化分子百分数 |
| D.催化剂可以改变反应的活化能,可以提高活化分子百分数,但是不能改变反应热 |
您最近一年使用:0次



