名校
解题方法
1 . 羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物 的反应机理如图所示,其中由①生成③的反应速率最慢。下列说法正确的是
的反应机理如图所示,其中由①生成③的反应速率最慢。下列说法正确的是

 的反应机理如图所示,其中由①生成③的反应速率最慢。下列说法正确的是
的反应机理如图所示,其中由①生成③的反应速率最慢。下列说法正确的是
| A.①为该反应的中间产物 |
| B.由③生成④的过程中有极性键的断裂和非极性键的生成 |
| C.由①生成③的反应在各步骤中吸收的热量最多 |
D.合成物质⑦的总反应为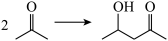 +2 +2 |
您最近半年使用:0次
2024-04-06更新
|
169次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
2 . 下列叙述正确的是


| A.由图甲可知, 2SO3(g)⇌2SO2(g)+O2(g) ∆H=(b-a)kJ·mol-1 |
| B.图乙表示反应物断键吸收的能量大于生成物成键放出的能量 |
| C.图丙表示燃料燃烧反应的能量变化 |
| D.图丁表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
您最近半年使用:0次
3 . 下列是哈伯法制氨气的流程图,其中为提高反应速率而采取的措施是
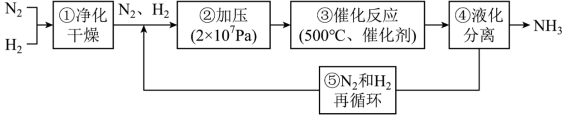

| A.①③④⑤ | B.①②③ | C.①②④ | D.②③④ |
您最近半年使用:0次
名校
解题方法
4 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如下:

下列说法正确的是

下列说法正确的是
| A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=+akJ/mol(a>0) |
| B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量 |
| C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗 |
| D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
您最近半年使用:0次
2024-01-21更新
|
133次组卷
|
5卷引用:北京市第三十五中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
5 . 已知反应S2O (aq)+2I-(aq)=2SO
(aq)+2I-(aq)=2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图,有关该反应的说法错误的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图,有关该反应的说法错误的是
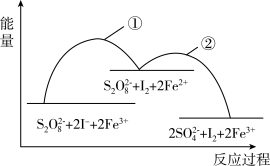
①:2Fe3+(aq)+2I-(aq)=I2(aq)+2Fe2+(aq)
②:2Fe2+(aq)+S2O (aq)=2Fe3+(aq)+2SO
(aq)=2Fe3+(aq)+2SO (aq)
(aq)
 (aq)+2I-(aq)=2SO
(aq)+2I-(aq)=2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图,有关该反应的说法错误的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图,有关该反应的说法错误的是
①:2Fe3+(aq)+2I-(aq)=I2(aq)+2Fe2+(aq)
②:2Fe2+(aq)+S2O
 (aq)=2Fe3+(aq)+2SO
(aq)=2Fe3+(aq)+2SO (aq)
(aq)| A.反应①和反应②相比,反应②更容易发生 |
| B.反应①和②都是放热反应 |
| C.增大Fe3+的浓度,能够加快反应速率 |
| D.Fe3+是该反应的催化剂 |
您最近半年使用:0次
名校
6 . 氨在能源、化肥生产等领域有着非常重要的用途。
(1)与H2-O2燃料电池相比,氨易液化、运输和储存方便,安全性能更高。新型NH3-O2燃科电池原理如下图所示:OH-离子向________ 移动(填“电极1或“电极2”),电极2的反应式为___________ 。

(2)氨的合成是当前的研究热点,目前最主要的方法是Haber-Bosch法:通常用以铁为主的催化剂在400~500℃和10~30MPa的条件下,由氮气和氢气直接合成氨。
①该反应放热,但仍选择较高温度。其原因是___________ 。
②列举一条既能提高速率又能提高原料转化率的措施___________ 。
(3)常温常压下电解法合成氨的原理如下图所示:
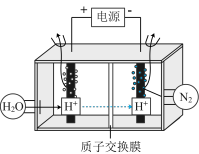
①阳极产生的气体是___________ 。
②阴极生成氨的电极反应式为___________ 。
③经检测在阴极表面发生了副反应,导致氨的产量降低。出该反应的电极反应式___________ 。
④为了尽可能避免副反应的发生,采用的方法是改进阴极表面的催化剂,这样设计是利用了催化剂具有___________ 性。
(1)与H2-O2燃料电池相比,氨易液化、运输和储存方便,安全性能更高。新型NH3-O2燃科电池原理如下图所示:OH-离子向

(2)氨的合成是当前的研究热点,目前最主要的方法是Haber-Bosch法:通常用以铁为主的催化剂在400~500℃和10~30MPa的条件下,由氮气和氢气直接合成氨。
①该反应放热,但仍选择较高温度。其原因是
②列举一条既能提高速率又能提高原料转化率的措施
(3)常温常压下电解法合成氨的原理如下图所示:

①阳极产生的气体是
②阴极生成氨的电极反应式为
③经检测在阴极表面发生了副反应,导致氨的产量降低。出该反应的电极反应式
④为了尽可能避免副反应的发生,采用的方法是改进阴极表面的催化剂,这样设计是利用了催化剂具有
您最近半年使用:0次
名校
7 . 一定条件下密闭容器中发生:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=akJ/mol反应过程中能量变化如图所示,下列说法正确的是
4NO(g)+6H2O(g) △H=akJ/mol反应过程中能量变化如图所示,下列说法正确的是

 4NO(g)+6H2O(g) △H=akJ/mol反应过程中能量变化如图所示,下列说法正确的是
4NO(g)+6H2O(g) △H=akJ/mol反应过程中能量变化如图所示,下列说法正确的是
| A.由图可知a>0 |
| B.将容器体积减小为原体积的一半时,水蒸气的浓度增大 |
| C.反应体系中加入催化剂可增加反应热, |
| D.升高温度可以提高NH3的转化率 |
您最近半年使用:0次
名校
8 . 金属催化剂在有机合成中有重要应用。
(1)合成芳香炔化合物的方法之一是在金属催化下,含炔氢的分子与溴苯反应,如:
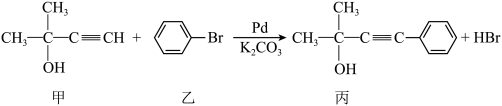
根据上式,请回答:
①按官能团分类,甲属于___________ ;丙能发生的反应是___________ (填字母序号)。
a.取代反应 b.加成反应 c.水解反应 d.氧化反应
②以苯为原料生成乙的化学方程式是___________ 。
③由丙制备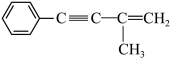 的反应条件是
的反应条件是___________ 。
④下列试剂能用来鉴别丙和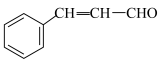 的是
的是___________ (填字母序号)。
a.NaOH溶液 b.银氨溶液 c.FeCl3溶液 d.溴水
(2)在催化剂表面,一种合成碳酸二甲酯的反应机理如下图:

①该反应中催化剂是___________ 。
②合成碳酸二甲酯的总反应方程式为___________ 。
(1)合成芳香炔化合物的方法之一是在金属催化下,含炔氢的分子与溴苯反应,如:

根据上式,请回答:
①按官能团分类,甲属于
a.取代反应 b.加成反应 c.水解反应 d.氧化反应
②以苯为原料生成乙的化学方程式是
③由丙制备
 的反应条件是
的反应条件是④下列试剂能用来鉴别丙和
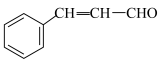 的是
的是a.NaOH溶液 b.银氨溶液 c.FeCl3溶液 d.溴水
(2)在催化剂表面,一种合成碳酸二甲酯的反应机理如下图:

①该反应中催化剂是
②合成碳酸二甲酯的总反应方程式为
您最近半年使用:0次
名校
9 . 某反应的反应机理可以分成如下两步,下列说法错误的是
| 反应机理 | 第一步反应 | 第二步反应 |
 (慢反应) (慢反应) | 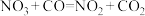 (快反应) (快反应) |
| A.在条件相同时,该反应的速率由第一步反应速率决定 |
| B.该反应的总反应方程式为NO2+CO=NO+CO2 |
| C.升高温度只会影响第一步反应速率,对第二步反应速率无影响 |
| D.加入合适的催化剂可降低反应的活化能,加快反应速率 |
您最近半年使用:0次
2024-01-01更新
|
136次组卷
|
11卷引用:安徽省A10联盟2022届高三上学期摸底考试化学试题
安徽省A10联盟2022届高三上学期摸底考试化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题陕西省宝鸡市金台区2021-2022学年高二上学期期中考试化学(理)试题(已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)2021年广东省高考化学试卷变式题11-21吉林省长春市第二十中学2021-2022学年高二上学期第一次质量检测化学试题湖北省武汉市部分学校2021-2022学年高二上学期12月联考化学试题四川省兴文第二中学校2023-2024学年高二上学期11月期中考试化学试题陕西省渭南市杜桥中学2023-2024学年高二上学期期中考试化学试卷 (已下线)专题02 化学反应速率-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题
名校
解题方法
10 . 二氧化硫的污染治理是化学研究的重要课题。
(1)石灰石-石膏法是一种常见的“钙基固硫”方法。其中,石灰石的溶解率与脱硫效果有着密切的关系。
可将催化条件下CaCO3吸收SO2宏观反应分为三步:
i.CaCO3由固相溶解进入液相,溶解速率为RA;
ii.SO2由气相扩散进入液相,扩散速率为RB;
iii.在催化剂作用下,溶解的SO2和Ca2+发生化学反应,且反应在液相中进行,反应速率为RC。温度变化对总反应速率的影响如图所示。___________ (填“RA”、“RB”或“Rc”)控制。
②45~55℃(催化剂活性不变)曲线呈下降趋势的原因:一是二氧化硫溶解度随温度升高而降低;二是___________ 。
(2)利用MnO2与SO2反应既可消除污染又可以制备MnSO4,将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c( )随反应时间的变化如图所示。导致溶液中c(Mn2+)和c(
)随反应时间的变化如图所示。导致溶液中c(Mn2+)和c( )的变化产生明显差异的原因是:
)的变化产生明显差异的原因是:_______ 。 与NO2反应的离子方程式为
与NO2反应的离子方程式为___________ 。
②请描述水催化促进硫酸盐形成的化学机制:通过“水分子桥”,处于纳米液滴中的 或
或 可以将电子快速转移给周围的气相NO2分子,
可以将电子快速转移给周围的气相NO2分子,___________ 。
(1)石灰石-石膏法是一种常见的“钙基固硫”方法。其中,石灰石的溶解率与脱硫效果有着密切的关系。
可将催化条件下CaCO3吸收SO2宏观反应分为三步:
i.CaCO3由固相溶解进入液相,溶解速率为RA;
ii.SO2由气相扩散进入液相,扩散速率为RB;
iii.在催化剂作用下,溶解的SO2和Ca2+发生化学反应,且反应在液相中进行,反应速率为RC。温度变化对总反应速率的影响如图所示。
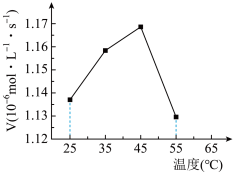
②45~55℃(催化剂活性不变)曲线呈下降趋势的原因:一是二氧化硫溶解度随温度升高而降低;二是
(2)利用MnO2与SO2反应既可消除污染又可以制备MnSO4,将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c(
 )随反应时间的变化如图所示。导致溶液中c(Mn2+)和c(
)随反应时间的变化如图所示。导致溶液中c(Mn2+)和c( )的变化产生明显差异的原因是:
)的变化产生明显差异的原因是: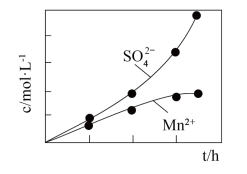
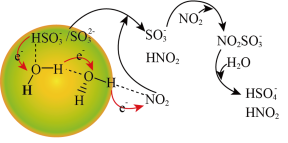
 与NO2反应的离子方程式为
与NO2反应的离子方程式为②请描述水催化促进硫酸盐形成的化学机制:通过“水分子桥”,处于纳米液滴中的
 或
或 可以将电子快速转移给周围的气相NO2分子,
可以将电子快速转移给周围的气相NO2分子,
您最近半年使用:0次
2023-12-25更新
|
219次组卷
|
5卷引用:江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题
江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题江苏省丹阳高级中学2023届高三上学期第一次阶段考试化学试题江苏省建湖高级中学2023-2024学年高三上学期暑期学情检测(一)化学试题江苏省如皋中学2023-2024学年高三上学期阶段考试(二) 化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)



