1 . Ⅰ.氢能是重要的新能源。他的开发、储存和应用,是当前人们关注的热点之一、
(1)开发氢能的方法之一是分解水。开发特殊物质做催化剂,___________ (填“能”或“不能”)降低水分解过程中所需能量。
(2)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2mol•L﹣1的KOH溶液,如图:
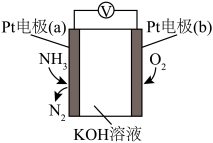
①此反应消耗的NH3与O2的物质的量之比为___________ 。
②a电极作为该原电池的___________ (填“正极”或“负极”),其电极反应式为 ___________ 。
③b电极上发生___________ (填“氧化”或“还原”)反应,溶液中OH-向___________ (填“a”或“b”)电极移动。
④每消耗17g NH3转移的电子数目为___________ 。
Ⅱ.人们通过化学方法可以开辟新能源和提高能源的利用率,根据情景回答下列问题:
(3)工业合成氨反应 是放热的可逆反应。已知高温高压1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将0.5molN2(g)和足量
是放热的可逆反应。已知高温高压1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将0.5molN2(g)和足量 (g)混合,使其充分反应,放出的热量
(g)混合,使其充分反应,放出的热量___________ (填“大于”“小于”或“等于”)46kJ。
(4)在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol ,用
,用 的化学反应速率为
的化学反应速率为___________ 
Ⅲ.汽车行驶、某些化工厂生产过程,会向空气中排放出NOx、CO、SO2等有害气体。
(5)NOx对环境的主要影响有___________(填字母标号)。
(6)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O
①用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量):
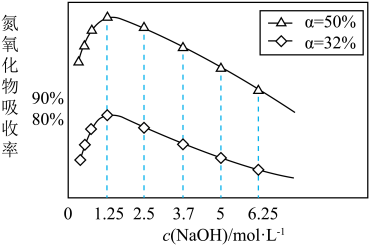
用NaOH溶液吸收氮氧化物的最佳条件为:α=___________ ,c(NaOH)=___________ 。
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为___________ 。
(1)开发氢能的方法之一是分解水。开发特殊物质做催化剂,
(2)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2mol•L﹣1的KOH溶液,如图:

①此反应消耗的NH3与O2的物质的量之比为
②a电极作为该原电池的
③b电极上发生
④每消耗17g NH3转移的电子数目为
Ⅱ.人们通过化学方法可以开辟新能源和提高能源的利用率,根据情景回答下列问题:
(3)工业合成氨反应
 是放热的可逆反应。已知高温高压1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将0.5molN2(g)和足量
是放热的可逆反应。已知高温高压1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将0.5molN2(g)和足量 (g)混合,使其充分反应,放出的热量
(g)混合,使其充分反应,放出的热量(4)在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol
 ,用
,用 的化学反应速率为
的化学反应速率为
Ⅲ.汽车行驶、某些化工厂生产过程,会向空气中排放出NOx、CO、SO2等有害气体。
(5)NOx对环境的主要影响有___________(填字母标号)。
| A.硝酸型酸雨 | B.温室效应 | C.破坏臭氧层 | D.光化学烟雾 |
①用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图(α表示NOx中NO2的含量):

用NaOH溶液吸收氮氧化物的最佳条件为:α=
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为
您最近一年使用:0次
名校
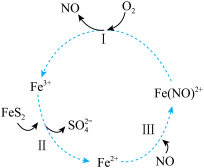
2 . 在酸性条件下,黄铁矿( )催化氧化的反应方程式为
)催化氧化的反应方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
 )催化氧化的反应方程式为
)催化氧化的反应方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
| A.在酸性条件下,黄铁矿催化氧化中NO作催化剂 |
| B.整个反应中,被氧化与被还原的元素的质量之比为7∶4 |
C.反应I的离子方程式为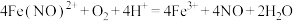 |
D.反应II的离子方程式为14Fe3++FeS2+8H2O=2 +15Fe2++16H+ +15Fe2++16H+ |
您最近一年使用:0次
解题方法
3 . Ⅰ. 已知某反应:A(g)+ 3B(g)  C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
(1)t1 h时,c(D) ___________ mol/L。
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)___________ mol·L-1·h-1。
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为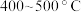 ,原因是
,原因是_________________________ 。
(5)合成氨反应可能的微观历程如图所示:
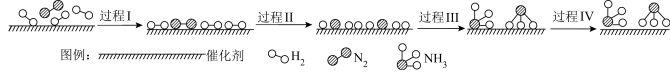
吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为___________ 。
 C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。浓度/( ) ) | c(A) | c(B) | c(D) |
| 0 | 1.0 | 3.0 | 0 |
 h h | 0.8 | ||
 h h | 2.1 |
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
| A.容器中的压强不随时间变化 | B.气体密度不再变化 |
| C.B和D的浓度之比为3:4 | D.消耗0.3 mol B的同时生成0.4 mol D |
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为
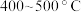 ,原因是
,原因是(5)合成氨反应可能的微观历程如图所示:

吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为
 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为
您最近一年使用:0次
名校
4 . 反应2NO + 2CO N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是
N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是
 N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是
N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是| A.升高温度能加快反应速率 |
| B.减小NO浓度能加快反应速率 |
| C.使用恰当的催化剂不能加快反应速率 |
| D.CO可以100%转化为产物 |
您最近一年使用:0次
2022-12-07更新
|
165次组卷
|
7卷引用:江苏省常州市八校2021-2022学年高一下学期期末联合调研化学试题
名校
5 . 已知某反应的一种反应机理如图所示,下列说法错误 的是


A. 参与了该催化循环 参与了该催化循环 |
B.该反应可消耗温室气体 |
C.该催化循环中 的成键数目发生变化 的成键数目发生变化 |
D. 降低了该反应的活化能,提高了化学反应速率 降低了该反应的活化能,提高了化学反应速率 |
您最近一年使用:0次
2022-12-02更新
|
340次组卷
|
5卷引用:浙江省乐清市知临中学2022-2023学年高一上学期期中考试化学试题(B)
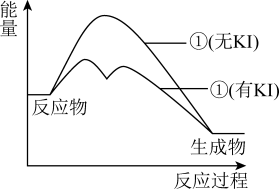
6 . H2O2是重要的消毒剂、氧化剂,研究其分解反应有重要意义。KI溶液能催化H2O2的分解。
①不加KI溶液: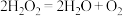
②加入KI溶液: ;
;
H2O2分解反应过程中能量变化如图所示。下列判断不正确 的是
①不加KI溶液:
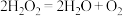
②加入KI溶液:
 ;
;
H2O2分解反应过程中能量变化如图所示。下列判断

A.加入KI溶液后改变了反应的历程,第一步反应 是吸热反应,是控速的一步 是吸热反应,是控速的一步 |
B.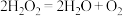 属于四大基本反应类型中的分解反应,H2O2分解时放出热量 属于四大基本反应类型中的分解反应,H2O2分解时放出热量 |
| C.反应速率与I-的浓度有关 |
D.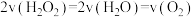 |
您最近一年使用:0次
7 . 常温下向双氧水的酸性溶液中滴入少量的FeSO4溶液,发生如下转化关系。下列说法不正确的是


| A.一定条件下,Fe3+可以做H2O2分解反应的催化剂 |
| B.图中转化关系表明氧化性由强到弱顺序为Fe3+>Fe2+>H2O2 |
| C.图中转化关系说明H2O2既有氧化性又有还原性 |
| D.生产和贮运H2O2的过程中要避免混入Fe2+或者Fe3+ |
您最近一年使用:0次
名校
解题方法
8 . 某温度下,向10mL0.40mol•L-1H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算标况)如表所示。
资料显示,反应分两步进行:
①2Fe3++H2O2=2Fe2++O2↑+2H+
②H2O2+2Fe2++2H+=2H2O+2Fe3+
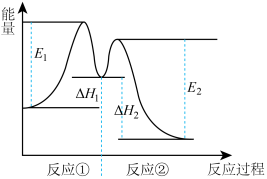
反应过程中能量变化如图所示:
下列说法不正确的是
| t/min | 0 | 2 | 4 | 6 |
| V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 |
①2Fe3++H2O2=2Fe2++O2↑+2H+
②H2O2+2Fe2++2H+=2H2O+2Fe3+
反应过程中能量变化如图所示:

下列说法不正确的是
| A.Fe3+的作用是增大过氧化氢的分解速率 |
| B.0~6min的平均反应速率;v(H2O2)=3.33×10-2mol•L-1•min-1 |
| C.反应2H2O2(aq)=2H2O(l)+O2(g)的△H=E1-E2<0 |
| D.反应①是吸热反应、反应②是放热反应 |
您最近一年使用:0次
2022-11-16更新
|
427次组卷
|
32卷引用:北京市中国人民大学附属中学2021-2022学年高一下学期期末考试化学试题
北京市中国人民大学附属中学2021-2022学年高一下学期期末考试化学试题江苏省徐州市邳州市运河中学2020-2021学年高一下学期期中考试(普通班)化学试题河南省重点高中2021-2022学年高二下学期阶段性调研联考一化学试题浙江省嘉兴市2021-2022学年高二下学期期末检测化学试题山东省莱州一中2022-2023学年高二上学期第一次月考化学试题天津市部分区2022-2023学年高三上学期期中考试化学试题 天津市武清区2022-2023学年高三上学期11月期中化学试题北京市海淀区2018届高三上学期期中考试化学试题山东省师范大学附属中学2018届高三第三次模拟考试化学试题山东师范大学附属中学2018届高三上学期第三次模拟考试化学试题四川省德阳市三校2018届高三联合测试化学试题河北省故城县高级中学2018届高三12月月考化学试题(已下线)2017-2018学年上学期期末复习备考之精准复习模拟题高二化学选修4(C卷)江西省莲塘一中、临川二中2018届高三上学期第一次联考化学试题(已下线)黄金30题系列 高三化学 小题易丢分(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】山东省枣庄市第八中学东校区2018届高三1月月考理科综合化学试题四川省攀枝花市2017-2018学年高二上学期调研检测化学试题【全国百强校】福建省泉州第五中学2017届高三上学期期中检测化学试题【全国百强校】北京市北京四中2019届高三上学期期中考试化学试题安徽省六安市第一中学2020届高三下学期自测卷(一)陕西省汉中市五校2020-2021学年高二上学期第一次月考化学试题山东省济南市济北中学2021届高三11月月考化学试题江西省南昌市第二中学2020-2021学年高二上学期第三次月考化学试题广东省梅州市2020-2021学年度高二上学期期末联考化学试题江西省抚州市黎川县第一中学2020-2021学年高二上学期第三次月考化学试题江西省宜春市奉新县第一中学2020-2021学年高二下学期第一次月考化学试题选择性必修1 专题2 第一单元综合训练(已下线)第18讲 化学反应速率(练) — 2022年高考化学一轮复习讲练测(新教材新高考)北京市中国农业大学附属中学2021-2022学年高三上学期开学考试化学试题黑龙江省鹤岗市第一中学2023-2024学年高二上学期开学考试化学试题(已下线)第1讲 化学反应速率及其影响因素
9 . 碳捕集技术是减少 排放的一种途径,下图所示可捕获和转化
排放的一种途径,下图所示可捕获和转化 ,减少排放并实现资源利用。反应①完成之后通入
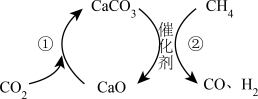
,减少排放并实现资源利用。反应①完成之后通入 ,反应过程中在催化剂上有积碳。下列说法错误的是
,反应过程中在催化剂上有积碳。下列说法错误的是
 排放的一种途径,下图所示可捕获和转化
排放的一种途径,下图所示可捕获和转化 ,减少排放并实现资源利用。反应①完成之后通入
,减少排放并实现资源利用。反应①完成之后通入 ,反应过程中在催化剂上有积碳。下列说法错误的是
,反应过程中在催化剂上有积碳。下列说法错误的是
| A.反应①属于化合反应 |
| B.反应过程中需添加CaO |
C.反应②的化学方程式为 |
D.反应②过程中可能有反应 发生 发生 |
您最近一年使用:0次
2022-11-13更新
|
155次组卷
|
2卷引用:山东省日照市2022-2023学年高一上学期期中校际联考化学试题
10 . 以黄铜矿[主要成分是二硫化亚铁铜( )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
Ⅰ.火法炼铜: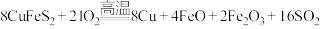
(1)反应中被还原的元素是_______ (填元素符号),氧化产物有_______ (填化学式)。
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为_______ ,冶炼过程中产生大量 ,下列处理方案中合理的是
,下列处理方案中合理的是_______ (填字母)。
A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成。
生成。
(3)配平该反应方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______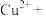 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是_______ 。
 )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。Ⅰ.火法炼铜:
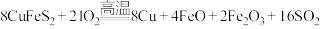
(1)反应中被还原的元素是
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为
 ,下列处理方案中合理的是
,下列处理方案中合理的是A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成。
生成。(3)配平该反应方程式:
_______
 _______
_______ _______
_______ _______
_______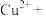 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是
您最近一年使用:0次
2022-11-06更新
|
301次组卷
|
2卷引用:辽宁省沈阳市市级重点高中联合体2022-2023学年高一上学期期中测试化学试题



