2023高三·全国·专题练习
解题方法
1 . 碳酸二甲酯DMC( )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
)是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
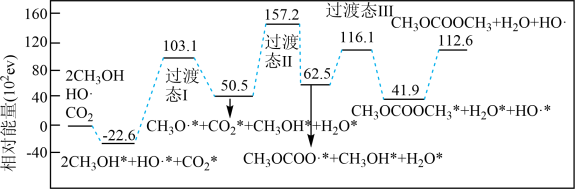
下列说法错误的是
 )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
)是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是
| A.HO·提高了反应的活化能 |
| B.过程CH3OH*+HO·*=CH3O·*+H2O*是该反应的决速步骤 |
| C.过程中既有H-O键的断裂,又有H-O键的形成 |
| D.吸附和脱附过程中共吸收1.126×104 eV的能量 |
您最近一年使用:0次
2023高三·全国·专题练习
2 . 硼氢化钠( )是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
)是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
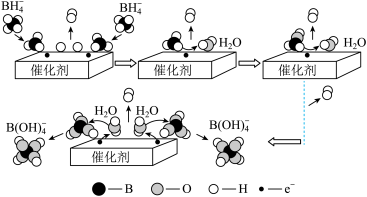
 )是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
)是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
| A.转化过程中,氢元素的化合价有−1价、0价和+1价 |
B. → → 过程中,有化学键的断裂,没有化学键的形成 过程中,有化学键的断裂,没有化学键的形成 |
C.总反应的实质为 中−1价氢与 中−1价氢与 中的+1价氢发生氧化还原反应生成氢气 中的+1价氢发生氧化还原反应生成氢气 |
| D.整个过程中出现了2种含硼微粒 |
您最近一年使用:0次
2023高三·全国·专题练习
3 . 我国在汽车尾气和燃煤尾气的净化方面取得了一定成效。汽车尾气净化的主要原理为 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。

(1) 温度下,
温度下, 内的平均反应速率
内的平均反应速率
___________ 。
(2)当固体催化剂的质量一定时,将催化剂磨成粉末,则反应速率___________ (填“增大”“减小”或“不变”,下同), 转化率
转化率___________ 。
(3)若在绝热、恒容的密闭体系中充入一定量的 和
和 气体进行该反应,下列示意图正确且能说明反应在进行到
气体进行该反应,下列示意图正确且能说明反应在进行到 时刻达到平衡状态的是
时刻达到平衡状态的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
(1)
 温度下,
温度下, 内的平均反应速率
内的平均反应速率
(2)当固体催化剂的质量一定时,将催化剂磨成粉末,则反应速率
 转化率
转化率(3)若在绝热、恒容的密闭体系中充入一定量的
 和
和 气体进行该反应,下列示意图正确且能说明反应在进行到
气体进行该反应,下列示意图正确且能说明反应在进行到 时刻达到平衡状态的是
时刻达到平衡状态的是a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2023高三·全国·专题练习
4 . 化学反应都伴随着能量的变化。回答下列问题:
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
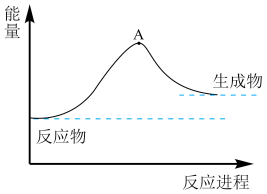
(2)一种分解海水制氢气的方法为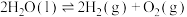 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将_______ (填“升高”、“降低”或“不变”)。
(3)已知: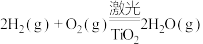
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:
由此计算x=___________ 。(用含a、c、d的代数式表示)
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
A. | B. |
C. | D.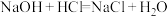 |
(2)一种分解海水制氢气的方法为
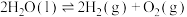 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将
(3)已知:
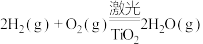
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:| 化学键 |  |  |  |
 | x | c | d |
您最近一年使用:0次
2023高三·全国·专题练习
5 . 近日,中国科学院化学物理研究所李灿院士团队揭示催化剂(Co3O4)上催化水氧化产氧历程如图所示(注明: s、ms、μs表示秒、毫秒、微秒)。下列叙述错误的是
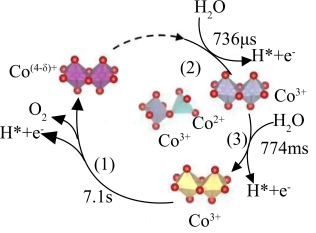

| A.第(1)步反应为总反应的控速反应 |
| B.Co原子价电子排布式为3d74s2,位于周期表中第四周期第Ⅷ族 |
| C.从总反应看,每生成标况22.4LO2必转移3mol 电子 |
| D.该反应过程中三步都断裂了极性键 |
您最近一年使用:0次
2023高三·全国·专题练习
6 . 绿色能源是未来能源发展的方向,积极发展氢能,是实现“碳达峰、碳中和”的重要举措。回答下列问题:
(1)通过生物柴油副产物甘油制取H2正成为绿色能源的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应如下(K1、K2分别为反应I、Ⅱ的化学平衡常数):
I.C3H8O3(g)⇌3CO(g)+4H2(g) ΔH1=+251kJ·mol-1 K1
Ⅱ.CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2=-41kJ·mol-1 K2
重整总反应C3H8O3(g)+3H2O(g)⇌3CO2(g)+7H2(g)的ΔH3=_________ ,平衡常数K3=_________ 。(用含K1、K2的计算式表示)
(2)大量研究表明Pt12Ni、Sn12Ni、Cu12Ni三种双金属合金团簇均可用于催化DRM反应(CH4+CO2⇌2CO+2H2),在催化剂表面涉及多个基元反应,其中甲烷逐步脱氢过程的能量变化如图甲所示(吸附在催化剂表面上的物种用*标注,TS1、TS2、TS3、TS4分别表示过渡态1、过渡态2、过渡态3、过渡态4)。
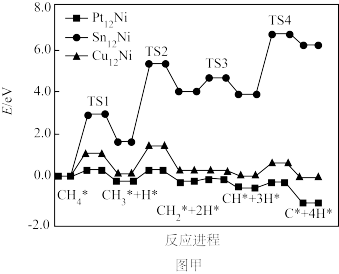
①Pt12Ni、Sn12Ni、Cu12Ni催化甲烷逐步脱氢过程的速率分别为v1、v2、v3,则脱氢过程的速率由小到大的关系为___________ 。
②甲烷逐步脱氢过程中,决定速率快慢的反应步骤是:___________ (用化学方程式表示)。
(3)甲烷干法重整制H2的过程为反应a:CH4+CO2⇌2CO+2H2,同时发生副反应b:CO2+H2⇌CO+H2O,T℃时,在恒压容器中,通入2molCH4和2molCO2发生上述反应,总压强为P0,平衡时甲烷的转化率为40%,H2O的分压为P,则反应a的压强平衡常数Kp=___________ (用含P和P0的计算式表示,已知分压=总压×物质的量分数)。
(4)甲烷裂解制氢的反应为CH4(g)=C(s)+2H2(g) ΔH=+75kJ·mol-1,Ni可作该反应的催化剂,CH4在催化剂孔道表面反应时,若孔道堵塞会导致催化剂失活。其他条件相同时,随时间增加,温度对Ni催化剂催化效果的影响如图乙所示。考虑综合因素,使用催化剂的最佳温度为___________ ;650℃条件下,1000s后,氢气的体积分数快速下降的原因是___________ 。

(1)通过生物柴油副产物甘油制取H2正成为绿色能源的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应如下(K1、K2分别为反应I、Ⅱ的化学平衡常数):
I.C3H8O3(g)⇌3CO(g)+4H2(g) ΔH1=+251kJ·mol-1 K1
Ⅱ.CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2=-41kJ·mol-1 K2
重整总反应C3H8O3(g)+3H2O(g)⇌3CO2(g)+7H2(g)的ΔH3=
(2)大量研究表明Pt12Ni、Sn12Ni、Cu12Ni三种双金属合金团簇均可用于催化DRM反应(CH4+CO2⇌2CO+2H2),在催化剂表面涉及多个基元反应,其中甲烷逐步脱氢过程的能量变化如图甲所示(吸附在催化剂表面上的物种用*标注,TS1、TS2、TS3、TS4分别表示过渡态1、过渡态2、过渡态3、过渡态4)。

①Pt12Ni、Sn12Ni、Cu12Ni催化甲烷逐步脱氢过程的速率分别为v1、v2、v3,则脱氢过程的速率由小到大的关系为
②甲烷逐步脱氢过程中,决定速率快慢的反应步骤是:
(3)甲烷干法重整制H2的过程为反应a:CH4+CO2⇌2CO+2H2,同时发生副反应b:CO2+H2⇌CO+H2O,T℃时,在恒压容器中,通入2molCH4和2molCO2发生上述反应,总压强为P0,平衡时甲烷的转化率为40%,H2O的分压为P,则反应a的压强平衡常数Kp=
(4)甲烷裂解制氢的反应为CH4(g)=C(s)+2H2(g) ΔH=+75kJ·mol-1,Ni可作该反应的催化剂,CH4在催化剂孔道表面反应时,若孔道堵塞会导致催化剂失活。其他条件相同时,随时间增加,温度对Ni催化剂催化效果的影响如图乙所示。考虑综合因素,使用催化剂的最佳温度为

您最近一年使用:0次
2023高三·全国·专题练习
7 . 甲苯(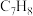 )和二甲苯(
)和二甲苯(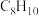 )是重要的化工原料。利用苯(
)是重要的化工原料。利用苯(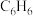 )和甲醇(
)和甲醇( )在催化剂作用下反应得到
)在催化剂作用下反应得到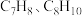 和副产物三甲苯(
和副产物三甲苯(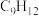 ),发生的主要反应如下:
),发生的主要反应如下:
Ⅰ.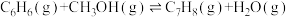
Ⅱ.
Ⅲ.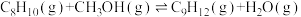
(1)500℃、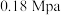 条件下,反应达到平衡时,结果如图所示。
条件下,反应达到平衡时,结果如图所示。

①由图分析,随着投料比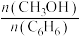 增加,
增加, 的平衡转化率
的平衡转化率___________ 。平衡时 的值
的值___________ (填“增大”、“减小”或“不变”)。
②投料比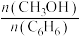 为1.0时,
为1.0时, 的平衡转化率为50%,产物中
的平衡转化率为50%,产物中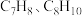 和
和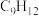 物质的量之比为6:3:1,
物质的量之比为6:3:1, 的平衡转化率为
的平衡转化率为___________ ,反应Ⅰ的平衡常数
___________ 。
(2)我国学者结合实验与计算机模拟结果,研究了反应Ⅰ在固体酸(HB)催化剂表面进行的反应历程如图所示,其中吸附在固体酸(HB)表面的物种用*标注。

①反应Ⅰ的
______ 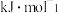 。
。
②吸附 的焓变
的焓变______ 吸附 的焓变(填“>”或“<”)。
的焓变(填“>”或“<”)。
③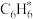 在催化剂表面转化为
在催化剂表面转化为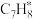 的反应方程式为
的反应方程式为______ 。
④在固体酸(HB)催化作用下,测得反应Ⅰ的速率方程为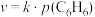 (
(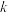 为速率常数)。在刚性容器中发生反应Ⅰ,关于反应Ⅰ的平衡常数(K)和反应速率(υ)的叙述正确的是
为速率常数)。在刚性容器中发生反应Ⅰ,关于反应Ⅰ的平衡常数(K)和反应速率(υ)的叙述正确的是______ (填标号)。
A.升高温度,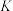 和
和 均增大 B.增大
均增大 B.增大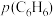 ,
,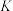 不变,
不变, 增大
增大
C.降低温度,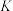 和
和 均增大 D.增大
均增大 D.增大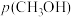 ,
,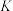 不变,
不变, 增大
增大
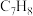 )和二甲苯(
)和二甲苯(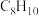 )是重要的化工原料。利用苯(
)是重要的化工原料。利用苯(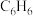 )和甲醇(
)和甲醇( )在催化剂作用下反应得到
)在催化剂作用下反应得到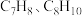 和副产物三甲苯(
和副产物三甲苯(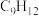 ),发生的主要反应如下:
),发生的主要反应如下:Ⅰ.
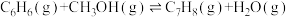
Ⅱ.

Ⅲ.
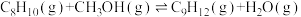
(1)500℃、
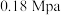 条件下,反应达到平衡时,结果如图所示。
条件下,反应达到平衡时,结果如图所示。
①由图分析,随着投料比
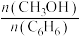 增加,
增加, 的平衡转化率
的平衡转化率 的值
的值②投料比
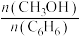 为1.0时,
为1.0时, 的平衡转化率为50%,产物中
的平衡转化率为50%,产物中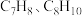 和
和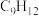 物质的量之比为6:3:1,
物质的量之比为6:3:1, 的平衡转化率为
的平衡转化率为
(2)我国学者结合实验与计算机模拟结果,研究了反应Ⅰ在固体酸(HB)催化剂表面进行的反应历程如图所示,其中吸附在固体酸(HB)表面的物种用*标注。

①反应Ⅰ的

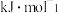 。
。②吸附
 的焓变
的焓变 的焓变(填“>”或“<”)。
的焓变(填“>”或“<”)。③
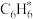 在催化剂表面转化为
在催化剂表面转化为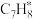 的反应方程式为
的反应方程式为④在固体酸(HB)催化作用下,测得反应Ⅰ的速率方程为
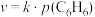 (
(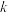 为速率常数)。在刚性容器中发生反应Ⅰ,关于反应Ⅰ的平衡常数(K)和反应速率(υ)的叙述正确的是
为速率常数)。在刚性容器中发生反应Ⅰ,关于反应Ⅰ的平衡常数(K)和反应速率(υ)的叙述正确的是A.升高温度,
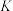 和
和 均增大 B.增大
均增大 B.增大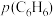 ,
,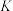 不变,
不变, 增大
增大C.降低温度,
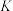 和
和 均增大 D.增大
均增大 D.增大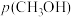 ,
,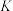 不变,
不变, 增大
增大
您最近一年使用:0次
2023高三·全国·专题练习
8 . 下列关于化学反应的调控措施说法不正确 的是________ 。
A.硫酸工业中,为使黄铁矿充分燃烧,可将矿石粉碎
B.硝酸工业中,氨的氧化使用催化剂是为了增大反应速率,提高生产效率
C.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
D.对于合成氨的反应,调控反应条件至最好,也不能使一种反应物的转化率达到100%
E.工业上增加炼铁高炉的高度可以有效降低尾气中CO的含量
F.合成氨工业中,从生产实际条件考虑,可盲目增大反应压强
G.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
A.硫酸工业中,为使黄铁矿充分燃烧,可将矿石粉碎
B.硝酸工业中,氨的氧化使用催化剂是为了增大反应速率,提高生产效率
C.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
D.对于合成氨的反应,调控反应条件至最好,也不能使一种反应物的转化率达到100%
E.工业上增加炼铁高炉的高度可以有效降低尾气中CO的含量
F.合成氨工业中,从生产实际条件考虑,可盲目增大反应压强
G.合成氨工业中,为提高氮气和氢气的利用率,采用循环操作
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . “氯化反应”一般指将氯元素引入化合物中的反应,一般包括置换氯化、加成氯化和氧化氯化。已知在制“氯乙烯反应”中, HC≡CH (g)+HCl(g) CH2=CHCl(g)的反应机理如图所示,下列说法正确的是
CH2=CHCl(g)的反应机理如图所示,下列说法正确的是

 CH2=CHCl(g)的反应机理如图所示,下列说法正确的是
CH2=CHCl(g)的反应机理如图所示,下列说法正确的是
| A.碳碳叁键的键能:M1大于CH≡CH |
| B.由题图可知M2→M3的变化过程是热能转变成化学能的过程 |
| C.该氯乙烯反应的总反应速率取决于M2→M3的反应速率 |
| D.HgCl2是“氯化反应”的催化剂,不会参与反应的过程 |
您最近一年使用:0次
2023高三·全国·专题练习
10 . 2SO2(g)+O2(g) 2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
 2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是| A.该反应速率主要由第②步基元反应决定 |
| B.由反应机理可知,V2O5是该反应的催化剂 |
| C.V2O5的存在提高了该反应活化能,使单位时间内有效碰撞次数增加,反应速率加快 |
| D.逆反应的活化能比正反应的活化能大198kJ•mol-1 |
您最近一年使用:0次



