1 . 由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一
反应②: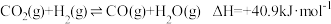
反应③: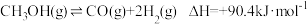
(1)反应①: 的
的
_______ 。
(2) 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。_______ 逆反应速率(填“>或<或=”)。
②下列叙述能说明上述反应能达到化学平衡状态的是_______ 。(填字母)。
a.3v(CO2)=v(H2) b. 的体积分数不再改变
的体积分数不再改变
c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后 2的平衡转化率降低的原因
2的平衡转化率降低的原因_______
(3)往一容积为 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与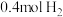 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是_______ ,则c点时 的体积分数是
的体积分数是_______ ;平衡后再加入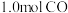 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率_______ (填“增大”或“不变”或“减小”)。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一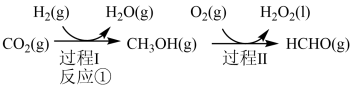
反应②:
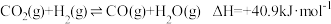
反应③:
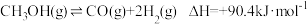
(1)反应①:
 的
的
(2)
 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。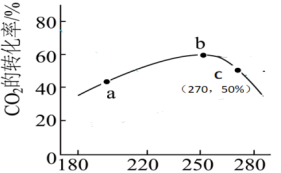
②下列叙述能说明上述反应能达到化学平衡状态的是
a.3v(CO2)=v(H2) b.
 的体积分数不再改变
的体积分数不再改变c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后
 2的平衡转化率降低的原因
2的平衡转化率降低的原因(3)往一容积为
 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与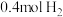 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是 的体积分数是
的体积分数是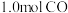 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率
您最近一年使用:0次
2 . 下列事实不能用勒夏特列原理解释的是
| A.使用新型催化剂可使氮气与氢气在常温常压下合成氨气 |
| B.用排饱和食盐水的方法收集氯气 |
C. 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| D.石灰石与稀盐酸在密闭瓶中反应结束后,打开瓶塞,溶液中有气泡产生 |
您最近一年使用:0次
3 . 在密闭容器中发生反应:xA(g)+yB(g)  zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
 zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是| A.x+y<z | B.平衡向正反应方向移动 | C.C的体积分数增大 | D.B的转化率降低 |
您最近一年使用:0次
4 . 目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。___________ 。
(2)温度降低,平衡常数K___________ (填“增大”、“不变”或“减小”)。
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率 (H2)为
(H2)为____________ mol·L-1·min-1, CO2和H2的转化率比是___________ 。___________ 。
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。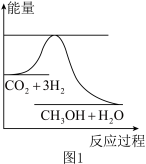
(2)温度降低,平衡常数K
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率
 (H2)为
(H2)为
您最近一年使用:0次
12-13高二上·吉林长春·期末
名校
解题方法
5 . 已知某可逆反应mA(g)+nB(g)⇌pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数φ(B)的关系曲线,由曲线分析,下列判断正确的是
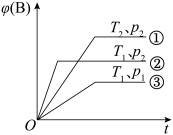
| A.T1<T2,p1>p2,m+n>p,放热反应 |
| B.T1>T2,p1<p2,m+n>p,吸热反应 |
| C.T1<T2,p1>p2,m+n<p,放热反应 |
| D.T1>T2,p1<p2,m+n<p,吸热反应 |
您最近一年使用:0次
2023-07-28更新
|
244次组卷
|
50卷引用:新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二上学期11月阶段性检测化学试题
新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二上学期11月阶段性检测化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题2016-2017学年吉林省汪清六中高二上第一次月考化学试卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷2016-2017学年江西省上高二中高二上10月月考化学试卷2016-2017学年湖北省鄂东南部分重点中学高二2月联考化学试卷河北省武邑中学2017-2018学年高二上学期第一次月考化学试题河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第一次月考化学试题四川省广安市友谊中学2018-2019学年高二上学期九月月考化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高二上学期9月月考化学试题新疆维吾尔自治区昌吉市第九中学2018-2019学年高二上学期期末考试化学试题江苏省常州礼嘉中学2018-2019学年高二6月月考化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(A)甘肃省静宁县第一中学2019-2020学年高二上学期第一次月考化学试题湖北省黄冈市浠水县实验高级中学2019-2020学年高二上学期9月份月考化学试题江西省赣州市寻乌中学2019-2020学年高二上学期第一次段考化学试题新疆阿克苏市实验中学2019-2020学年高二上学期期末考试化学试题贵州省贵阳市第三实验中学2019-2020学年高二上学期第一次月考化学试题河南省三门峡市第一高级中学2020-2021学年高二上学期9月月考化学试题内蒙古包头市第四中学2020-2021学年高二上学期第一次月考化学试题湖南省永州市祁阳县第四中学2023-2024学年高二上学期10月月考化学试题(已下线)2011-2012学年吉林省长春外国语学校高二上学期期末考试化学试卷(已下线)2011-2012学年内蒙古包头三十三中高二上学期期末考试化学试卷(已下线)2011-2012学年四川省成都市六校协作体高二下学期期中联考化学试卷2015-2016学年湖南省株洲十八中高二上学期期中(理)化学试卷2015-2016学年江西省赣州市高二上学期期末考试化学试卷2015-2016学年甘肃省嘉峪关市第一中学高二上学期期末化学试卷2015-2016学年河南省孟津一中高二上学期期末化学试卷2016-2017学年云南省玉溪一中高二上期中化学卷湖北省监利县实验高中2017-2018学年高二上学期期中考试化学试题【全国百强校】甘肃省会宁县第一中学2018-2019学年高二(理科)上学期期中考试化学试题山西省吕梁市高级中学2018-2019学年高二上学期期中考试化学试题贵州省安顺市平坝第一高级中学2018-2019学年高二上学期期中考试化学试题吉林省白城市第一中学2018-2019学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2019-2020学年高二上学期开学考试(8月)化学试题吉林省吉化第一高级中学校2019-2020学年高二9月月考化学试题贵州省安顺市平坝第一高级中学2019-2020学年高二上学期期中考试化学试题广东省潮州市潮安区颜锡祺中学2019-2020学年高二上学期期中考试化学试题湖北省武汉市钢城第四中学2019-2020学年高二上学期期中考试化学试题广西柳州市柳江中学2019-2020学年高二上学期期中考试化学(理)试题湖北省鄂州市泽林高中2019-2020学年高二上学期期末联考化学试题吉林省长春市兴华中学2019-2020学年高二上学期期末考试化学试题安徽省枞阳县浮山中学2019-2020学年高二下学期开学考试化学试题(已下线)四川省棠湖中学2018-2019学年高二上学期期末模拟理综-化学试题安徽省蚌埠第三中学2019-2020学年高二上学期期中考试化学试题甘肃省武威第一中学2020-2021学年高二上学期期中考试化学试题微专题(四)——化学平衡状态的判定云南省西双版纳傣族自治州第一中学2022-2023学年高二下学期期末考试化学试题(已下线)第4讲 化学反应速率及平衡图像
6 . 在一定条件下,反应:2SO2(g)+O2(g) 2SO3(g)达到了平衡,改变某一条件,发生下述变化,其中可确定该平衡一定发生移动的是
2SO3(g)达到了平衡,改变某一条件,发生下述变化,其中可确定该平衡一定发生移动的是
 2SO3(g)达到了平衡,改变某一条件,发生下述变化,其中可确定该平衡一定发生移动的是
2SO3(g)达到了平衡,改变某一条件,发生下述变化,其中可确定该平衡一定发生移动的是| A.O2的百分含量发生变化 | B.SO3的密度不变 |
| C.v(SO2)增大 | D.v(SO3)减小 |
您最近一年使用:0次
7 . 完成下列问题:
Ⅰ.将5 mL0.005 mol•L-1的FeCl3溶液与5 mL0.01 mol•L-1的KSCN溶液混合,建立平衡:FeCl3+3KSCN 3KCl+Fe(SCN)3(红色)。
3KCl+Fe(SCN)3(红色)。
(1)若滴加1 mol•L-1KSCN溶液4滴,平衡向___________ 方向移动,溶液红色___________ 。
(2)若加入少量KCl固体,则平衡___________ 移动(填“正向”、“逆向”或“不”)。
Ⅱ.利用反应CO(g)+H2O(g) H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。
(3)该反应化学平衡常数表达式K=___________ 。
(4)该反应的平衡常数随温度的变化如表:
从上表可以推断:此反应是___________ (填“吸热”或“放热”)反应。
(5)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol,2min内v(CO2)=___________ ,此时反应进行的方向是___________ ,(填正向进行或逆向进行)依据是___________ ,可以判断该反应达到平衡的标志是___________ (填字母)。
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
Ⅰ.将5 mL0.005 mol•L-1的FeCl3溶液与5 mL0.01 mol•L-1的KSCN溶液混合,建立平衡:FeCl3+3KSCN
 3KCl+Fe(SCN)3(红色)。
3KCl+Fe(SCN)3(红色)。(1)若滴加1 mol•L-1KSCN溶液4滴,平衡向
(2)若加入少量KCl固体,则平衡
Ⅱ.利用反应CO(g)+H2O(g)
 H2(g)+CO2(g)可得到清洁能源H2。
H2(g)+CO2(g)可得到清洁能源H2。(3)该反应化学平衡常数表达式K=
(4)该反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(5)830℃时,向容积为2L的密闭容器中充入1molCO与1molH2O,2min时CO为0.6mol,2min内v(CO2)=
a.体系的压强不再发生变化 b.混合气体的密度不变
c.CO的消耗速率与CO2的消耗速率相等 d.各组分的物质的量浓度不再改变
您最近一年使用:0次
8 . 密闭容器中进行的可逆反应:aA(g)+bB(g) cC(g)+dD(s)在不同温度(
cC(g)+dD(s)在不同温度( 和
和 )及压强(
)及压强( 和
和 )下,混合气体中B的体积分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是
)下,混合气体中B的体积分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是

 cC(g)+dD(s)在不同温度(
cC(g)+dD(s)在不同温度( 和
和 )及压强(
)及压强( 和
和 )下,混合气体中B的体积分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是
)下,混合气体中B的体积分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是
A. ,a+b>c+d,正反应为放热反应 ,a+b>c+d,正反应为放热反应 |
B. ,a+b ,a+b c+d,正反应为吸热反应 c+d,正反应为吸热反应 |
C. ,a+b ,a+b c,正反应为吸热反应 c,正反应为吸热反应 |
D. ,a+b>c,正反应为放热反应 ,a+b>c,正反应为放热反应 |
您最近一年使用:0次
2022-11-30更新
|
116次组卷
|
2卷引用:新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题
名校
9 . 请回答下列问题。
I.在一定体积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_______ 。
(2)该反应的逆反应为_______ (填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式: ,试判断此时的温度为
,试判断此时的温度为_______ ℃。此温度下加入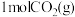 和
和 ,充分反应,达到平衡时,CO2的转化率为
,充分反应,达到平衡时,CO2的转化率为_______ 。
(4)在 时,发生上述反应,某一时刻测得容器内各物质的浓度分别为
时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 为
为 ,
, 为
为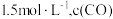 为
为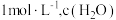 为
为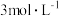 ,则此时平衡
,则此时平衡_______ (填“向左移动”“向右移动”或“不移动”)。
II.可将炼铁产生的 与
与 反应得到气体燃料,其反应原理为:
反应得到气体燃料,其反应原理为: 。某小组向体积是
。某小组向体积是 的刚性密闭容器中充入物质的量均是
的刚性密闭容器中充入物质的量均是 的
的 与
与 ,反应过程中
,反应过程中 的平衡转化率与温度、压强的关系如图所示。
的平衡转化率与温度、压强的关系如图所示。

(5)压强:p1______ p2(填“ ”或“
”或“ ”)。
”)。
(6)1100℃、p1条件下,反应经 达到平衡,则平均反应速率
达到平衡,则平均反应速率
_______  。反应的平衡常数Kp=
。反应的平衡常数Kp=________ (用含 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压
为以分压表示的平衡常数,分压 总压
总压 物质的量分数);若在平衡体系再充入
物质的量分数);若在平衡体系再充入 和
和 ,重新达平衡后,
,重新达平衡后, 的转化率
的转化率_______ (选填“增大”、“减小”或“不变”)。
I.在一定体积的密闭容器中,进行如下化学反应:
 ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示: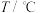 | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 2 | 4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应的逆反应为
(3)某温度下,平衡浓度符合下式:
 ,试判断此时的温度为
,试判断此时的温度为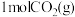 和
和 ,充分反应,达到平衡时,CO2的转化率为
,充分反应,达到平衡时,CO2的转化率为(4)在
 时,发生上述反应,某一时刻测得容器内各物质的浓度分别为
时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 为
为 ,
, 为
为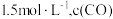 为
为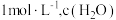 为
为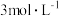 ,则此时平衡
,则此时平衡II.可将炼铁产生的
 与
与 反应得到气体燃料,其反应原理为:
反应得到气体燃料,其反应原理为: 。某小组向体积是
。某小组向体积是 的刚性密闭容器中充入物质的量均是
的刚性密闭容器中充入物质的量均是 的
的 与
与 ,反应过程中
,反应过程中 的平衡转化率与温度、压强的关系如图所示。
的平衡转化率与温度、压强的关系如图所示。
(5)压强:p1
 ”或“
”或“ ”)。
”)。(6)1100℃、p1条件下,反应经
 达到平衡,则平均反应速率
达到平衡,则平均反应速率
 。反应的平衡常数Kp=
。反应的平衡常数Kp= 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压
为以分压表示的平衡常数,分压 总压
总压 物质的量分数);若在平衡体系再充入
物质的量分数);若在平衡体系再充入 和
和 ,重新达平衡后,
,重新达平衡后, 的转化率
的转化率
您最近一年使用:0次
名校
解题方法
10 . 工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应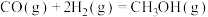 。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol
。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol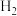 和一定量的CO后,CO和
和一定量的CO后,CO和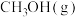 的浓度随时间变化。
的浓度随时间变化。
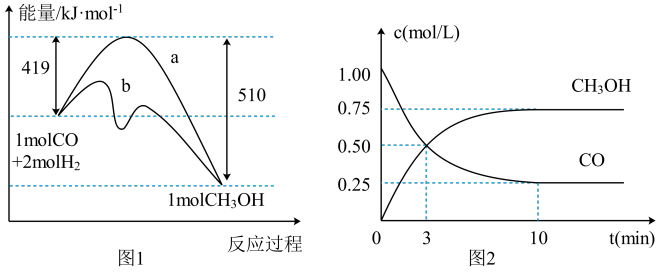
请回答下列问题:
(1)在“图1”中,曲线_______ (填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应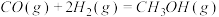 的
的
_______ 。
(2)下列说法正确的是_______ 。
A.起始充入的CO的物质的量为1mol
B.增加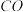 的浓度,
的浓度,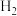 的转化率会增大
的转化率会增大
C.反应时间为3分钟时,反应达到平衡状态
(3)从反应开始到建立平衡,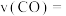
_______ ;达到平衡时,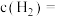
_______ ,该温度下 的化学平衡常数为
的化学平衡常数为_______ 。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡_______ 移动(填“正向”、“逆向”或“不”)。
(4)已知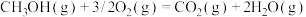
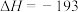 kJ/mol。又知
kJ/mol。又知 ;
; kJ/mol,请写出32g的
kJ/mol,请写出32g的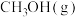
完全燃烧生成液态水的热化学方程式_______ 。
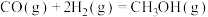 。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol
。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol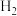 和一定量的CO后,CO和
和一定量的CO后,CO和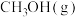 的浓度随时间变化。
的浓度随时间变化。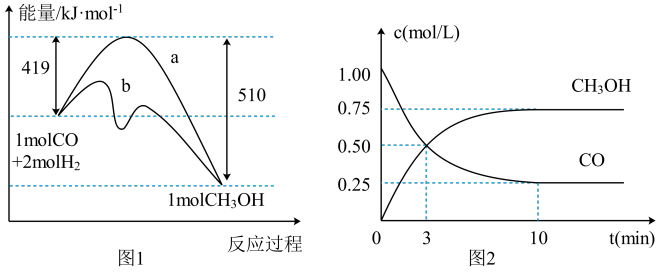
请回答下列问题:
(1)在“图1”中,曲线
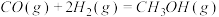 的
的
(2)下列说法正确的是
A.起始充入的CO的物质的量为1mol
B.增加
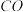 的浓度,
的浓度,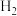 的转化率会增大
的转化率会增大C.反应时间为3分钟时,反应达到平衡状态
(3)从反应开始到建立平衡,
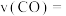
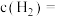
 的化学平衡常数为
的化学平衡常数为(4)已知
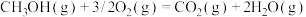
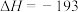 kJ/mol。又知
kJ/mol。又知 ;
; kJ/mol,请写出32g的
kJ/mol,请写出32g的
完全燃烧生成液态水的热化学方程式
您最近一年使用:0次



