1 . 298K时,向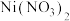 、
、 、
、 的混合液中滴加KCN溶液,混合液中lgx与
的混合液中滴加KCN溶液,混合液中lgx与 的关系如图所示,
的关系如图所示, 或
或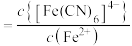 或
或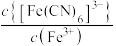 。下列叙述不正确的是
。下列叙述不正确的是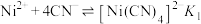 ;
;
(2) ;
;
(3)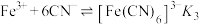 ,且
,且 。
。
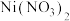 、
、 、
、 的混合液中滴加KCN溶液,混合液中lgx与
的混合液中滴加KCN溶液,混合液中lgx与 的关系如图所示,
的关系如图所示, 或
或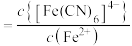 或
或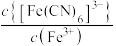 。下列叙述不正确的是
。下列叙述不正确的是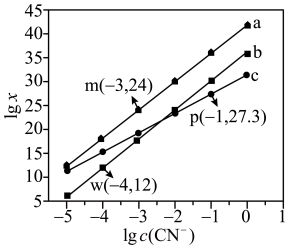
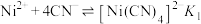 ;
;(2)
 ;
;(3)
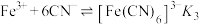 ,且
,且 。
。A.直线b代表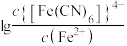 与 与 的关系 的关系 |
B.根据图像可计算平衡常数 数量级为 数量级为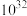 |
C. 的平衡常数 的平衡常数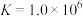 |
D.向含相同浓度的 和 和 的溶液中滴加 的溶液中滴加 溶液,先生成 溶液,先生成 |
您最近一年使用:0次
7日内更新
|
45次组卷
|
2卷引用:2024届新疆高三下学期5月第三次适应性检测理综试卷-高中化学
解题方法
2 . 一种催化还原NO的机理如图所示,下列说法正确的是
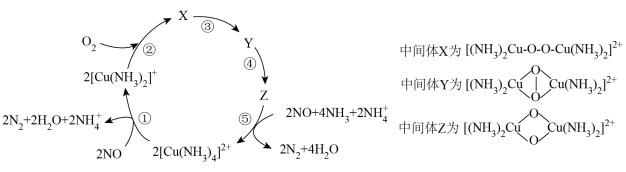

| A.中间体X和Z中O和Cu的化合价均不变 |
B.使用催化剂 ,可以提高NO的反应速率和平衡转化率 ,可以提高NO的反应速率和平衡转化率 |
| C.过程①中既有极性键的断裂,也有极性键的形成 |
D.该催化还原过程的总反应方程式为 |
您最近一年使用:0次
7日内更新
|
43次组卷
|
2卷引用:2024届新疆高三下学期5月第三次适应性检测理综试卷-高中化学
3 . 由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一
反应②: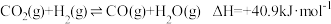
反应③: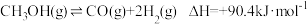
(1)反应①: 的
的
_______ 。
(2) 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。_______ 逆反应速率(填“>或<或=”)。
②下列叙述能说明上述反应能达到化学平衡状态的是_______ 。(填字母)。
a.3v(CO2)=v(H2) b. 的体积分数不再改变
的体积分数不再改变
c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后 2的平衡转化率降低的原因
2的平衡转化率降低的原因_______
(3)往一容积为 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与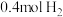 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是_______ ,则c点时 的体积分数是
的体积分数是_______ ;平衡后再加入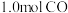 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率_______ (填“增大”或“不变”或“减小”)。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一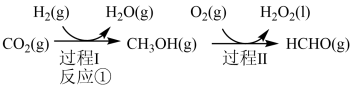
反应②:
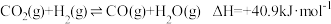
反应③:
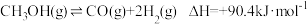
(1)反应①:
 的
的
(2)
 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。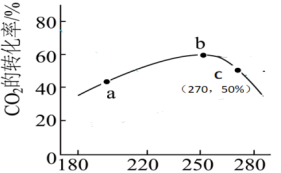
②下列叙述能说明上述反应能达到化学平衡状态的是
a.3v(CO2)=v(H2) b.
 的体积分数不再改变
的体积分数不再改变c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后
 2的平衡转化率降低的原因
2的平衡转化率降低的原因(3)往一容积为
 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与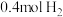 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是 的体积分数是
的体积分数是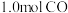 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率
您最近一年使用:0次
4 . 下列事实不能用勒夏特列原理解释的是
| A.使用新型催化剂可使氮气与氢气在常温常压下合成氨气 |
| B.用排饱和食盐水的方法收集氯气 |
C. 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| D.石灰石与稀盐酸在密闭瓶中反应结束后,打开瓶塞,溶液中有气泡产生 |
您最近一年使用:0次
5 . 在密闭容器中发生反应:xA(g)+yB(g)  zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
 zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是| A.x+y<z | B.平衡向正反应方向移动 | C.C的体积分数增大 | D.B的转化率降低 |
您最近一年使用:0次
6 . 目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。___________ 。
(2)温度降低,平衡常数K___________ (填“增大”、“不变”或“减小”)。
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率 (H2)为
(H2)为____________ mol·L-1·min-1, CO2和H2的转化率比是___________ 。___________ 。
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。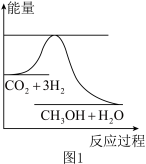
(2)温度降低,平衡常数K
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率
 (H2)为
(H2)为
您最近一年使用:0次
解题方法
7 . 水解平衡和其他化学平衡一样也是动态平衡,外界条件改变,平衡就会发生移动,以CH3COONa的水解为例( )填写下表(填写“增大”,“减小”,“不变”等)
)填写下表(填写“增大”,“减小”,“不变”等)
 )填写下表(填写“增大”,“减小”,“不变”等)
)填写下表(填写“增大”,“减小”,“不变”等)| 条件 | c(CH3COO-) | c(CH3COOH) | c(OH-) | c(H+) | pH | 水解程度 |
| 升温 | ||||||
| 加H2O | ||||||
| 加NaOH(s) |
您最近一年使用:0次
8 . 合成氨时采用400-500℃左右的温度进行,主要是因为在该温度时
| A.合成氨的化学反应限度最大 | B.N2的转化率最高 |
| C.催化剂的活性最大 | D.NH3在平衡混合气体中的体积分数最大 |
您最近一年使用:0次
解题方法
9 . (Ⅰ)已知反应mA(g)+nB(g) pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
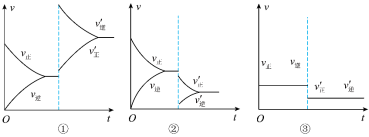
回答下列问题:
(1)①表示改变压强的方式是___________ (填“增大”或“减小”)压强,m+n___________ p+q(填“>”“<”或“=”)。
(2)②表示改变温度的方式是___________ (填“升高”或“降低”)温度,该反应的反应热ΔH___________ 0(填“>”“<”或“=”)。
(3)③表示改变压强,则m+n___________ p+q。
(Ⅱ)氨气是重要的化工原料,在国民经济中占重要地位。工业合成氨的反应为
 。回答下列问题:
。回答下列问题:
(4)图甲表示合成氨反应在某段时间 中反应速率与时间的曲线图,
中反应速率与时间的曲线图, 、
、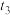 、
、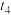 时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中,
时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是
的体积分数最小的一段时间是___________ (填字母)。
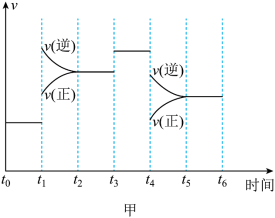
A. B.
B. C.
C. D.
D.
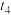 时刻改变的条件是
时刻改变的条件是___________ 。
 pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
回答下列问题:
(1)①表示改变压强的方式是
(2)②表示改变温度的方式是
(3)③表示改变压强,则m+n
(Ⅱ)氨气是重要的化工原料,在国民经济中占重要地位。工业合成氨的反应为

 。回答下列问题:
。回答下列问题:(4)图甲表示合成氨反应在某段时间
 中反应速率与时间的曲线图,
中反应速率与时间的曲线图, 、
、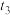 、
、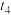 时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中,
时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是
的体积分数最小的一段时间是
A.
 B.
B. C.
C. D.
D.
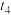 时刻改变的条件是
时刻改变的条件是
您最近一年使用:0次
10 . 下列过程中的颜色变化不能用勒夏特列原理解释的是
A.向5mL0.1mol•L-1重铬酸钾溶液中(存在平衡: (橙色)+H2O⇌2 (橙色)+H2O⇌2 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 |
| B.对2NO2(g)⇌N2O4(g)平衡体系增大压强(缩小体积)的瞬间,气体的颜色变深 |
| C.将NO2球浸泡在热水中,红棕色变深 |
| D.溴水中有平衡:Br2+H2O⇌HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 |
您最近一年使用:0次



