1 . 由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一
反应②: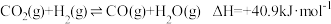
反应③: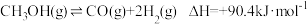
(1)反应①: 的
的
_______ 。
(2) 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。_______ 逆反应速率(填“>或<或=”)。
②下列叙述能说明上述反应能达到化学平衡状态的是_______ 。(填字母)。
a.3v(CO2)=v(H2) b. 的体积分数不再改变
的体积分数不再改变
c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后 2的平衡转化率降低的原因
2的平衡转化率降低的原因_______
(3)往一容积为 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与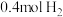 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是_______ ,则c点时 的体积分数是
的体积分数是_______ ;平衡后再加入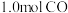 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率_______ (填“增大”或“不变”或“减小”)。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一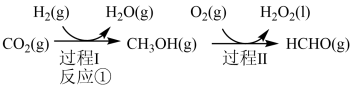
反应②:
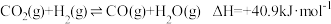
反应③:
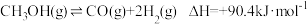
(1)反应①:
 的
的
(2)
 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。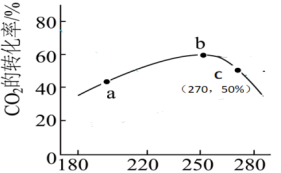
②下列叙述能说明上述反应能达到化学平衡状态的是
a.3v(CO2)=v(H2) b.
 的体积分数不再改变
的体积分数不再改变c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后
 2的平衡转化率降低的原因
2的平衡转化率降低的原因(3)往一容积为
 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与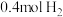 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是 的体积分数是
的体积分数是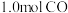 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率
您最近一年使用:0次
2 . 下列事实不能用勒夏特列原理解释的是
| A.使用新型催化剂可使氮气与氢气在常温常压下合成氨气 |
| B.用排饱和食盐水的方法收集氯气 |
C. 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| D.石灰石与稀盐酸在密闭瓶中反应结束后,打开瓶塞,溶液中有气泡产生 |
您最近一年使用:0次
3 . 在密闭容器中发生反应:xA(g)+yB(g)  zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
 zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是
zC(g)平衡时测得A的浓度为0.50mol•L-1保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol•L-1。下列判断正确的是| A.x+y<z | B.平衡向正反应方向移动 | C.C的体积分数增大 | D.B的转化率降低 |
您最近一年使用:0次
4 . 目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。___________ 。
(2)温度降低,平衡常数K___________ (填“增大”、“不变”或“减小”)。
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率 (H2)为
(H2)为____________ mol·L-1·min-1, CO2和H2的转化率比是___________ 。___________ 。
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。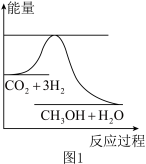
(2)温度降低,平衡常数K
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率
 (H2)为
(H2)为
您最近一年使用:0次
解题方法
5 . 水解平衡和其他化学平衡一样也是动态平衡,外界条件改变,平衡就会发生移动,以CH3COONa的水解为例( )填写下表(填写“增大”,“减小”,“不变”等)
)填写下表(填写“增大”,“减小”,“不变”等)
 )填写下表(填写“增大”,“减小”,“不变”等)
)填写下表(填写“增大”,“减小”,“不变”等)| 条件 | c(CH3COO-) | c(CH3COOH) | c(OH-) | c(H+) | pH | 水解程度 |
| 升温 | ||||||
| 加H2O | ||||||
| 加NaOH(s) |
您最近一年使用:0次
6 . 合成氨时采用400-500℃左右的温度进行,主要是因为在该温度时
| A.合成氨的化学反应限度最大 | B.N2的转化率最高 |
| C.催化剂的活性最大 | D.NH3在平衡混合气体中的体积分数最大 |
您最近一年使用:0次
解题方法
7 . (Ⅰ)已知反应mA(g)+nB(g) pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
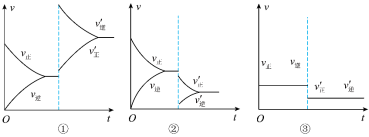
回答下列问题:
(1)①表示改变压强的方式是___________ (填“增大”或“减小”)压强,m+n___________ p+q(填“>”“<”或“=”)。
(2)②表示改变温度的方式是___________ (填“升高”或“降低”)温度,该反应的反应热ΔH___________ 0(填“>”“<”或“=”)。
(3)③表示改变压强,则m+n___________ p+q。
(Ⅱ)氨气是重要的化工原料,在国民经济中占重要地位。工业合成氨的反应为
 。回答下列问题:
。回答下列问题:
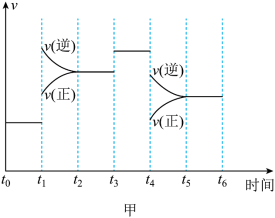
(4)图甲表示合成氨反应在某段时间 中反应速率与时间的曲线图,
中反应速率与时间的曲线图, 、
、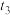 、
、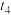 时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中,
时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是
的体积分数最小的一段时间是___________ (填字母)。
A. B.
B. C.
C. D.
D.
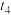 时刻改变的条件是
时刻改变的条件是___________ 。
 pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
pC(g)+qD(g),当反应达到平衡后,改变外界条件,其反应速率的变化曲线分别如图所示。
回答下列问题:
(1)①表示改变压强的方式是
(2)②表示改变温度的方式是
(3)③表示改变压强,则m+n
(Ⅱ)氨气是重要的化工原料,在国民经济中占重要地位。工业合成氨的反应为

 。回答下列问题:
。回答下列问题:(4)图甲表示合成氨反应在某段时间
 中反应速率与时间的曲线图,
中反应速率与时间的曲线图, 、
、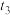 、
、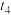 时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中,
时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是
的体积分数最小的一段时间是
A.
 B.
B. C.
C. D.
D.
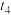 时刻改变的条件是
时刻改变的条件是
您最近一年使用:0次
8 . 下列过程中的颜色变化不能用勒夏特列原理解释的是
A.向5mL0.1mol•L-1重铬酸钾溶液中(存在平衡: (橙色)+H2O⇌2 (橙色)+H2O⇌2 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 (黄色)+2H+)滴入10滴浓硫酸后,橙色变深 |
| B.对2NO2(g)⇌N2O4(g)平衡体系增大压强(缩小体积)的瞬间,气体的颜色变深 |
| C.将NO2球浸泡在热水中,红棕色变深 |
| D.溴水中有平衡:Br2+H2O⇌HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 |
您最近一年使用:0次
名校
解题方法
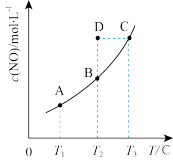
9 . 在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应: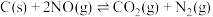 ,平行时
,平行时 与温度
与温度 的关系如图所示,则下列说法正确的是
的关系如图所示,则下列说法正确的是
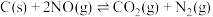 ,平行时
,平行时 与温度
与温度 的关系如图所示,则下列说法正确的是
的关系如图所示,则下列说法正确的是
A.在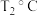 时,若反应体系处于状态D,则此时反应速率: 时,若反应体系处于状态D,则此时反应速率: |
B.若该反应在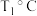 、 、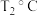 时的平衡常数分别为 时的平衡常数分别为 、 、 ,则 ,则 |
C.该反应的 |
D.若状态B、C、D的压强分别为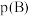 、 、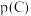 、 、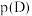 ,则 ,则 |
您最近一年使用:0次
2023-12-18更新
|
446次组卷
|
60卷引用:新疆维吾尔自治区石河子二中2018-2019学年高二上学期第二次月考化学试题
新疆维吾尔自治区石河子二中2018-2019学年高二上学期第二次月考化学试题黑龙江省哈尔滨师大附中2016-2017学年高二10月月考化学卷2016-2017学年新疆生产建设兵团二中高二上期中化学卷湖北省宜昌市葛洲坝中学2017-2018学年高二9月月考化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题(实验班)河北省安平中学2019-2020学年高二上学期第一次月考化学试题黑龙江省大庆实验中学2019-2020学年高二上学期第一次月考化学试题山西省运城市景胜中学2019-2020学年高二12月月考化学试题河南省洛阳市孟津县第二高级中学2020-2021学年高二上学期9月月考化学试题江西省南昌市第十中学2020-2021学年高二上学期第一次月考化学试题河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学试题(普通版)江西省南昌市八一中学2020-2021学年高二上学期10月考试化学试题黑龙江省大庆中学2020-2021学年高二10月月考化学试题(已下线)【南昌新东方】7. 南昌十中 徐钢 刘惠文.河北省张家口市第一中学2021-2022学年高二上学期10月月考化学试题山东学情2023-2024学年高二上学期10月质量检测(人教版)化学试题天津市滨海新区塘沽第一中学2020-2021学年高二上学期第一次月考化学试题辽宁省沈阳市第十五中学2023-2024学年高二上学期12月月考化学试题2017届广东省仲元中学、中山一中等七校高三第一次联考化学试卷重庆市九校联盟2017-2018学年高二上学期期中考试化学试题山西省平遥中学2017-2018学年高二上学期期中考试化学试题【全国百强校】湖北省随州市第一中学2018-2019学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期中考试化学试题陕西省黄陵中学2019-2020学年高二上学期期末考试(普通班)化学试题安徽省滁州市民办高中2019-2020学年高二上学期期末考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期期末考试(实验班)化学试题安徽省枞阳县浮山中学2019-2020学年高二下学期开学考试化学试题湖北省荆州市2018-2019学年高二下学期质量检查化学试题甘肃省兰州大学附属中学(33中)2019-2020学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 专题3 化学平衡图像分析高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 专题2 化学平衡图像分析四川省成都市简阳市阳安中学2020-2021学年高二上学期期中考试化学试题(已下线)【南昌新东方】)5. 2020 高二上 进贤一中 期中考试 田荣达河北省衡水市武邑武罗学校2020-2021学年高二上学期期中考试化学试题江西省新建一中2020-2021学年高二下学期开学考试化学试题选择性必修1 专题2 第三单元 突破3 化学平衡图像分析河南省原阳县2020-2021学年高二上学期期末考试化学试题江苏省泰州中学2021-2022学年高二上学期期中检测化学试题河北省唐山市遵化市2021-2022学年高二上学期期中考试化学试题辽宁省铁岭市清河高级中学2021-2022学年高一下学期第三次阶段考试化学试题辽宁省铁岭市清河高级中学2021-2022学年高一下学期第三次阶段考试化学试题山东省青岛第二中学2019-2020学年高二上学期期中考试化学试题北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题(已下线)【知识图鉴】单元讲练测选择性必修1第2单元03巩固练2.3.3化学平衡中的图像问题 课后甘肃省天水市清水县2022-2023学年高二上学期12月期中考试化学试题上海市上海中学2023-2024学年高二上学期期中考试化学试题辽宁省朝阳市建平县实验中学2023-2024学年高二上学期11月期中考试化学试题北京市铁路第二中学2023-2024学年高二上学期期中考试化学试题四川省泸州市泸县第一中学2023-2024学年高二上学期1月期末化学试题四川省泸州市泸县第四中学2023-2024学年高二上学期1月期末化学试题四川省宜宾市兴文第二中学校2023-2024学年高二上学期1月期末化学试题甘肃省天水市第一中学2023-2024学年高二下学期开学化学试题2016届北京市丰台区高三上学期期末练习化学试卷2016届湖北省武昌实验中学高三高考前模拟理综化学试卷湖北省部分重点中学2018届高三起点考试化学试题上海市奉贤中学2016年高三模拟考试(三模)化学试题安徽省六安市第一中学2019-2020学年高一下学期期末考试化学试题(已下线)第七章 化学反应速率与化学平衡 第41练 化学平衡状态 化学平衡常数
名校
10 . 已知反应:
 kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
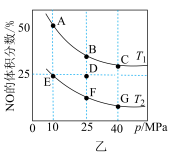
(1)充分反应达到平衡后,放出的热量Q___________ 746.5 kJ(选填“大于”、“小于”、“等于”)
(2)据图分析可知,
________  (选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)
(选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)
A.压缩容器体积 B.升高温度 C.恒压充入氦气 D.加入催化剂
(3)反应在D点达平衡后,若此时降低温度,同时压缩容器体积,在重新达到平衡过程中,D点会向A~G点中的___________ 点方向移动。
(4)工业上可用C与水蒸气在高温下制CO,反应原理为:
 。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g
。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g  ,发生上述反应。达到平衡后,测得
,发生上述反应。达到平衡后,测得 的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后,
的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后, 的浓度仍为0.75 mol/L的是___________(填字母)。
的浓度仍为0.75 mol/L的是___________(填字母)。
(5)工业上可用CO制备甲醇( )。原理为:
)。原理为:
 。
。
在Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中充入相同的CO和 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
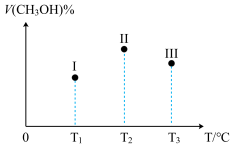
、 且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时
且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时 的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是
的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是___________ 。据此判断上述反应的
___________ (填“>”或“<”)0。
(6)CO可用于工业炼铁。原理为: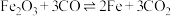 。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
若甲容器中CO的平衡转化率为60%。则T℃时,乙容器中CO的平衡转化率为___________ 。

 kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
(1)充分反应达到平衡后,放出的热量Q
(2)据图分析可知,

 (选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)
(选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)A.压缩容器体积 B.升高温度 C.恒压充入氦气 D.加入催化剂
(3)反应在D点达平衡后,若此时降低温度,同时压缩容器体积,在重新达到平衡过程中,D点会向A~G点中的
(4)工业上可用C与水蒸气在高温下制CO,反应原理为:

 。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g
。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g  ,发生上述反应。达到平衡后,测得
,发生上述反应。达到平衡后,测得 的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后,
的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后, 的浓度仍为0.75 mol/L的是___________(填字母)。
的浓度仍为0.75 mol/L的是___________(填字母)。A. | B.2 mol CO+2 mol  |
C.0.5 mol CO+0.5 mol  | D.27 g 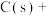 9 g 9 g  0.5 mol 0.5 mol 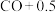 mol mol  |
(5)工业上可用CO制备甲醇(
 )。原理为:
)。原理为:
 。
。在Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中充入相同的CO和
 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时
且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时 的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是
的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是

(6)CO可用于工业炼铁。原理为:
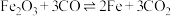 。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。 | CO | Fe |  | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
您最近一年使用:0次



