13-14高二下·浙江温州·期中
1 . 在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ,则下列分析正确的是( )
2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ,则下列分析正确的是( )
 2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ,则下列分析正确的是( )
2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ,则下列分析正确的是( )| A.在该条件下,反应前后的压强之比为6∶5.3 |
| B.若反应开始时容器容积为2 L,则0—2min内v(SO3)=0.35 mol·L-1·min-1 |
| C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol |
| D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ |
您最近一年使用:0次
2020-08-10更新
|
724次组卷
|
25卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高二(理)上学期10月月考化学试题
【全国百强校】山西省太原市第五中学2018-2019学年高二(理)上学期10月月考化学试题(已下线)2013-2014浙江省温州中学高二下学期期中化学试卷(已下线)2014届浙江省温州中学高二下学期期中化学试卷 (已下线)2015届安徽省六校教育研究会高三第一次联考化学试卷2015-2016学年辽宁省沈阳二中高二上10月月考化学试卷2015-2016学年天津市静海一中等六校高二上学期期末联考化学试卷2016-2017学年江西省上高二中高二上9月月考化学试卷广西陆川县中学2017-2018学年高二上学期期末考试化学试题河南省固始县2017-2018学年上期期末高中二年级期末化学试题【校级联考】天津市七校(静海一中、宝坻一中、杨村一中等)2018-2019学年高二上学期期末考试化学试题江西省上高县第二中学2019-2020学年高二上学期第三次月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期阶段性检测(一)化学试题(已下线)第2章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)2.3.1化学平衡状态(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)辽宁省沈阳市法库县高级中学2020-2021学年高二9月月考化学试题湖南省娄底市2020-2021学年高二上学期期中考试化学试题(已下线)第23讲 化学平衡状态 化学平衡的移动(精练)-2021年高考化学一轮复习讲练测江西省上高二中2020-2021学年高二上学期第三次月考化学试题黑龙江省哈尔滨市宾县第一中学2021届高三上学期第三次月考化学试题江西省赣州市信丰中学2020-2021学年高二上学期入学考试化学试题新疆乌鲁木齐市第八中学2018-2019学年高二上学期期中考试化学试题(已下线)第19讲 化学平衡 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)安徽省宿州市十三所重点中学2021-2022学年高二上学期期末质量检测(理科人教版)化学试题山东省青岛第二中学2020-2021学年高二上学期期中考试化学试题内蒙古赤峰第四中学2023-2024学年高二上学期12月期中考试化学试题
名校
2 . 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为2L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)前10min, (CO2)=
(CO2)=____ mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是____ (填字母)。
a.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
b.混合气体的压强不随时间的变化而变化
c.单位时间内生成1molH2O,同时生成1molCH3OH
d.混合气体的平均相对分子质量不随时间的变化而变化
e.混合气体的密度不随时间的变化而变化
f.CO2和CH3OH的反应速率之比为1∶1
(3)反应前与平衡时的压强比为____ 。
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是____ 。
(5)平衡时H2的转化率为____ 。

(1)前10min,
 (CO2)=
(CO2)=(2)能说明上述反应达到平衡状态的是
a.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
b.混合气体的压强不随时间的变化而变化
c.单位时间内生成1molH2O,同时生成1molCH3OH
d.混合气体的平均相对分子质量不随时间的变化而变化
e.混合气体的密度不随时间的变化而变化
f.CO2和CH3OH的反应速率之比为1∶1
(3)反应前与平衡时的压强比为
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是
(5)平衡时H2的转化率为
您最近一年使用:0次
2022-04-29更新
|
172次组卷
|
3卷引用:山西省长治市第二中学校2021-2022学年高一下学期期中考试化学试题
名校
解题方法
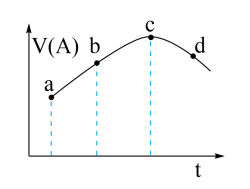
3 . 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A、B,发生反应:A(g)+2B(g) 3C(g)+D(l),下图是A的正反应速率v(A)随时间变化的示意图。下列说法正确的是( )
3C(g)+D(l),下图是A的正反应速率v(A)随时间变化的示意图。下列说法正确的是( )
 3C(g)+D(l),下图是A的正反应速率v(A)随时间变化的示意图。下列说法正确的是( )
3C(g)+D(l),下图是A的正反应速率v(A)随时间变化的示意图。下列说法正确的是( )
| A.反应物A的浓度:a点小于b点 |
| B.可能是某种物质对反应起到的催化作用 |
| C.曲线上的c、d两点都表示达到反应限度 |
| D.平均反应速率:ab段大于bc段 |
您最近一年使用:0次
2020-03-19更新
|
656次组卷
|
4卷引用:山西省太原市山西省实验中学2019-2020学年高二上学期10月月考化学试题
名校
解题方法
4 . 在一定温度下的恒容容器中,发生反应:2A(g)+B(s) ⇌C(g)+D(g),下列描述中能表明反应已达到平衡状态的是
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内 A、C、D 三种气体的浓度之比为 2∶1∶1
⑤单位时间内生成 n mol C,同时生成 n mol D
⑥单位时间内生成 n mol D,同时生成 2n mol A
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内 A、C、D 三种气体的浓度之比为 2∶1∶1
⑤单位时间内生成 n mol C,同时生成 n mol D
⑥单位时间内生成 n mol D,同时生成 2n mol A
| A.①②⑤ | B.②③⑤ | C.②③⑥ | D.①③⑥ |
您最近一年使用:0次
2020-04-03更新
|
603次组卷
|
13卷引用:山西省稷山中学2021-2022学年高一下学期期中考试化学试题
山西省稷山中学2021-2022学年高一下学期期中考试化学试题天津市第二南开学校2019-2020学年高一下学期阶段性检测化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第三节 化学反应的快慢和限度 方法帮甘肃省兰州市教育局第四片区2020-2021学年高一下学期期中考试化学试题吉林省延边朝鲜族自治州延边二中北校区2020-2021学年高一下学期第一次月考化学试题新疆乌鲁木齐市第四中学2021-2022学年高一下学期期中考试化学试题湖北省黄冈市麻城市第二中学2021-2022学年高一下学期期中考试化学试题吉林省大安市第六中学校2021-2022学年高一下学期期中考试化学试题辽宁省鞍山市普通高中2022-2023学年高一下学期期中考试化学(A卷)试题新疆维吾尔自治区喀什第二中学2022-2023学年高一下学期期中考试化学试题吉林省长春市绿园区长春市新解放学校2022-2023学年高一下学期6月期中化学试题第2课时 化学反应的限度、化学反应条件的控制江西省横峰中学2023-2024学年高一下学期期中考试化学试题
13-14高三·黑龙江哈尔滨·阶段练习
名校
解题方法
5 . 一定条件下,对于可逆反应X(g)+3Y(g)⇌2Z(g),若X、Y、Z的起始浓度分别为c0(X)、c0(Y)、c0(Z)(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol⋅L−1、0.3 mol⋅L−1、0.08 mol⋅L−1,则下列判断正确的是
| A.c0(X):c0(Y)=3:1 |
| B.平衡时,Y和Z的生成速率之比为2:3 |
| C.c0(X)的取值范围为0 mol⋅L−1<c0(X)<0.14 mol⋅L−1 |
| D.X、Y的转化率不相等 |
您最近一年使用:0次
2020-04-17更新
|
343次组卷
|
25卷引用:山西省太原市山西省实验中学2019-2020学年高二上学期10月月考化学试题
山西省太原市山西省实验中学2019-2020学年高二上学期10月月考化学试题(已下线)2015届黑龙江省哈尔滨市第三中学高三第一次测试化学试卷2015-2016学年辽宁省沈阳二中高二上10月月考化学试卷2016-2017学年贵州省安顺平坝第一高级中学高二上期中化学卷2018-2019学年人教版高中化学选修四章化学反应速率和化学平衡末综合测评(二)江苏省泰州市第二中学2017-2018学年高二上学期期中考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高二(理)下学期寒假学情检测化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第二次月考化学试题广东省中山市第一中学2018-2019学年高二上学期第一次段考化学试题甘肃省镇原县镇原中学2019-2020学年高二上学期期中考试化学(理)试题甘肃省镇原县镇原中学2019-2020学年高一上学期期中考试化学(理)试题(已下线)专题7.2 化学平衡状态 化学平衡移动(讲)-《2020年高考一轮复习讲练测》夯基提能2020届高三化学选择题对题专练——选修四化学反应原理—— 转化率与产率的相关计算夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——化学平衡状态的建立及判断(已下线)【南昌新东方】2019 新建二中 高二上 第二次月考(已下线)【南昌新东方】2019 南昌二中 高一下 第二次月考(已下线)第23讲 化学平衡状态 化学平衡的移动 (精讲)——2021年高考化学一轮复习讲练测陕西省西安市第一中学2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 易错疑难集训(一)河北省黄骅中学2020-2021学年高二上学期第一次月考化学试题福建省福州市福建师范大学附属中学2020-2021学年高二上学期期中考试化学试题广东省华附、省实、广雅、深中四校2020-2021学年高二下学期期末联考化学试题黑龙江双鸭山市第一中学2020-2021学年高一下学期期末考试化学试题(已下线)第19讲 化学平衡(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)安徽省六安市第一中学2021-2022学年高二上学期开学考试化学试题
6 . 在密闭容器中进行反应:X2(g)+3Y2(g) 2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
 2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
2Z(g),其中X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。| A.c(Z)=0.5 mol·L-1 | B.c(Y2)=0.5 mol·L-1 |
| C.c(X2)=0.2 mol·L-1 | D.c(Y2)=0.6 mol·L-1 |
您最近一年使用:0次
2016-12-09更新
|
1966次组卷
|
14卷引用:山西省大同市天镇一中2019-2020学年高二上学期期中考试化学试题
山西省大同市天镇一中2019-2020学年高二上学期期中考试化学试题(已下线)2014学年高一化学人教版必修2 2章化学反应与能量练习卷2015-2016学年新疆生产建设兵团二中高一下期中化学试卷河北省邯郸市第一中学2019—2020学年高一4月月考化学试题山东济南市历城第二中学2019-2020学年高一下学期开学考试化学试题河南省兰考县第三高级中学卫星试验部2020-2021学年高二上学期第一次月考化学试题安徽省合肥市第九中学2020-2021学年高二上学期第一次月考化学试题河北保定市博野县实验中学2020-2021学年高一下学期期中考试化学试题河南省焦作市武陟县第一中学东校区2021-2022学年高一下学期4月月考化学试题 河北省邯郸市鸡泽县第一中学2022-2023学年高一下学期第一次月考化学试题江西省抚州市七校2022-2023学年高一下学期期中考试化学试题江西省南丰县第一中学 黎川一中 宜黄一中 南城二中 金溪一中 广昌一中 乐安县实验学校2022-2023学年高一下学期期中联考化学试卷 云南省保山市腾冲市第八中学2022-2023学年高一下学期期中考试化学试卷新疆乌鲁木齐市高级中学2023-2024学年高一下学期期中考试 化学试卷
名校
解题方法
7 . 恒温时,向2L密闭容器中通入一定量的气体X和Y,发生反应:2X(g)+Y(g)⇌3Z(g)。Y的物质的量随时间变化的曲线如图所示。下列说法正确的是
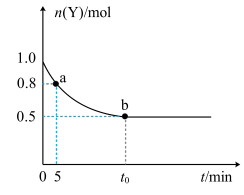

| A.a点时,正反应速率小于逆反应速率 |
| B.0~5min内,以X表示的反应速率是0.02mol·L-1·min-1 |
| C.b点时该反应达到了最大限度,反应停止 |
| D.t0min时,c(Z)=0.75mol·L-1 |
您最近一年使用:0次
2021-05-11更新
|
243次组卷
|
3卷引用:山西省大同市灵丘一中、广灵一中2020-2021学年高一下学期期中联考化学试题
名校
8 . 一定温度和压强下,在2L的密闭容器中合成氨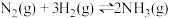 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法不正确的是
。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法不正确的是
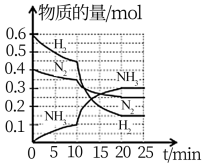
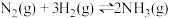 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法不正确的是
。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法不正确的是
A.0~10min内,以 表示的平均反应速率为 表示的平均反应速率为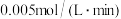 |
B.10~20min内, 浓度变化的原因可能是缩小容器容积 浓度变化的原因可能是缩小容器容积 |
C. 的平衡转化率与 的平衡转化率与 平衡转化率相等 平衡转化率相等 |
| D.该反应在20min时达到化学平衡状态 |
您最近一年使用:0次
2021-05-21更新
|
204次组卷
|
2卷引用:山西省怀仁市2020-2021学年高一下学期期中化学试题
9-10高一下·陕西西安·期末
解题方法
9 . 一定温度下,某一密闭且体积不变的容器内有可逆反应A(g)+3B(g) 2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是( )
2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是( )
 2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是( )
2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是( )| A.C物质的生成速率和分解速率相等 |
| B.容器内气体的密度不再随时间而改变 |
| C.单位时间内生成amol物质A,同时生成3amol物质B |
| D.A、B、C的分子数之比为1:3:2 |
您最近一年使用:0次
2020-05-19更新
|
315次组卷
|
7卷引用:山西省忻州市第二中学2019-2020学年高一下学期期末考试化学试题
解题方法
10 . 下列方法中可以证明2HI(气) H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是
①单位时间内生成nmolH2的同时生成nmolHI
②一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④反应速率v(H2)=v(I2)=0.5v(HI)时
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
 H2(气)+I2(气)已达平衡状态的是
H2(气)+I2(气)已达平衡状态的是①单位时间内生成nmolH2的同时生成nmolHI
②一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④反应速率v(H2)=v(I2)=0.5v(HI)时
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
| A.②③④⑤⑥ | B.②⑥⑦⑧⑨ | C.①②⑥⑧ | D.②⑥⑨ |
您最近一年使用:0次
2021-11-06更新
|
161次组卷
|
2卷引用:山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题



