1 . 将 转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人
转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如表所示。
的浓度随时间变化如表所示。
(1)从0min到6min,
___________  。
。
(2)能说明上述反应达到平衡状态的是___________(填标号)。
(3)上述反应10min时,混合气体中 的物质的量分数为
的物质的量分数为___________ %。(取整数)
(4)上述反应12min末时,混合气体中 和
和 的质量之比是
的质量之比是___________ 。
(5)第3min时的
___________ (填“>”、“<”、“=”或“无法比较”)第9min时的 。
。
(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2L的恒容密闭容器中,发生反应 ,X和
,X和 两种物质的浓度随时间的变化情况如表所示。
两种物质的浓度随时间的变化情况如表所示。
①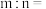
___________ 。
②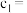
___________  。(保留两位有效数字)
。(保留两位有效数字)
③若反应在第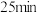 时改变某种条件,则
时改变某种条件,则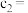
___________  。
。
 转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人
转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如表所示。
的浓度随时间变化如表所示。时间 | 0 | 3 | 6 | 9 | 12 |
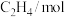 | 0 | 0.25 | 0.32 | 0.37 | 0.37 |
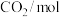 | 1 | 0.50 | 0.36 | 0.26 | 0.26 |

 。
。(2)能说明上述反应达到平衡状态的是___________(填标号)。
A.反应中 与 与 的物质的量浓度之比为 的物质的量浓度之比为 |
| B.混合气体的压强不随时间的变化而变化 |
C.单位时间内生成 ,同时生成 ,同时生成 |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
 的物质的量分数为
的物质的量分数为(4)上述反应12min末时,混合气体中
 和
和 的质量之比是
的质量之比是(5)第3min时的

 。
。(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2L的恒容密闭容器中,发生反应
 ,X和
,X和 两种物质的浓度随时间的变化情况如表所示。
两种物质的浓度随时间的变化情况如表所示。时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
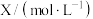 | 0.2 |  | 0.6 | 0.6 | 0.6 | 0.9 |  |  |
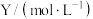 | 0.6 |  | 0.4 | 0.4 | 0.4 | 0.4 | 0.5 | 0.5 |
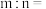
②
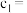
 。(保留两位有效数字)
。(保留两位有效数字)③若反应在第
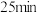 时改变某种条件,则
时改变某种条件,则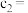
 。
。
您最近一年使用:0次
2 . 在一定条件下,向V L密闭容器中充入 和
和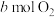 ,发生反应
,发生反应 。
。
(1)反应刚开始时,由于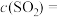
___________ ,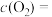
___________ ,而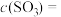
___________ ,所以化学反应速率___________ 最大,而___________ 最小(为零)(填“v(正)”或“v(逆)”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为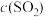
___________ (填“增大”“减小”或“不变”下同),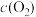
___________ ,而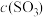
___________ ,从而化学反应速率v(正)___________ ,而v(逆)___________ 。
(3)当反应进行到时v(正)与v(逆)___________ 时,此时可逆反应达到最大限度,若保持外界条件不变时,混合物中各组分的物质的量、浓度、质量分数、体积分数及总压强都___________ 。
(4)以下是反应: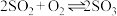 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。
试回答下列问题:
①提高该化学反应限度的途径:___________ 。
②要实现 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是___________ 。
 和
和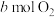 ,发生反应
,发生反应 。
。(1)反应刚开始时,由于
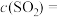
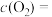
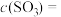
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为
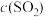
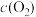
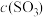
(3)当反应进行到时v(正)与v(逆)
(4)以下是反应:
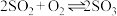 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。压强 转化率 温度 | 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
①提高该化学反应限度的途径:
②要实现
 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是
您最近一年使用:0次
3 . 向某容积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答下列问题:
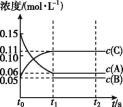
(1)密闭容器的容积是_______ L。
(2)若t1=15时,则t0~t1s内以C物质浓度变化表示的反应速率v(C)=_______ 。
(3)写出反应的化学方程式:_______ 。
(4)t2s时,C在平衡混合气体中的百分含量为_______ ,此时v正(A)_______ v逆(B)(选填“>”“<”或“=”)。
(5)B的起始的物质的量是_______ 。

(1)密闭容器的容积是
(2)若t1=15时,则t0~t1s内以C物质浓度变化表示的反应速率v(C)=
(3)写出反应的化学方程式:
(4)t2s时,C在平衡混合气体中的百分含量为
(5)B的起始的物质的量是
您最近一年使用:0次
4 . 向2L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3——t4阶段为使用催化剂。观察下图,回答下列问题:
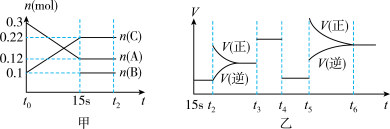
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为____________ 。
(2)乙图中t2时引起平衡移动的条件是____________ ,t5时引起平衡移动的条件是____________ 。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是____________ 。
(4)该反应的化学方程式可以表示为:____________ 。
(5)反应开始时加入的B的物质的量为____________ 。

(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为
(2)乙图中t2时引起平衡移动的条件是
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是
(4)该反应的化学方程式可以表示为:
(5)反应开始时加入的B的物质的量为
您最近一年使用:0次
2020-08-22更新
|
88次组卷
|
2卷引用:山西省运城市景胜中学2020-2021学年高二10月月考化学试题
5 . 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
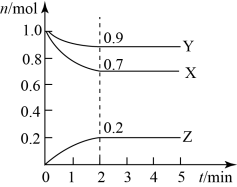
根据图中数据填空:
(1)该反应的化学方程式为___ 。
(2)若X、Y、Z均为气体,2min时反应达到平衡,此时体系内压强与开始时的压强之比为___ 。
(3)若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时___ (填“增大”“减小”或“相等”)。

根据图中数据填空:
(1)该反应的化学方程式为
(2)若X、Y、Z均为气体,2min时反应达到平衡,此时体系内压强与开始时的压强之比为
(3)若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时
您最近一年使用:0次
名校
解题方法
6 . 一定条件下,恒容密闭容器中发生某可逆反应,A、B、C三种气体的物质的量浓度随时间的变化如图所示。请回答下列问题:
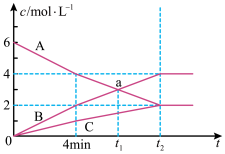
(1)此反应的化学方程式为___ 。
(2)反应从开始至4min末,用A表示的平均反应速率为____ 。
(3)t2的值___ 8(填“大于”、“等于”或“小于”),其原因是___ 。
(4)某同学经分析得出如下结论,其中正确的是___ (填选项序号)。
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度

(1)此反应的化学方程式为
(2)反应从开始至4min末,用A表示的平均反应速率为
(3)t2的值
(4)某同学经分析得出如下结论,其中正确的是
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度
您最近一年使用:0次
2020-06-07更新
|
75次组卷
|
2卷引用:山西省太原市第五中学2019-2020学年高一下学期5月开学摸底考试化学试题
解题方法
7 . 某温度下在2L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。
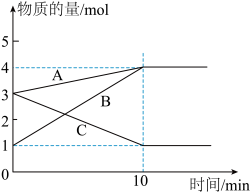
(1)该反应的化学方程式是________________________
(2)若A、B、C均为气体,10min后反应达到平衡,
①此时体系的压强是开始时的________ 倍。
②在该条件达到平衡时反应物的转化率为________ %(计算结果保留1位小数)
(3)关于该反应的说法正确的是_________ 。
a.到达10min时停止反应
b.在到达10min之前C气体的消耗速率大于它的生成速率
c.在10min时B气体的正反应速率等于逆反应速率

(1)该反应的化学方程式是
(2)若A、B、C均为气体,10min后反应达到平衡,
①此时体系的压强是开始时的
②在该条件达到平衡时反应物的转化率为
(3)关于该反应的说法正确的是
a.到达10min时停止反应
b.在到达10min之前C气体的消耗速率大于它的生成速率
c.在10min时B气体的正反应速率等于逆反应速率
您最近一年使用:0次
名校
解题方法
8 . 某温度下,在 2 L 恒容密闭容器中 3 种物质间进行反应,X、Y、Z 的物质的量随时间的变化曲线如图所示,反应在 t1 min 时达到平衡。
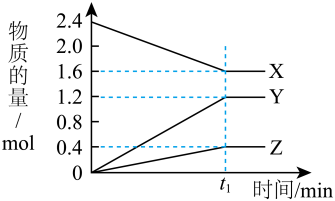
(1)请写出该反应的化学方程式:_____ 。
(2)若上述反应中X、Y、Z 分别为 NH3、H2、N2,在此 t1 min 时间内,用H2表示该反应的平均速率 v(H2)为_____ 。
(3)拆开 1mol 共价键所需吸收的能量如下表:
1mol N2完全反应为NH3_____ (填:吸收或放出)_____ kJ 能量。事实上,将 1molN2和3molH2放在反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是_________ 。
(4)下列叙述能判断该反应达到平衡状态的是_____ (填字母代号)。
A 容器内各气体组分的质量分数不再发生改变
B 正反应速率与逆反应速率相等
C 容器内气体的密度不再发生改变
D 混合气体的平均相对分子质量不再发生改变

(1)请写出该反应的化学方程式:
(2)若上述反应中X、Y、Z 分别为 NH3、H2、N2,在此 t1 min 时间内,用H2表示该反应的平均速率 v(H2)为
(3)拆开 1mol 共价键所需吸收的能量如下表:
共价键 | H-H | N≡N | N-H |
吸收的能量/kJ | 436 | 946 | 391 |
(4)下列叙述能判断该反应达到平衡状态的是
A 容器内各气体组分的质量分数不再发生改变
B 正反应速率与逆反应速率相等
C 容器内气体的密度不再发生改变
D 混合气体的平均相对分子质量不再发生改变
您最近一年使用:0次
名校
9 . 一定温度下,在容积为VL的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
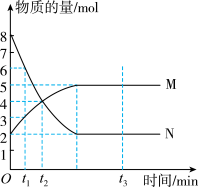
(1)此反应的化学方程式中 =
=____ 。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为_____ 。
(3)下列叙述能说明上述反应达到平衡状态的是____ (填字母)。
A 反应中M与N的物质的量之比为1∶1
B 混合气体的总质量不随时间的变化而变化
C 混合气体的总物质的量不随时间的变化而变化
D 单位时间内消耗a mol N,同时生成b mol M
E 混合气体的压强不随时间的变化而变化
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中
 =
=(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3)下列叙述能说明上述反应达到平衡状态的是
A 反应中M与N的物质的量之比为1∶1
B 混合气体的总质量不随时间的变化而变化
C 混合气体的总物质的量不随时间的变化而变化
D 单位时间内消耗a mol N,同时生成b mol M
E 混合气体的压强不随时间的变化而变化
您最近一年使用:0次
2019-06-27更新
|
371次组卷
|
6卷引用:山西省长治市第一中学校2021-2022学年高一下学期第六次练考化学试题
山西省长治市第一中学校2021-2022学年高一下学期第六次练考化学试题(已下线)09~10年黄冈中学高一下学期期末考试化学卷(已下线)同步君 必修2 第2章 第3节 化学反应的限度高中化学人教版 必修2 第二章 化学反应与能量 第三节 化学反应的速率和限度 化学反应的限度江西省鄱阳县第二中学2018-2019学年高一下学期期中考试化学试题苏教版高一化学必修2专题2《化学反应与能量转化》测试卷
11-12高二上·山西大同·期中
解题方法
10 . 将物质的量均为3.00mol物质A、B混合于5L溶 器中,发生如下反应 3A+B 2C,在反应过程中C的物质的量分数随温度变化如图所示:
2C,在反应过程中C的物质的量分数随温度变化如图所示:
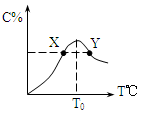
(1)T0对应的反应速率v正和v逆的关系是_____ (用含“>”“<”“=”表示,下同);
(2)此反应的正反应为______ 热反应;
(3)X、Y两点A物质正反应速率的大小关系是______________ ;
(4)温度T<T0时,C%逐渐增大的原因是________________________ ;
(5)若Y点的C的物质的量分数为25%,则参加反应的A的物质的量为_______ ;若Y点时所耗时间为2 min,则B物质的反应速率为__________ 。
 2C,在反应过程中C的物质的量分数随温度变化如图所示:
2C,在反应过程中C的物质的量分数随温度变化如图所示:
(1)T0对应的反应速率v正和v逆的关系是
(2)此反应的正反应为
(3)X、Y两点A物质正反应速率的大小关系是
(4)温度T<T0时,C%逐渐增大的原因是
(5)若Y点的C的物质的量分数为25%,则参加反应的A的物质的量为
您最近一年使用:0次



