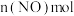1 . 苯乙烯是生产塑料、橡胶的重要原料,工业上以铁钴催化剂催化乙苯催化脱氢可获得苯乙烯。主要发生的反应为:_______ 。
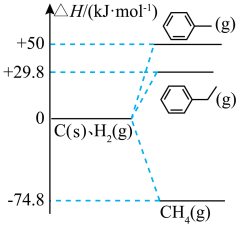
(2)已知,在298K、101kPa条件下,某些物质的相对能量(△H)变化关系如图所示,则△H2=_______ kJ•mol-1。_______ 。
(4)往刚性密闭容器中同时通入乙苯和一定比例水蒸气,控制反应温度为600℃、体系起始总压强为100kPa的条件下进行反应。
①通入水蒸气的作用有_______ 。
②假设容器中只发生反应I,测得体系总压和乙苯转化率随时间变化结果如图所示。_______ kPa,平衡常数Kp=_______ kPa(Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
③反应速率v正=k正×p(乙苯),v逆=k逆×p(苯乙烯)×p(氢气),k正、k逆分别为正、逆反应速率常数,则a点时 =
=_______ 。
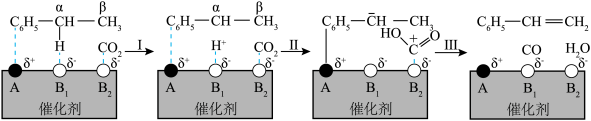
(5)工业上也可以利用CO2弱氧化性在催化剂条件下制备苯乙烯,其反应的机理如图所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。αC—H的极性_______ (选填“>”或“<”)βC—H,步骤Ⅲ形成苯乙烯后更容易脱附的原因为_______ 。
反应I: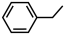 (g)
(g)
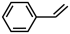 (g)+H2(g) △H1=+117.6kJ•mol-1
(g)+H2(g) △H1=+117.6kJ•mol-1
反应Ⅱ: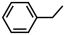 (g)+H2(g)
(g)+H2(g)
 (g)+CH4(g) △H2
(g)+CH4(g) △H2
反应Ⅲ: (g)
(g) 8C(s)+H2(g) △H3=-1.67kJ•mol-1
8C(s)+H2(g) △H3=-1.67kJ•mol-1
(2)已知,在298K、101kPa条件下,某些物质的相对能量(△H)变化关系如图所示,则△H2=
| A.v正(C6H5C2H5)=v正(C6H5C2H3) | B.容器内气体密度不再变化 |
| C.苯乙烯、H2的分子数之比不再变化 | D.气体的平均相对分子质量不再变化 |
(4)往刚性密闭容器中同时通入乙苯和一定比例水蒸气,控制反应温度为600℃、体系起始总压强为100kPa的条件下进行反应。
①通入水蒸气的作用有
②假设容器中只发生反应I,测得体系总压和乙苯转化率随时间变化结果如图所示。
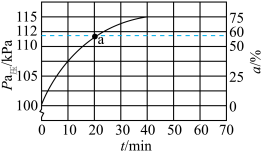
③反应速率v正=k正×p(乙苯),v逆=k逆×p(苯乙烯)×p(氢气),k正、k逆分别为正、逆反应速率常数,则a点时
 =
=(5)工业上也可以利用CO2弱氧化性在催化剂条件下制备苯乙烯,其反应的机理如图所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。αC—H的极性
您最近一年使用:0次
2 . 一定条件下的密闭容器中,可逆反应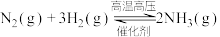 达到平衡时,下列说法正确的是
达到平衡时,下列说法正确的是
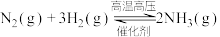 达到平衡时,下列说法正确的是
达到平衡时,下列说法正确的是| A.正反应速率为0 |
B. 、 、 、 、 的百分含量相等 的百分含量相等 |
C. 的浓度不再随时间的变化而变化 的浓度不再随时间的变化而变化 |
D. 、 、 、 、 的物质的量之比为1∶3∶2 的物质的量之比为1∶3∶2 |
您最近一年使用:0次
解题方法
3 . 在一定条件下,对于密闭容器中进行的反应: ,下列说法能充分说明该反应已达到化学平衡状态的是
,下列说法能充分说明该反应已达到化学平衡状态的是
 ,下列说法能充分说明该反应已达到化学平衡状态的是
,下列说法能充分说明该反应已达到化学平衡状态的是A. 、 、 完全转化为 完全转化为 | B. 、 、 、 、 的浓度一定相等 的浓度一定相等 |
| C.正、逆反应速率相等且等于零 | D. 、 、 、 、 的浓度不再改变 的浓度不再改变 |
您最近一年使用:0次
名校
解题方法
4 . 道路千万条,安全第一条。当汽车在高速行驶中受到猛烈撞击时,会产生大量气体充满气囊,从而保护驾驶员和乘客的安全。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:______ (填“吸热”或“放热”)反应。
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为______ kJ(用含a、b的代数式表示)。
Ⅱ.汽车尾气中的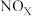 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应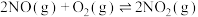 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:
(3)下图表示 的变化的曲线是
的变化的曲线是______ ______ (选填序号,下同)。
a.容器内气体的颜色不再变化 b.
c. d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是______ 。
a.增大 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体
Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示:______ 极(填写“正”或“负”),M处电极反应式是______ ;
(7)该电池产生11.2L(标况下) ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为______ 。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:
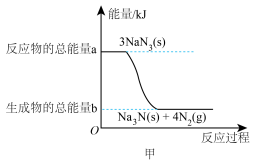
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为
Ⅱ.汽车尾气中的
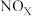 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应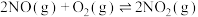 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(3)下图表示
 的变化的曲线是
的变化的曲线是 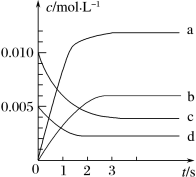
a.容器内气体的颜色不再变化 b.

c.
 d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是
a.增大
 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应
 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示: 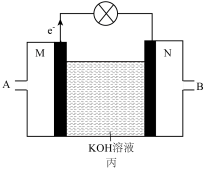
(7)该电池产生11.2L(标况下)
 ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为
您最近一年使用:0次
5 .  和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。
Ⅰ.
Ⅱ.
Ⅲ.
(1) =
=___________ 。
(2)① =1:1对应图中曲线
=1:1对应图中曲线___________ (填序号)。
②900K下,曲线b、c、d的平衡转化率显著大于a的原理为___________ 。
(3)900K,将 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。
①下列说法正确的是___________ (填序号)。
A.通入氩气可提高 的平衡转化率
的平衡转化率
B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡
D.改善催化剂的性能可提高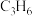 生产效率
生产效率
②若初始压强为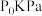 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
=___________  ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=___________ 。
(4)利用反应 可制备高纯Ni。
可制备高纯Ni。
① 晶体中不存在的作用力有
晶体中不存在的作用力有___________ 。
A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
② 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是___________ ,判断依据是___________ 。
 和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。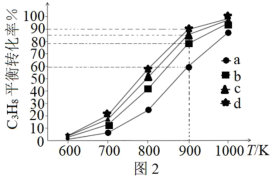
Ⅰ.

Ⅱ.

Ⅲ.

(1)
 =
=(2)①
 =1:1对应图中曲线
=1:1对应图中曲线②900K下,曲线b、c、d的平衡转化率显著大于a的原理为
(3)900K,将
 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。①下列说法正确的是
A.通入氩气可提高
 的平衡转化率
的平衡转化率B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当
 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡D.改善催化剂的性能可提高
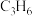 生产效率
生产效率②若初始压强为
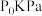 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
= ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=(4)利用反应
 可制备高纯Ni。
可制备高纯Ni。①
 晶体中不存在的作用力有
晶体中不存在的作用力有A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
②
 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是
您最近一年使用:0次
6 . 甲硫醇(CH3SH)是重要的有机化工中间体,可用于合成维生素。通过CH3OH和H2S合成CH3SH的主要反应为:
Ⅰ.
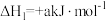
Ⅱ.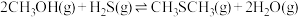
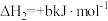
回答下列问题:
(1)计算反应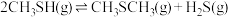 的△H=
的△H=________ kJ/mol。
(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是________ (填选项字母);若按相同比例再充入一定量CH3OH(g)和H2S(g),CH3OH(g)的平衡转化率将________ (填“变大”“变小”或“不变”)。
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为________ (CH3SH的选择性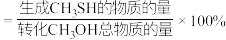 )。
)。
②反应Ⅰ的平衡常数Kp=________ (Kp是用分压表示的平衡常数,结果保留两位小数)。
(4)在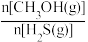 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。________ Mpa/min(结果保留两位有效数字)。
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为________ 。
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:________ 。
Ⅰ.

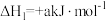
Ⅱ.
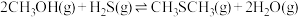
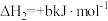
回答下列问题:
(1)计算反应
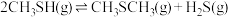 的△H=
的△H=(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为
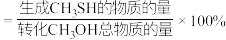 )。
)。②反应Ⅰ的平衡常数Kp=
(4)在
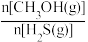 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。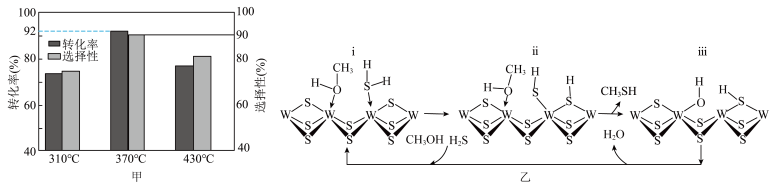
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:
您最近一年使用:0次
名校
7 . 化学反应过程既有物质变化也有能量变化。
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。
(1)由 和
和 合成氨时,需要
合成氨时,需要_____________ (填“吸收”或“放出”)能量,写出该反应的热化学方程式_________________ 。
Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。_______ (填“氧化反应”或“还原反应”),电池工作过程中, 向极移动
向极移动_________ (填“A”或“B”);
②该燃料电池的总反应方程式可表示为__________ 。在标准状况下,若A极区产生11.2L  ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是__________ mol。
Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:_____________ 。
(4)反应开始至2min,以气体X表示的平均反应速率为___________ 。
(5)下列措施能增大反应速率的是_________ 。
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436
 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。(1)由
 和
和 合成氨时,需要
合成氨时,需要Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。
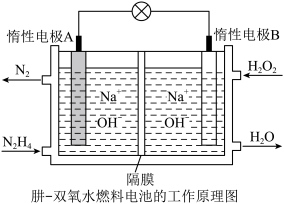
 向极移动
向极移动②该燃料电池的总反应方程式可表示为
 ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
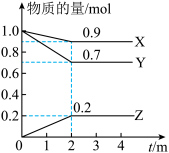
(4)反应开始至2min,以气体X表示的平均反应速率为
(5)下列措施能增大反应速率的是
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
| A.混合气体的压强不随时间的变化而变化 | B. |
| C.X体积分数保持不变 | D.混合气体的密度不随时间的变化而变化 |
您最近一年使用:0次
名校
解题方法
8 . 某温度下CO2加氢制甲醇的总反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:_______ (填“大于”“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)2 min末时v正_______ (填“<”“>”或“=”)v逆。
(3)恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.混合气体的密度保持不变
B.消耗1molCO2的同时消耗1molCH3OH
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.CO2(g)体积分数保持不变
E.v(H2) = 3v(CH3OH)
(4)该反应平衡时H2的转化率为_______ 。
(5)二氧化碳加氢制甲醇一般认为可通过两步反应来实现,物质变化与体系能量变化如题图所示。 CO(g)+H2O(g)。
CO(g)+H2O(g)。
②_______ (用化学方程式表示)。
总反应可表示为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH_______ (填“>”或“<”)0。
 CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答: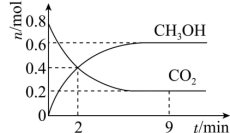
(2)2 min末时v正
(3)恒温恒容条件下,能说明反应已达平衡状态的是
A.混合气体的密度保持不变
B.消耗1molCO2的同时消耗1molCH3OH
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.CO2(g)体积分数保持不变
E.v(H2) = 3v(CH3OH)
(4)该反应平衡时H2的转化率为
(5)二氧化碳加氢制甲醇一般认为可通过两步反应来实现,物质变化与体系能量变化如题图所示。
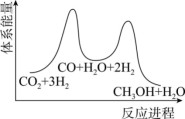
 CO(g)+H2O(g)。
CO(g)+H2O(g)。②
总反应可表示为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH
您最近一年使用:0次
9 . Ⅰ。在下列事实中,什么因素影响了化学反应速率?
(1)集气瓶中有 和
和 的混合气体,在瓶外点燃镁条时发生爆炸
的混合气体,在瓶外点燃镁条时发生爆炸___________ ;
黄铁矿煅烧时要粉碎成细小的矿粒。___________ ;
熔化的 放出气泡很慢,加入少量
放出气泡很慢,加入少量 后很快产生气体。
后很快产生气体。___________ ;
夏天食品容易变质,冬天就不易发生该现象。___________ ;
同样大小的石灰石分别在 的盐酸和
的盐酸和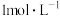 的盐酸中反应,反应速率不同。
的盐酸中反应,反应速率不同。___________ 。
Ⅱ。某温度时,在 密闭容器中
密闭容器中 三种气态物质的物质的量
三种气态物质的物质的量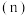 随时间
随时间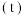 变化的曲线如图所示,由图中数据分析:
变化的曲线如图所示,由图中数据分析:___________ 。
(3)反应开始至 ,用
,用 表示的平均反应速率为
表示的平均反应速率为___________ 。此时, 的转化率为
的转化率为___________ 。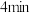 时,加入1体积
时,加入1体积 ,反应速率
,反应速率___________ (填“变大”、“变小”、“不变”)
(4)下列叙述不能说明上述反应达到化学平衡状态的是___________ (填序号)。
A. 的物质的量不随时间变化而变化
的物质的量不随时间变化而变化
B. 的质量分数不随时间变化而变化
的质量分数不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.
E.
F.单位时间内每消耗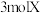 ,同时生成
,同时生成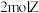
(1)集气瓶中有
 和
和 的混合气体,在瓶外点燃镁条时发生爆炸
的混合气体,在瓶外点燃镁条时发生爆炸黄铁矿煅烧时要粉碎成细小的矿粒。
熔化的
 放出气泡很慢,加入少量
放出气泡很慢,加入少量 后很快产生气体。
后很快产生气体。夏天食品容易变质,冬天就不易发生该现象。
同样大小的石灰石分别在
 的盐酸和
的盐酸和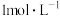 的盐酸中反应,反应速率不同。
的盐酸中反应,反应速率不同。Ⅱ。某温度时,在
 密闭容器中
密闭容器中 三种气态物质的物质的量
三种气态物质的物质的量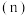 随时间
随时间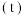 变化的曲线如图所示,由图中数据分析:
变化的曲线如图所示,由图中数据分析:
(3)反应开始至
 ,用
,用 表示的平均反应速率为
表示的平均反应速率为 的转化率为
的转化率为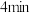 时,加入1体积
时,加入1体积 ,反应速率
,反应速率(4)下列叙述不能说明上述反应达到化学平衡状态的是
A.
 的物质的量不随时间变化而变化
的物质的量不随时间变化而变化 B.
 的质量分数不随时间变化而变化
的质量分数不随时间变化而变化C.混合气体的总物质的量不随时间变化而变化
D.

E.

F.单位时间内每消耗
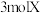 ,同时生成
,同时生成
您最近一年使用:0次
10 . 对于在一定条件下的密闭容器中进行的反应 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.将木炭磨成粉末可以加快反应速率 | B.升高温度可以加快反应速率 |
C.容器体积不变时,向其中充入 ,反应速率不变 ,反应速率不变 | D.容器中物质总质量不变可说明反应达到平衡 |
您最近一年使用:0次