名校
1 . 一定温度下,在2个容积均为1L的恒容密闭容器中,加入一定量的反应物,发生反应: △H<0,相关数据见下表。
△H<0,相关数据见下表。
下列说法不正确 的是
 △H<0,相关数据见下表。
△H<0,相关数据见下表。容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
|
|
| ||
Ⅰ |
| 0.2 | 0.2 | 0.1 |
Ⅱ |
| 0.2 | 0.2 | 0.12 |
| A.T1>T2 |
| B.达到平衡所需要的时间:Ⅰ<Ⅱ |
| C.Ⅱ中反应达到平衡时,NO的转化率为60% |
| D.对于Ⅰ,平衡后向容器中再充入0.2mol CO和0.2mol CO2,平衡正向移动 |
您最近一年使用:0次
名校
解题方法
2 . 一定条件下,在甲、乙两个恒容密闭容器(容器容积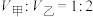 )中投入等物质的量的X和Y,发生反应
)中投入等物质的量的X和Y,发生反应 ,达到平衡时,Q的物质的量浓度与温度和容器容积的关系如图所示。下列说法正确的是
,达到平衡时,Q的物质的量浓度与温度和容器容积的关系如图所示。下列说法正确的是
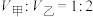 )中投入等物质的量的X和Y,发生反应
)中投入等物质的量的X和Y,发生反应 ,达到平衡时,Q的物质的量浓度与温度和容器容积的关系如图所示。下列说法正确的是
,达到平衡时,Q的物质的量浓度与温度和容器容积的关系如图所示。下列说法正确的是
| A.x+y>p+q | B.c(P):b>2a |
| C.压强:2p(b)<p(c) | D.平衡常数: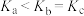 |
您最近一年使用:0次
解题方法
3 . 某研究学习小组把一定量的固体X放入容积为2L的真空密闭容器中,在 下分解:
下分解: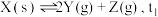 时达到化学平衡,
时达到化学平衡,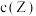 随时间t变化曲线(
随时间t变化曲线( 时间段)如图所示.下列说法错误的是
时间段)如图所示.下列说法错误的是
 下分解:
下分解: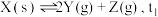 时达到化学平衡,
时达到化学平衡,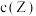 随时间t变化曲线(
随时间t变化曲线( 时间段)如图所示.下列说法错误的是
时间段)如图所示.下列说法错误的是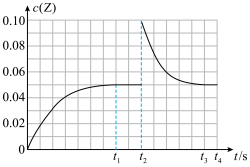
A.在 时间内该化学反应速率 时间内该化学反应速率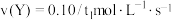 |
| B.T℃时,该反应的化学平衡常数K的值为0.0005 |
| C.Z的体积分数不变证明该分解反应已经达到平衡 |
D.若其他条件不变, 时将容器体积压缩到1L, 时将容器体积压缩到1L, 时达到新的平衡,c(Z)在 时达到新的平衡,c(Z)在 时间内的变化曲线如上图所示 时间内的变化曲线如上图所示 |
您最近一年使用:0次
2024-05-28更新
|
142次组卷
|
2卷引用:河北省衡水市2024届高三下学期高考预测卷化学试题
4 . 下列化学反应表示错误的是
A. 与NaOH溶液反应: 与NaOH溶液反应: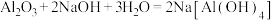 |
B.碱性锌锰电池的正极反应: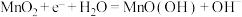 |
C.向蓝色 溶液中加入浓NaCl溶液,发生反应: 溶液中加入浓NaCl溶液,发生反应: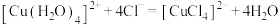 |
D.苯甲酰胺在盐酸中水解: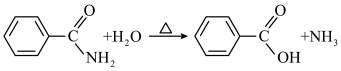 |
您最近一年使用:0次
名校
解题方法
5 .  和
和 联合重整能减少温室气体的排放。
联合重整能减少温室气体的排放。 联合
联合 和
和 制取
制取 时,发生的主要反应如下:
时,发生的主要反应如下:
①
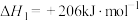
②
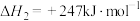
将 、
、 和
和 按一定比例通入填充有催化剂的恒容反应器,在不同温度下(均在催化剂活性范围内),反应相同时间内(反应均未达到化学平衡状态)测得
按一定比例通入填充有催化剂的恒容反应器,在不同温度下(均在催化剂活性范围内),反应相同时间内(反应均未达到化学平衡状态)测得 的值如图所示。下列说法正确的是
的值如图所示。下列说法正确的是
 和
和 联合重整能减少温室气体的排放。
联合重整能减少温室气体的排放。 联合
联合 和
和 制取
制取 时,发生的主要反应如下:
时,发生的主要反应如下:①

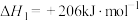
②

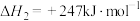
将
 、
、 和
和 按一定比例通入填充有催化剂的恒容反应器,在不同温度下(均在催化剂活性范围内),反应相同时间内(反应均未达到化学平衡状态)测得
按一定比例通入填充有催化剂的恒容反应器,在不同温度下(均在催化剂活性范围内),反应相同时间内(反应均未达到化学平衡状态)测得 的值如图所示。下列说法正确的是
的值如图所示。下列说法正确的是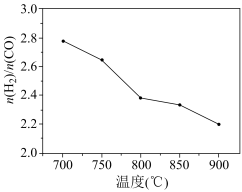
A.由①②可知,  |
| B.随着温度的升高,温度对反应①速率的影响大于对反应②速率的影响 |
C.其他条件不变时,升高温度,①②反应的 、 、 、 、 均增大 均增大 |
D.其他条件不变时,增大原料中 的浓度可以提高产物中 的浓度可以提高产物中 的值 的值 |
您最近一年使用:0次
解题方法
6 . 已知:
Ⅰ.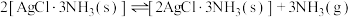 ;
;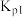
Ⅱ.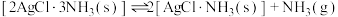 ;
;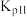
Ⅲ.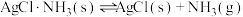 ;
;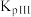
0℃,真空恒容密闭容器中,选择合适的固体试剂E,只吸收氨气,速率较慢。忽略E及其产物,体系中固体组成表示为: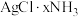 。测定
。测定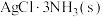 的逐级分解的体系中x与体系压强(p)的关系如图。下列说法不正确的是
的逐级分解的体系中x与体系压强(p)的关系如图。下列说法不正确的是
Ⅰ.
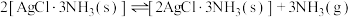 ;
;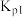
Ⅱ.
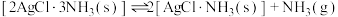 ;
;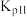
Ⅲ.
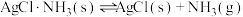 ;
;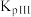
0℃,真空恒容密闭容器中,选择合适的固体试剂E,只吸收氨气,速率较慢。忽略E及其产物,体系中固体组成表示为:
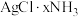 。测定
。测定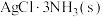 的逐级分解的体系中x与体系压强(p)的关系如图。下列说法不正确的是
的逐级分解的体系中x与体系压强(p)的关系如图。下列说法不正确的是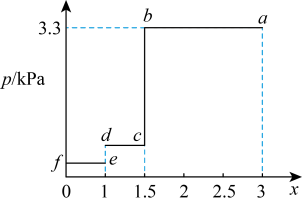
A.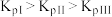 |
B.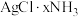 最终以 最终以 存在 存在 |
C.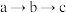 过程中, 过程中,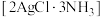 的质量先增多,后不变 的质量先增多,后不变 |
D.若固体试剂E失效,可向容器中缓慢通入 ,使反应物继续分解 ,使反应物继续分解 |
您最近一年使用:0次
名校
7 . 二水合重铬酸钠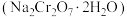 是重要的工业氧化剂,工业上可由铬铁矿(主要成分为
是重要的工业氧化剂,工业上可由铬铁矿(主要成分为 ,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
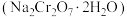 是重要的工业氧化剂,工业上可由铬铁矿(主要成分为
是重要的工业氧化剂,工业上可由铬铁矿(主要成分为 ,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
| A.“焙烧”时,纯碱的作用是将铝、硅、铬元素转化为可溶性钠盐 |
B.滤渣1的主要成分是 、 、 |
C.“调 ”的目的是除去含铝、硅元素的杂质 ”的目的是除去含铝、硅元素的杂质 |
D.“转化”的目的是将 转化为 转化为 |
您最近一年使用:0次
8 . 下列事实不能 用平衡移动原理解释的是
A.FeS可用于除去废水中的 |
| B.25℃~100℃,随温度升高,纯水的pH减小 |
C.加热 溶液,液体由黄色变为红褐色 溶液,液体由黄色变为红褐色 |
D.  ,采用高温提高单位时间内 ,采用高温提高单位时间内 的产率 的产率 |
您最近一年使用:0次
名校
9 . 向碘水、淀粉的混合液中加入 溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
 溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
溶液,蓝色褪去。为探究褪色原因,设计如下图所示的实验。
A.①中 氧化了 氧化了 | B.①后溶液pH可能明显变小 |
C.③的目的是除去过量的 溶液 溶液 | D.④可发生 |
您最近一年使用:0次
解题方法
10 . 已知反应: .按起始投料比
.按起始投料比 加入反应物,测得
加入反应物,测得 的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
 .按起始投料比
.按起始投料比 加入反应物,测得
加入反应物,测得 的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
的平衡转化率和催化剂催化效率受温度的影响如下图所示.下列说法不正确的是
A. 时,b点反应向逆反应方向进行 时,b点反应向逆反应方向进行 |
| B.生成乙烯的速率c点一定大于a点 |
C. ,催化效率降低是由于温度升高引起的 ,催化效率降低是由于温度升高引起的 |
D.a点乙烯的体积分数约为 |
您最近一年使用:0次








