1 . 已知:重铬酸钾( )具有强氧化性,其还原产物
)具有强氧化性,其还原产物 在水溶液中呈绿色。在
在水溶液中呈绿色。在 溶液中存在下列平衡:
溶液中存在下列平衡: (橙色)
(橙色) (黄色)
(黄色) 。用
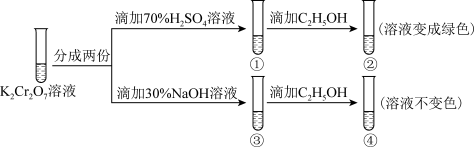
。用 溶液进行如图所示实验,下列说法不正确的是
溶液进行如图所示实验,下列说法不正确的是
 )具有强氧化性,其还原产物
)具有强氧化性,其还原产物 在水溶液中呈绿色。在
在水溶液中呈绿色。在 溶液中存在下列平衡:
溶液中存在下列平衡: (橙色)
(橙色) (黄色)
(黄色) 。用
。用 溶液进行如图所示实验,下列说法不正确的是
溶液进行如图所示实验,下列说法不正确的是
| A.①中溶液橙色加深,③中溶液变为黄色 |
B.②中 被 被 还原 还原 |
C.对比②和④可知, 酸性溶液氧化性强 酸性溶液氧化性强 |
D.若向④中加入70% 溶液至过量,溶液变为橙色 溶液至过量,溶液变为橙色 |
您最近一年使用:0次
2022-09-04更新
|
855次组卷
|
91卷引用:山西省临汾市2020届高三上学期第二次月考化学试题
山西省临汾市2020届高三上学期第二次月考化学试题2016年全国普通高等学校招生统一考试化学(北京卷精编版)2017届河北省沧州市第一中学高三上周测化学试卷2017届河南省开封市高三上学期10月定位考试化学试卷2017届江西省鹰潭市第一中学高三上学期第四次月考化学试卷2016-2017学年辽宁东北育才学校高二上阶段考二化学卷2017届宁夏固原一中高三上适应性训练四化学卷2017届河北省冀州中学高三(高复班)上学期一轮检测(二)化学试卷安徽省淮北市第一中学2016-2017学年高二下学期期中考试化学试题福建省福州市第八中学2016-2017学年高二下学期期中考试化学试题辽宁省葫芦岛市2017届高三第二次模拟考试(5月)化学试题山东省泰安市第一中学2016-2017学年高一下学期学情检测化学试题黑龙江省哈尔滨市第六中学2016-2017学年高二6月月考化学试题辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷2018版化学(苏教版)高考总复习对接高考精练--氧化还原反应基础黑龙江省哈尔滨市第六中学2018届高三9月阶段检测化学试题辽宁省大连育明高级中学2018届高三人教版选修四同步测试化学试题河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第一次月考化学试题吉林省实验中学2018届高三上学期第二次月考化学试题吉林省长春市2018届高三上学期第二次月考化学试题北京市八一中学2016-2017学年高二上学期期中考试化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题(实验班)内蒙古巴彦淖尔市第一中学2018届高三12月月考理科综合化学试题江西省抚州市临川区第一中学2017-2018学年高二12月月考化学试题(已下线)学科网2019年高考化学一轮复习讲练测2.3 氧化还原反应的基本概念 练福建省厦门市湖滨中学2019届高三上学期第一次阶段检测化学试题陕西省渭南市尚德中学2019届高三上学期第一次教学质量检测化学试题山西省运城市河津二中2018-2019学年高二上学期9月月考化学试题【全国百强校】四川省彭州中学2018-2019学年高二上学期10月月考化学试题浙江省诸暨中学2018-2019学年高二上学期10月(期中)阶段性考试实验班化学试题【全国百强校】湖南省衡阳市第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)2016年全国普通高等学校招生统一考试化学(北京卷参考版)云南省腾冲市第八中学2018-2019学年高二下学期期中考试化学试题河北省迁西县第一中学2019-2020学年高二10月月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题浙江省宁波市北仑中学2019-2020学年高二上学期期中考试化学(2-10班)试题湖北省沙市中学2019-2020学年高二上学期期中考试化学(选考)试题河北省张家口市第一中学2019-2020学年高二12月月考化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的综合分析夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用夯基提能2020届高三化学选择题对题专练——氧化还原反应(强化练习)夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学平衡移动及其影响因素(强化练习)专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期末考试化学试题河北省保定市2019-2020学年高二上学期期末调研考试化学试题(已下线)专题四 氧化还原反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)专题十一 化学反应速率和化学平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训河北省衡水中学2020届高三四月份质量监测理综化学试题湖南长沙长郡中学2020届高三2月份网络教学质量监测卷理综化学试题湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题吉林省长春市东北师大附中2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分山西省运城市新绛中学2021届高三上学期8月月考化学试题河北省衡水市桃城区第十四中学2021届高三上学期一调考试化学试题四川省宜宾翠屏棠湖学校2020-2021学年高二上学期10月月考化学试题山西省太原市第五中学2020-2021学年高二上学期10月月考试题湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题重庆市第一中学校2020-2021高三上学期第一次月考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题山西省太原市2020-2021学年高二上学期期中质量监测化学(理)试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题四川省成都市金堂县竹篙中学2020-2021学年高二10月月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研化学试题上海市嘉定区2021届高三一模化学试题安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题广东省汕尾市2020-2021学年高二上学期期末学业质量监测化学试题河北省衡水市第十四中学2020-2021学年高二上学期期末考试化学试题广东省韶关市2021届高三综合测试化学试题(已下线)考点32 化学反应条件的控制-备战2022年高考化学一轮复习考点帮(浙江专用)广东省深圳市西乡中学2021-2022学年高二上学期期中考试化学试题上海市徐汇中学2021-2022学年高三上学期期中考试化学试题(已下线)专题05 氧化还原反应-2022年高考化学二轮复习重点专题常考点突破练湖南省株洲市九方中学2022届高三下学期4月月考化学试题第二节 化学平衡 第3课时 影响化学平衡的因素内蒙古包头市第四中学2020-2021学年高二上学期期中考试化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题新疆维吾尔自治区喀什市喀什第二中学2022-2023学年高三上学期网上11月月考化学试题广东省中山市小榄中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题四 氧化还原反应-实战高考·二轮复习核心突破(已下线)化学预测卷(六)-预测卷(浙江专版)(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素四川省资阳中学2022-2023学年高二上学期期末考试化学试题(已下线)T13-实验方案的设计与评价(已下线)考点04 氧化还原反应的基本概念和规律(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)四川省绵阳市南山中学实验学校2022-2023学年高二下学期3月月考化学试题广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题北京市第一○一中学2023-2024学年高二上学期统练一化学试题北京市首都师范大学附属中学2022-2023学年高三上学期开学测试化学试题北京市日坛中学2023-2024学年高三上学期10月检测化学试题云南省大理市下关第一中学2023-2024学年高二上学期11月期中考试化学试题
10-11高二下·江苏南京·期中
名校
2 . 下列对化学平衡移动的分析中,不正确 的是
①已达平衡的反应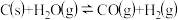 ,当增加反应物的物质的量时,平衡一定向正反应方向移动
,当增加反应物的物质的量时,平衡一定向正反应方向移动
②已达平衡的反应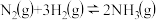 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
①已达平衡的反应
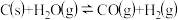 ,当增加反应物的物质的量时,平衡一定向正反应方向移动
,当增加反应物的物质的量时,平衡一定向正反应方向移动②已达平衡的反应
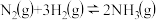 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
2021-11-19更新
|
442次组卷
|
71卷引用:2014-2015学年山西省曲沃中学校高二上学期期中化学试卷
2014-2015学年山西省曲沃中学校高二上学期期中化学试卷(已下线)2010—2011学年江苏省南京六中高二下学期期中考试化学试题(已下线)2010-2011年云南省玉溪一中高二下学期期末考试化学试卷(已下线)2011-2012学年浙江省浙东北三校高二下学期期中联考化学试卷(已下线)2012-2013学年江苏省江都区丁沟中学高二下学期期中考试化学试卷(已下线)2013-2014学年贵州省册亨县民族中学高二上学期期末考试化学试卷(已下线)2014-2015学年甘肃省兰州一中高二上学期期中考试化学卷2014-2015吉林省松原市扶余县一中高二上学期期末化学试卷2015-2016学年河南省鄢陵高级中学高二上学期第二次月考化学试卷2015-2016学年江西省上高二中高二上二次月考化学试卷2015-2016学年江西省上高二中高二上第二次月考化学试卷2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷2015-2016学年广东省深圳市明德外语学校高二上学期期中理化学试卷2015-2016学年浙江省杭州二中高二上学期期末化学试卷2015-2016学年四川省彭州中学高二下2月月考化学试卷2015-2016学年河北省邢台一中高一下期中化学试卷2016-2017学年河北冀州中学高二上第一次月考化学试卷2016-2017学年宁夏育才中学高二上第一次月考化学卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷2017届黑龙江省哈尔滨市第六中学高三上学期期中考试化学试卷2016-2017学年甘肃省兰州一中高二上期中理化学试卷2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷甘肃省临夏中学2016-2017学年高二上学期期末考试化学试题河北省张家口市第一中学2016-2017学年高一(衔接班)下学期期末考试(理)化学试题陕西省黄陵中学2016-2017学年高一(重点班)下学期期末考试化学试题山西省运城市康杰中学2017-2018学年高二上学期第一次月考化学试题河南省中原名校(即豫南九校)2017-2018学年高二上学期第一次联考化学试题山西省太原市小店区2017—2018学年高二化学上学期10月月考试题山西大学附属中学2017-2018学年高二上学期10月模块诊断化学试题陕西煤铜川市炭建设公司第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】四川省棠湖中学2018-2019学年高二上学期期中考试理综-化学试题【全国百强校】海南省海南中学2017-2018学年高二(理)上学期期末考试化学试题西藏自治区日喀则市南木林高级中学2018-2019学年高二上学期期中考试化学试题吉林省白城市第一中学2018-2019学年高一6月月考化学试题湖北省孝感高级中学2019-2020学年高二9月调研化学试题江西省宜春市上高二中2019-2020学年高二上学期第二次月考化学试题河南省南阳市第一中学2019-2020学年高二上学期第四次月考化学试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题西藏自治区日喀则市南木林高级中学2019-2020学年高二上学期期中化学试题湖南省常德市石门县第二中学2019-2020学年高二上学期第二次月考化学试题云南省文山马关实验高级中学2019-2020学年高二期末考试化学试题河南省周口市扶沟县包屯高中2019---2020学年高二上期期末考试化学试题湖北省黄石市2018-2019学年高二上学期期末质量监测考试化学试题辽宁省大连市庄河市高级中学2019-2020学年高二下学期5月网上月考化学试题宁夏石嘴山市第三中学2019-2020学年高一下学期期中考试化学试题陕西省咸阳市实验中学2019-2020学年高二上学期第二次月考化学试题黑龙江省伊春市伊美区第二中学2019-2020学年高二上学期开学考试化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 教材帮四川省宜宾翠屏棠湖学校2020-2021学年高二上学期10月月考化学试题甘肃省庄浪县第一中学2020-2021学年高二上学期第二学段考试化学试题湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题内蒙古呼和浩特市第十六中学2020-2021学年高二上学期第一次质量检测化学试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP415(2)】【化学】青海省北外附属西宁新华联国际学校2020-2021学年高二上学期期末考试化学试题山西省寿阳县第一中学2020—2021学年高二上学期第二次月考化学试题甘肃省民勤县第四中学2020-2021学年高二下学期开学考试化学试题陕西省西安市高新一中2020-2021学年高一下学期5月月考化学试题黑龙江嫩江市高级中学等八校2021-2022学年高二上学期9月联合考试化学试题河北省保定市定州市2021-2022学年高二上学期期中考试化学试题广东省高州市校际2021-2022学年高二11月联考化学试题江西省吉安市永新中学2021-2022学年高二上学期期中考试化学(理科)试题四川省广安代市中学校2021-2022学年高二上学期第一次月考化学试题四川省广安代市中学校2021-2022学年上学期高二第三次月考化学试题福建省建瓯市芝华中学2021-2022学年高二上学期期中考试化学试题天津市第二十五中学2022-2023 学年高二上学期期末阶段测试化学试题天津市和平区2017-2018学年高二上学期期中质量调查化学试题重庆市荣昌永荣中学校2021-2022学年高二上学期期中考试化学试题作业(八) 浓度、压强对化学平衡的影响第2课时 温度、浓度对化学平衡的影响
3 . 将0.4molN2O4充入2L固定容积的密闭容器中发生反应:N2O4(g) 2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
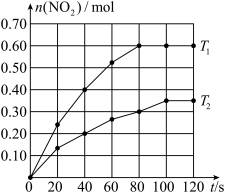
(1)该反应的△H_______ (填“>”“<”或“=”)0,理由是_______ 。
(2) T1时,40~80s内用N2O4的浓度变化表示的反应速率为_______ mol·L-1·s-1。
(3) T1时,反应的平衡常数K=_______ 。恒温恒容条件下,下列能说明该反应达到平衡状态的是_______ (填序号)。
①v(NO2)=2v(N2O4);②反应体系的总压强保持恒定不变;③混合气体的密度保持恒定不变;④体系颜色保持不变;⑤容器内NO2和N2O4的浓度相等
(4)T2时,改变条件使反应重新达到平衡时, 的值变小,则采取的措施可能是_______(填字母)。
的值变小,则采取的措施可能是_______(填字母)。
 2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
(1)该反应的△H
(2) T1时,40~80s内用N2O4的浓度变化表示的反应速率为
(3) T1时,反应的平衡常数K=
①v(NO2)=2v(N2O4);②反应体系的总压强保持恒定不变;③混合气体的密度保持恒定不变;④体系颜色保持不变;⑤容器内NO2和N2O4的浓度相等
(4)T2时,改变条件使反应重新达到平衡时,
 的值变小,则采取的措施可能是_______(填字母)。
的值变小,则采取的措施可能是_______(填字母)。| A.增大 N2O4的起始浓度 | B.升高温度 |
| C.向混合气体中通入NO2 | D.使用高效催化剂 |
您最近一年使用:0次
2023-02-11更新
|
131次组卷
|
2卷引用:山西省临汾市2022-2023学年高二下学期开学考试化学试题
名校
4 . 一定量的混合气体在密闭容器中发生反应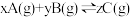 ,达到平衡后测得A的浓度为
,达到平衡后测得A的浓度为 ,保持温度不变,将密闭容器的容积压缩为原来的一半,再次达到平衡后,测得A的浓度为
,保持温度不变,将密闭容器的容积压缩为原来的一半,再次达到平衡后,测得A的浓度为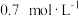 ,则下列叙述正确的是
,则下列叙述正确的是
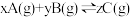 ,达到平衡后测得A的浓度为
,达到平衡后测得A的浓度为 ,保持温度不变,将密闭容器的容积压缩为原来的一半,再次达到平衡后,测得A的浓度为
,保持温度不变,将密闭容器的容积压缩为原来的一半,再次达到平衡后,测得A的浓度为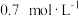 ,则下列叙述正确的是
,则下列叙述正确的是| A.C的体积分数降低 | B.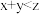 |
| C.B的物质的量浓度减小 | D.平衡向正反应方向移动 |
您最近一年使用:0次
名校
5 . 如图表示可逆反应:N2+3H2 2NH3,ΔH<0达到平衡状态时,受外界因素影响导致平衡移动的曲线,据此判断影响此平衡移动的因素是
2NH3,ΔH<0达到平衡状态时,受外界因素影响导致平衡移动的曲线,据此判断影响此平衡移动的因素是

 2NH3,ΔH<0达到平衡状态时,受外界因素影响导致平衡移动的曲线,据此判断影响此平衡移动的因素是
2NH3,ΔH<0达到平衡状态时,受外界因素影响导致平衡移动的曲线,据此判断影响此平衡移动的因素是
| A.增大反应物的浓度,同时减小生成物的浓度 |
| B.减小压强,同时降温 |
| C.增大反应物浓度,使用催化剂 |
| D.升高温度,同时加压 |
您最近一年使用:0次
2021-12-03更新
|
81次组卷
|
2卷引用:山西省侯马市第一中学校2021-2022年高二上学期期中测试化学试题
名校
6 . 下列事实,不能用勒夏特列原理解释的是
| A.溴水中有如下平衡:Br2+H2O⇋HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 |
| B.合成NH3反应,为提高NH3的产率,理论上应采取相对较低温度的措施 |
| C.氯气在水中的溶解度大于在饱和食盐水中的溶解度 |
| D.对CO(g)+NO2(g)⇋CO2(g)+NO(g)平衡体系增大压强可使颜色变深 |
您最近一年使用:0次
10-11高二上·吉林·阶段练习
7 . 在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:2A(g)+B(g) 3C(g)+D(g)
3C(g)+D(g)
达到平衡时,C的浓度为W mol·L-1.若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度与W的关系(用“>”“<”“=”表示)。
(1)加入1 mol A和1 mol B时,C的平衡浓度_______ W mol·L-1。
(2)加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度_______ W mol·L-1。
(3)加入3 mol C和1 mol D时,C的平衡浓度_______ W mol·L-1。
(4)加入2 mol B、3 mol C、1 mol D时,C的平衡浓度_______ W mol·L-1。
 3C(g)+D(g)
3C(g)+D(g)达到平衡时,C的浓度为W mol·L-1.若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度与W的关系(用“>”“<”“=”表示)。
(1)加入1 mol A和1 mol B时,C的平衡浓度
(2)加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度
(3)加入3 mol C和1 mol D时,C的平衡浓度
(4)加入2 mol B、3 mol C、1 mol D时,C的平衡浓度
您最近一年使用:0次
11-12高一下·山西临汾·期中
8 . 判断下列说法是否正确。
1.一个D2O分子所含的中子数为8。_______
2.HI、HBr、HCl、HF的稳定性依次增强。_______
3.同主族元素从上到下,单质的熔点逐渐降低。_______
4.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。_______
5.从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。_______
6.将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。_______
7.在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。_______
8.二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。_______
9.用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。_______
10.苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。_______
1.一个D2O分子所含的中子数为8。
2.HI、HBr、HCl、HF的稳定性依次增强。
3.同主族元素从上到下,单质的熔点逐渐降低。
4.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。
5.从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。
6.将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。
7.在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。
8.二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。
9.用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。
10.苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。
您最近一年使用:0次



