名校
解题方法
1 . 10mL0.1mol•L-1KI溶液与5mL0.1mol•L-1FeCl3溶液发生反应:2Fe3+(aq)+2I-(aq)⇌2Fe2+(aq)+I2(aq),达到平衡。下列说法不正确的是
| A.加入少量氯化钾固体,平衡不移动 |
| B.加适量水稀释,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该反应是可逆反应 |
D.该反应的平衡常数K=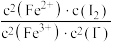 |
您最近半年使用:0次
2022-04-01更新
|
492次组卷
|
12卷引用:浙江省2021届高三下学期3月联考化学试题
浙江省2021届高三下学期3月联考化学试题(已下线)浙江省“超级全能生”2021年3月高考选考科目联考化学试题(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)课时3影响化学平衡的因素随堂练习
2 . 5 mL 0.1mol·L−1KI溶液与10 mL 0.1 mol·L−1FeCl3溶液发生反应:2Fe3+(aq)+2I−(aq) 2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是
 2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡。下别说法不正确的是| A.加入一定量铁粉,平衡逆向移动 |
| B.向该水溶液中加入CCl4,振荡,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该化学反应存在限度 |
D.该反应的平衡常数K= |
您最近半年使用:0次
名校
解题方法
3 . 已知难溶性化合物 的化学式为
的化学式为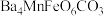 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。
(1) 高温下在
高温下在 气流中的反应
气流中的反应________ 氧化还原反应(填“属于”或“不属于”), 中钡元素的化合价为
中钡元素的化合价为________ 。
(2)步骤Ⅳ可以进行的原因除了生成 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因________ 。
(3)下列说法正确的是________。
(4)固体 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式________ 。
(5)设计实验检验混合气体A(除 外)的成份
外)的成份________ 。
 的化学式为
的化学式为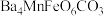 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。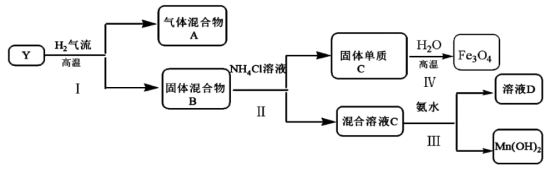
 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。(1)
 高温下在
高温下在 气流中的反应
气流中的反应 中钡元素的化合价为
中钡元素的化合价为(2)步骤Ⅳ可以进行的原因除了生成
 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因(3)下列说法正确的是________。
A.溶液D中阳离子只有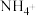 |
| B.若磁铁能吸引反应Ⅳ的剩余固体,则证明铁有剩余 |
| C.步骤Ⅱ中的氯化铵溶液也可以用盐酸代替 |
D.依据步骤Ⅲ可知碱性强弱 |
 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式(5)设计实验检验混合气体A(除
 外)的成份
外)的成份
您最近半年使用:0次
解题方法
4 . 下列实验操作、实验现象以及所得出的结论均正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向 和KSCN混合溶液中,加入少量KCl的固体 和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 |  平衡向逆反应方向移动 平衡向逆反应方向移动 |
| B | 用广泛pH试纸测定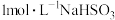 溶液的酸碱性 溶液的酸碱性 | 测得pH=3.2 |  溶液呈酸性,证明 溶液呈酸性,证明 在水中的电离程度大于水解程度 在水中的电离程度大于水解程度 |
| C | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | 酸的强弱:HX<HY |
| D | 向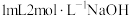 溶液中先滴加2滴 溶液中先滴加2滴 溶液,再滴加2滴 溶液,再滴加2滴 溶液 溶液 | 先生成白色沉淀,后生成红褐色沉淀 | 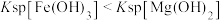 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 下列实验装置,可以达到实验目的的是
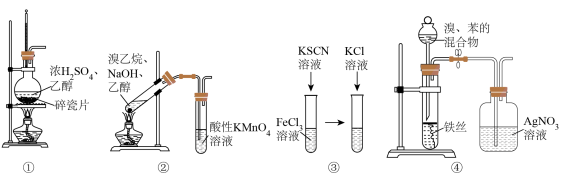

| A.用装置①在实验室制备乙烯 |
| B.用装置②证明溴乙烷消去反应有乙烯生成 |
C.用装置③探究KCl浓度是否对FeCl3+3KSCN Fe(SCN)3+3KCl的平衡移动有影响 Fe(SCN)3+3KCl的平衡移动有影响 |
| D.用装置④证明溴和苯发生的是取代反应而不是加成反应 |
您最近半年使用:0次
6 . 下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 检验铜和浓硫酸反应之后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入盐酸和BaCl2溶液 | 若出现白色沉淀,则硫酸剩余 |
| B | 探究淀粉在酸性条件下的水解程度 | 取少量淀粉溶液,加入适量稀硫酸加热5min后,再加NaOH中和硫酸,最后滴加碘水 | 溶液无明显现象,则淀粉完全水解 |
| C | 比较CH3COOH和HClO的酸性强弱 | 相同条件下分别用pH试纸测定0.1mol•L-1CH3COONa溶液、0.1mol•L-1NaClO溶液的pH | NaClO溶液pH>CH3COONa溶液的pH,证明CH3COOH的酸性比HClO的酸性强 |
| D | 探究浓度对化学平衡的影响 | 在4mL0.1mol•L-1K2Cr2O7溶液中加入数滴1mol•L-1NaOH溶液 | 若溶液由橙色变为黄色,则H+浓度减小,Cr2O +H2O +H2O 2CrO 2CrO +2H+平衡正移 +2H+平衡正移 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究食用盐是否含碘 | 取粥汤,加入足量食用盐 | 若不变蓝,则不含碘元素 |
| B | 探究火柴头中是否含有 | 火柴头浸泡液中加 溶液和 溶液和 溶液 溶液 | 若有白色沉淀产生则含有 |
| C | 检验乙醇消去反应的产物中有乙烯 | 加热乙醇与 的混合物,将产生的气体通过溴水 的混合物,将产生的气体通过溴水 | 若溴水褪色,则产物中含有乙烯 |
| D | 探究氯化钴溶液的变色原理 | 0.5 溶液中滴入浓盐酸 溶液中滴入浓盐酸 | 若溶液的颜色由蓝色变成粉红色则证明氯化钴溶液中存在平衡 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 下列方案设计、现象和结论不正确 的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 鉴别NaNO2溶液和NaCl溶液 | 分别取适量未知溶液于两支试管中,分别滴加1~2滴AgNO3溶液,再加入稀硝酸 | 出现白色沉淀并溶于稀硝酸的试管对应的原溶液为NaNO2溶液 |
| B | 探究不同催化剂对H2O2分解速率的影响 | 常温下将质量均为0.1g粉末状的MnO2、Fe2O3分别同时与5mL6%的H2O2溶液反应 | 观察到用MnO2催化时放出的气泡速率快,说明不同催化剂对同种物质的催化效果不同 |
| C | 探究浓度对化学平衡的影响 | 向稀的氯化钴溶液加入少量NaCl固体(提示:溶液中存在平衡:[Co(H2O)6]2+(粉红色)+4Cl- [CoCl4]2-(蓝色)+6H2O) [CoCl4]2-(蓝色)+6H2O) | 溶液由粉红色变为蓝色,说明增加反应物的浓度,反应向正向移动 |
| D | 证明丙烯醛(CH2=CHCHO)分子中的碳碳双键 | 取适量丙烯醛于试管中,向其中加入少量溴水 | 溴水褪色,说明丙烯醛分子中含有碳碳双键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 验证压强对化学平衡的影响 | 先将注射器充满 气体,然后将活塞往里推压缩体积 气体,然后将活塞往里推压缩体积 | 观察到注射器内气体颜色加深,证明加压平衡朝生成 气体的方向移动 气体的方向移动 |
| B | 探究反应物浓度对化学反应速率的影响 | 分别取 溶液和 溶液和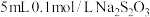 溶液、 溶液、 蒸馏水于两支试管中,然后同时加入 蒸馏水于两支试管中,然后同时加入 溶液 溶液 | 前者出现浑浊的时间更短,说明增大 浓度,可以加快反应速率 浓度,可以加快反应速率 |
| C | 鉴别 和 和 溶液 溶液 | 分别取少量溶液于试管中,再滴加 酸性溶液 酸性溶液 | 若溶液由橙色变为绿色,则该溶液为 溶液 溶液 |
| D | 检验某无色溶液中是否含有 | 取适量该溶液于试管中,加入少量氯水,再加 ,振荡,静置 ,振荡,静置 | 溶液分层,两层均无色,则该溶液中无 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2020高三·全国·专题练习
解题方法
10 . 下列相关实验能达到预期目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 可逆反应FeCl3(aq)+3KSCN(aq)⇌Fe(SCN)3(aq)+3KCl(aq)建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化 | 验证浓度对化学平衡的影响 |
| B | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和硫酸中,观察气泡产生的快慢 | 验证固体接触面积对化学反应速率的影响 |
| C | 相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量MnO2固体 | 验证不同催化剂对H2O2分解速率的影响 |
| D | 将SO2气体通入溴水中,观察溶液颜色的变化 | 证明SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



