1 . 利用含钴废料(主要成分为 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: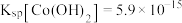 ;
;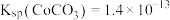 。
。
请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为 和
和___________ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为___________ 。
(2)“萃取”时 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)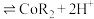 ,若萃取剂的量一定时,
,若萃取剂的量一定时,___________ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。若“酸浸”后浸出液的 ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为___________ (结果保留一位小数,溶液体积变化忽略不计)。
(3)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为___________ 。
(4)可以通过电解 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是___________ 。若Ⅱ室溶液中溶质的质量增加了 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为___________ 。
 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: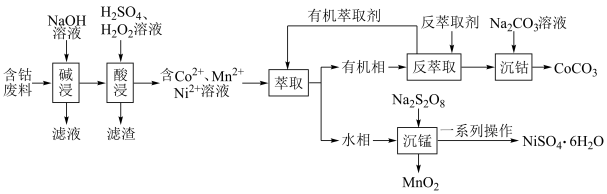
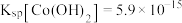 ;
;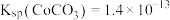 。
。请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为
 和
和 发生反应的总离子方程式为
发生反应的总离子方程式为(2)“萃取”时
 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)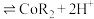 ,若萃取剂的量一定时,
,若萃取剂的量一定时, ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为(3)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为(4)可以通过电解
 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为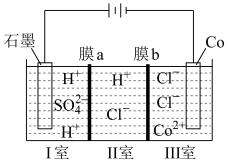
您最近一年使用:0次
2 . 重铬酸钾溶液中存在如下平衡:H2O+Cr2O (aq,橙色)
(aq,橙色) 2CrO
2CrO (aq,黄色)+2H+(aq)。下列说法正确的是
(aq,黄色)+2H+(aq)。下列说法正确的是
 (aq,橙色)
(aq,橙色) 2CrO
2CrO (aq,黄色)+2H+(aq)。下列说法正确的是
(aq,黄色)+2H+(aq)。下列说法正确的是A.该反应的平衡常数的表达式为K= |
| B.加水稀释重铬酸钾溶液,所有离子浓度均减小 |
| C.向橙黄色的重铬酸钾溶液中滴加足量的氢氧化钠溶液,溶液变为橙色 |
| D.由于Ag2CrO4难溶于水,向重铬酸钾溶液中滴加AgNO3溶液,溶液的pH值减小 |
您最近一年使用:0次
3 . 已知CO和NO能发生反应: ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是
 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是| A.升高温度会减小正反应速率 |
| B.平衡时增大CO的浓度能增大逆反应速率 |
| C.当上述可逆反应达到平衡时,NO的转化率为100% |
D.当上述可逆反应达到平衡时,体系中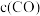 与 与 一定相等 一定相等 |
您最近一年使用:0次
2022-06-29更新
|
124次组卷
|
3卷引用:陕西省安康市2021-2022学年高二下学期期末考试化学试题
4 . 在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是




 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是



| A.依据图a可判断正反应为吸热反应 |
| B.在图b中,虚线可表示压强增大 |
| C.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0 |
| D.若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动 |
您最近一年使用:0次
2021-10-22更新
|
189次组卷
|
2卷引用:陕西省安康市白河高中2021-2022学年高二上学期期末考试(实验班)化学试题
名校
解题方法
5 . 下列实验方案不能达到相应目的的是
| A | B | C | D | |
| 目的 | 探究温度对化学平衡的影响 | 研究浓度对化学平衡的影响 | 实现铜棒镀银 | 证明化学反应存在一定的限度 |
| 实验方案 | 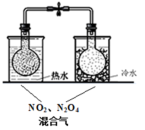 | 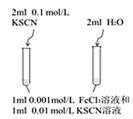 | 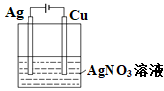 | 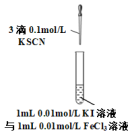 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-13更新
|
277次组卷
|
4卷引用:陕西省安康市六校联考2021-2022学年高二上学期期末考试化学试题
名校
6 . 已知反应: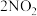 (红棕色)
(红棕色)
 (无色),分别进行如下两个实验:
(无色),分别进行如下两个实验:
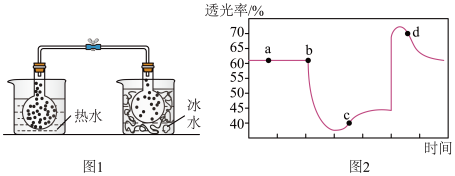
实验ⅰ:将 球分别浸泡在热水和冰水中,现象如图1。
球分别浸泡在热水和冰水中,现象如图1。
实验ⅱ:将一定量的 充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(
充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小 ),如图2。下列说法不正确 的是( )
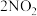 (红棕色)
(红棕色)
 (无色),分别进行如下两个实验:
(无色),分别进行如下两个实验:实验ⅰ:将
 球分别浸泡在热水和冰水中,现象如图1。
球分别浸泡在热水和冰水中,现象如图1。实验ⅱ:将一定量的
 充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(
充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(
| A.图1现象说明该反应为放热反应 |
| B.图2中b点的操作是压缩注射器 |
C.d点: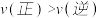 |
| D.若不忽略体系温度变化,且没有能量损失,则T(b)<T(c) |
您最近一年使用:0次
2020-09-06更新
|
166次组卷
|
2卷引用:陕西省安康市安康中学2023-2024学年高二上学期10月月考化学试题



