解题方法
1 . 在恒容容器中发生CH4(g)燃烧。写出1molCH4(g)完全燃烧的热化学方程式____  达到平衡后,若向其中加入H2O后,平衡
达到平衡后,若向其中加入H2O后,平衡____ (选填:向右移动,向左移动,不移动),加入O2后,甲烷转化率____ 。
 达到平衡后,若向其中加入H2O后,平衡
达到平衡后,若向其中加入H2O后,平衡
您最近一年使用:0次
2 . 下列事实能用平衡移动原理解释的是
| A.合成氨工业中使用铁触媒作催化剂 |
B.铁钉放入浓 中不再变化后,加热能产生大量红棕色气体 中不再变化后,加热能产生大量红棕色气体 |
C.氯碱工业中阳极区的溶液用盐酸调pH为2~3,促进 的产生 的产生 |
D.锌片与稀 反应过程中,加入少量 反应过程中,加入少量 固体,促进 固体,促进 的产生 的产生 |
您最近一年使用:0次
名校
解题方法
3 . 下列实验能达到实验目的的是
| A | B |
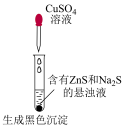 | 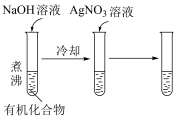 |
比较相同温度下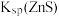 和 和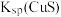 的大小 的大小 | 检验有机化合物中含溴原子 |
| C | D |
 | 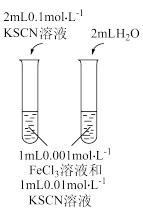 |
| 探究干燥的氯气是否具有漂白性 | 研究浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
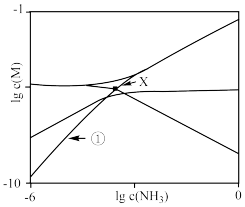
4 . 在 悬浊液中滴加氨水[浓度以
悬浊液中滴加氨水[浓度以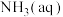 计],存在平衡关系:
计],存在平衡关系:
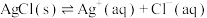 ;
;
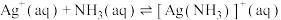 ;
;
 ,
,
平衡常数分别为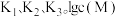 与
与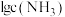 的关系如图所示(其中
的关系如图所示(其中 代表
代表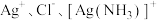 或
或 )。下列说法错误的是
)。下列说法错误的是
 悬浊液中滴加氨水[浓度以
悬浊液中滴加氨水[浓度以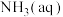 计],存在平衡关系:
计],存在平衡关系: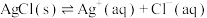 ;
;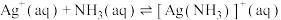 ;
; ,
,平衡常数分别为
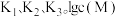 与
与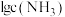 的关系如图所示(其中
的关系如图所示(其中 代表
代表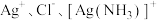 或
或 )。下列说法错误的是
)。下列说法错误的是
A. 时,溶液中 时,溶液中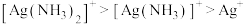 |
B.加入少量 固体后,X点坐标下移 固体后,X点坐标下移 |
C.随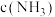 浓度增大, 浓度增大,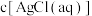 也增大 也增大 |
D.X点对应的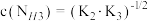 |
您最近一年使用:0次
名校
解题方法
5 . 钯(Pd)见一种银白色过渡金属,质软、有良好的延展性和可塑性,他锻造、压延和拉丝。块状金属钯能吸收大量氢气,使体积显著胀大、变脆乃至破裂成碎片。一种从废钯催化剂(杂质主要含有机物、活性炭及少量Fe、Cu、Al等元素)中回收钯和类芬顿催化剂 的工艺流程如图所示:
的工艺流程如图所示:
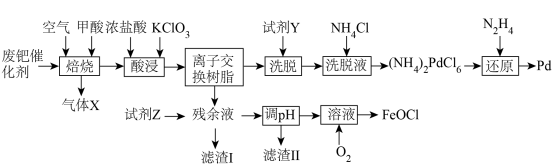
已知:①常温下,钯不溶于盐酸;Pd易被氧化为难溶于酸的 而失去催化活性;
而失去催化活性;
②阴、阳离子交换树脂的基本工作原理分别为 、
、 (R—表示树脂的有机成分);
(R—表示树脂的有机成分);
③常温下,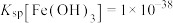 ;
;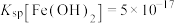 ;
; ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;
④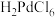 是一种二元强酸,
是一种二元强酸, 在溶液中存在配位平衡:
在溶液中存在配位平衡: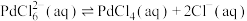
 ;
;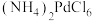 在水中溶解度小。
在水中溶解度小。
回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧,其主要目的是___________ ,再通入甲酸继续焙烧的目的是___________ 。
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为___________ ,实现浸取Pd的同时,还可能会存在的缺陷是___________ 。
(3)“洗脱”时,加入最佳“试剂Y”的名称是___________ ,“洗脱液”中要加入过量 的目的是
的目的是___________ 。
(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为___________ 。“调pH”步骤中,若铁元素和铝元素浓度均为 ,则调pH的范围为
,则调pH的范围为___________ (lg2=0.3)。
 的工艺流程如图所示:
的工艺流程如图所示:
已知:①常温下,钯不溶于盐酸;Pd易被氧化为难溶于酸的
 而失去催化活性;
而失去催化活性;②阴、阳离子交换树脂的基本工作原理分别为
 、
、 (R—表示树脂的有机成分);
(R—表示树脂的有机成分);③常温下,
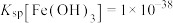 ;
;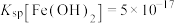 ;
; ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;④
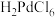 是一种二元强酸,
是一种二元强酸, 在溶液中存在配位平衡:
在溶液中存在配位平衡: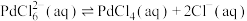
 ;
;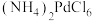 在水中溶解度小。
在水中溶解度小。回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧,其主要目的是
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为
(3)“洗脱”时,加入最佳“试剂Y”的名称是
 的目的是
的目的是(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为
 ,则调pH的范围为
,则调pH的范围为
您最近一年使用:0次
名校
解题方法
6 . 下列实验操作、现象及相应结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用pH 计测定浓度均为0.1mol/L的 、 、 溶液的酸碱性 溶液的酸碱性 |  溶液显碱性, 溶液显碱性, 溶液显酸性 溶液显酸性 | 可以确定 是弱酸,无法判断 是弱酸,无法判断 是否为弱酸 是否为弱酸 |
B | 铬酸钾溶液中存在平衡: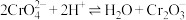 ,向铬酸钾溶液中加水稀释 ,向铬酸钾溶液中加水稀释 | 溶液黄色加深 | 平衡逆向移动 |
C | 向肉桂醛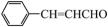 中加入溴水 中加入溴水 | 溴水溶液褪色 | 证明肉桂醛中含有碳碳双键 |
D | 取少量 溶液于试管中,先加入足量稀硝酸,再加足量 溶液于试管中,先加入足量稀硝酸,再加足量 溶液 溶液 | 有白色沉淀生成 | 证明 溶液已经被氧化变质 溶液已经被氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 某兴趣小组将4g铁钉放入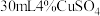 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
①CuSCN:白色固体,不溶于水;
②室温下,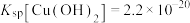 ,
, ,
, 。
。
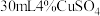 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是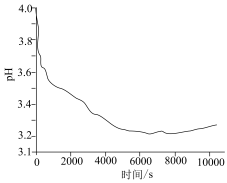
①CuSCN:白色固体,不溶于水;
②室温下,
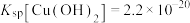 ,
, ,
, 。
。A. 溶液 溶液 的原因是 的原因是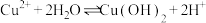 |
B.0~6000s,随着反应进行,溶液pH下降的原因可能是 被 被 氧化为 氧化为 |
C.反应后期溶液pH略有上升的可能原因是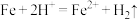 |
D.溶液先变红后又褪色的可能原因是 的反应速率快, 的反应速率快,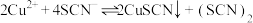 的反应限度大 的反应限度大 |
您最近一年使用:0次
2024-02-29更新
|
115次组卷
|
3卷引用:北京市第一七一中学2023-2024学年高三下学期开学考试化学试题
23-24高三下·北京·开学考试
名校
解题方法
8 . 下列方程式不正确 的是
A.用稀 清洗银镜: 清洗银镜: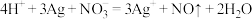 |
B.氢氧化亚铁露置在空气中变为红褐色: |
C.向苯酚钠溶液中通入 ,溶液变浑浊:2 ,溶液变浑浊:2  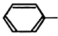 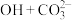 |
D.向 溶液中滴加少量硫酸,溶液橙色加深: 溶液中滴加少量硫酸,溶液橙色加深: |
您最近一年使用:0次
名校
解题方法
9 . 某化学小组通过测定溶液pH,计算K2Cr2O7溶液中“Cr2O (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:
下列说法不合理的是
 (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:| 实验序号 | 温度(°C) | K2Cr2O7溶液浓度(mol/L) | pH | 平衡常数 |
| ① | 26.3 | 0.1000 | a | 2.5×10-15 |
| ② | 26.3 | 0.3000 | 3.78 | b |
| ③ | 50.0 | 0.1000 | 3.75 | 1.01×10-14 |
| A.a大于3.78 |
| B.b等于2.5×10-15 |
| C.由实验①③结果可说明该反应为吸热反应 |
| D.向实验①2mL溶液中加入6滴6mol/LNaOH溶液,溶液橙色加深;恢复原温度,平衡常数不变 |
您最近一年使用:0次
名校
10 . I.某小组对Cu与浓HNO3的反应进行研究。记录如下:
(1)Cu与浓HNO3反应的化学方程式是___________ 。
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是___________ 。
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是___________ 、___________ 。
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii. 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)
据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了 使溶液呈绿色。
使溶液呈绿色。
丙进行如下实验:
①亚硝酸分解的化学方程式是___________ 。
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:___________ 。
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是___________ 。请依据实验现象阐述理由:___________ 。
| 装置 | 药品 | 现象 | |
| 实验1 | 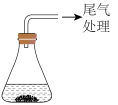 | 0.64gCu片(0.01mol) Cu片和20.0 mL浓HNO3 | Cu片消失,得到绿色溶液A,放置较长时间后得到蓝色溶 液B,…… |
(1)Cu与浓HNO3反应的化学方程式是
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii.
 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了
 使溶液呈绿色。
使溶液呈绿色。丙进行如下实验:
| 操作 | 现象 | |
| 实验3 | i.配制与溶液A的c(H+)相同的HNO3溶液,取20.0mL,通入NO2气体 | 溶液呈黄色 |
| ii.再加0.01molCu(NO3)2固体搅拌至完全溶解 | 溶液变为绿色 | |
| iii.加水稀释 | 溶液立即变蓝 | |
| 实验4 | i.向20.0mL0.5mol/L Cu(NO3)2蓝色溶液中通入少量NO2 | 溶液呈绿色 |
| ii.加入稀H2SO4 | 有无色气体放出,遇空气变红棕色,溶液很快变为蓝色 |
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是
您最近一年使用:0次



