2021高三·全国·专题练习
名校
解题方法
1 . 在一密闭容器中发生反应N2+3H2=2NH3 ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
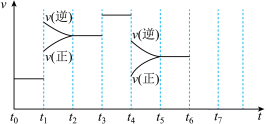
回答下列问题:
(1)处于平衡状态的时间段是___________ (填字母,下同)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻___________ ;t3时刻___________ ;t4时刻___________ 。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是___________ 。
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线______ 。

回答下列问题:
(1)处于平衡状态的时间段是
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线
您最近一年使用:0次
2021-05-05更新
|
1344次组卷
|
7卷引用:小题30 化学平衡常规图像——备战2021年高考化学经典小题考前必刷(全国通用)
(已下线)小题30 化学平衡常规图像——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)第七章 化学反应速率与化学平衡 第44讲 化学反应速率、平衡的常规图像(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)广西玉林市市直六所普通高中2021-2022学年高二上学期期中考试理科综合化学试题江苏省连云港市赣榆智贤中学2022-2023学年高二上学期第一次学情检测化学试题四川省泸县第四中学2022-2023学年高二上学期期中考试化学试题四川省成都市第八中学校2022-2023学年高二上学期11月期中考试化学试题
2022高二·上海·专题练习
2 . 将2molA和1molB混合置于一容积可变的密闭容器中,在温度T下发生如下反应:2A(g)+B(g) 2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:
2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:
(1)该反应的平衡常数表达式为___________ ;
(2)下列有关化学平衡常数K的说法正确的是___________(填字母)
(3)若降低温度,则该反应的K值___________ (填“增大”、“减小”或“不变”,下同),A的转化率___________ ,化学反应速率___________ ;
(4)反应进行tmin后,C的体积分数为___________ 。
 2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:
2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:(1)该反应的平衡常数表达式为
(2)下列有关化学平衡常数K的说法正确的是___________(填字母)
| A.在任何情况下,化学平衡常数K均为一个定值 |
| B.改变气体A或C的浓度,都会改变平衡常数K |
| C.平衡常数K只与温度有关,与反应物的浓度无关 |
| D.从平衡常数K的大小可以推断一个反应进行的限度 |
(4)反应进行tmin后,C的体积分数为
您最近一年使用:0次
2022高三·全国·专题练习
3 . 碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。溶洞景区限制参观的游客数量,主要原因之一是游客呼吸产生的气体对钟乳石有破坏作用,从化学平衡的角度说明其原因___________ 。
您最近一年使用:0次
4 . 在密闭容器中发生如下反应
 ;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
(1)升高温度,平衡_______ 移动;
(2)增大压强,平衡_______ 移动:
(3)增大H2(g)浓度,平衡_______ 移动:加入C,平衡_______ 移动;
(4)加入催化剂,平衡_______ 移动。

 ;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)(1)升高温度,平衡
(2)增大压强,平衡
(3)增大H2(g)浓度,平衡
(4)加入催化剂,平衡
您最近一年使用:0次
2021-05-04更新
|
858次组卷
|
4卷引用:2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)新疆喀什巴楚县第一中学2020-2021学年高二下学期期中考试化学试题课前-2.4 化学反应的调控-课前、课中、课后(人教版2019选择性必修1)
名校
解题方法
5 . CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。请回答下列问题:
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
(1)达到平衡时,反应a,b对比:CO2的体积分数φ(a)_______ φ(b)(填“>”、“<”或“=”))。
(2)下列能说明反应a达到平衡状态的是_______ (填字母)。
A.v正(CO2)=3v逆(H2)
B.混合气体的平均摩尔质量不再改变
C.c(CH3OH)=c(H2O)
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
在密闭容器中通入3mol的的H2和1mol的CO2,分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。
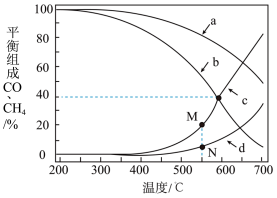
(3)1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是_______ 和_______ 。M点平衡组成含量高于N点的原因是_______ 。
(4)图中当CH4和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为_______ 。
III.在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和H2,发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。
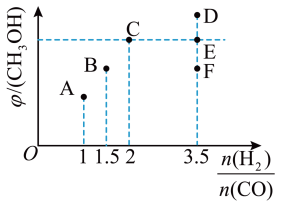
(5)当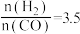 时,达到平衡后,CH3OH的体积分数可能是图象中的
时,达到平衡后,CH3OH的体积分数可能是图象中的_______ (填“D”、“E”或“F”)点。
(6) =
=_______ 时,CH3OH的体积分数最大。
I.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
| CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应a(恒温恒容) | 1 | 3 | 0 | 0 |
| 反应b(绝热恒容) | 0 | 0 | 1 | 1 |
(2)下列能说明反应a达到平衡状态的是
A.v正(CO2)=3v逆(H2)
B.混合气体的平均摩尔质量不再改变
C.c(CH3OH)=c(H2O)
D.容器内压强不再改变
II.我国科学家研究了不同反应温度对含碳产物组成的影响。
已知:反应1:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH<0
反应2:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0
在密闭容器中通入3mol的的H2和1mol的CO2,分别在1MPa和10MPa下进行反应。实验中对平衡体系组成的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4的影响如图所示。

(3)1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是
(4)图中当CH4和CO平衡组成均为40%时,若容器的体积为1L,该温度下反应1的平衡常数K的值为
III.在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的的CO和H2,发生反应CO(g)+2H2(g) ⇌ CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。

(5)当
 时,达到平衡后,CH3OH的体积分数可能是图象中的
时,达到平衡后,CH3OH的体积分数可能是图象中的(6)
 =
=
您最近一年使用:0次
2021-03-04更新
|
821次组卷
|
4卷引用:第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测
(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)吉林省延边州2021届高三下学期教学质量检测(2月底) 理综化学试题江苏省扬州中学2021-2022学年高二上学期期中考试化学试题
2022高一·上海·专题练习
6 . 某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g)  2SO3(g) (放热反应)的正、逆反应速率的影响如图所示:
2SO3(g) (放热反应)的正、逆反应速率的影响如图所示:
(1)加催化剂对反应速率影响的图象是___________ (填序号,下同),平衡___________ 移动。
(2)升高温度对反应速率影响的图象是___________ ,平衡向___________ 方向移动。
(3)增大O2的浓度对反应速率影响的图象是___________ ,平衡向___________ 方向移动。
 2SO3(g) (放热反应)的正、逆反应速率的影响如图所示:
2SO3(g) (放热反应)的正、逆反应速率的影响如图所示:
(1)加催化剂对反应速率影响的图象是
(2)升高温度对反应速率影响的图象是
(3)增大O2的浓度对反应速率影响的图象是
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
7 . 氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:
已知:① Cr2O +H2O
+H2O 2CrO
2CrO +2H+;
+2H+;
② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体___________ ,蒸发浓缩,___________ ,过滤, ___________ ,低温干燥,得到CrCl3·6H2O(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)。

已知:① Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+;
+2H+;② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 . 已知:I.CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
II.CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
III.CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
如图为一定比例的CO2、H2;CO、H2;CO、CO2、H2三个反应体系下甲醇生成速率与温度的关系。

490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因:_______ 。
 CO2(g)+H2(g)
CO2(g)+H2(g)II.CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)III.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)如图为一定比例的CO2、H2;CO、H2;CO、CO2、H2三个反应体系下甲醇生成速率与温度的关系。

490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因:
您最近一年使用:0次
2021高二·全国·专题练习
9 . 对于以下三个反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答下列问题。
(1)PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
再充入PCl5(g),平衡向____ 方向移动,达到平衡后,PCl5(g)的转化率____ ,PCl5(g)的百分含量____ 。
(2)2HI(g) I2(g)+H2(g)
I2(g)+H2(g)
再充入HI(g),平衡向____ 方向移动,达到平衡后,HI的分解率____ ,HI的百分含量____ 。
(3)2NO2(g) N2O4(g)
N2O4(g)
再充入NO2(g),平衡向____ 方向移动,达到平衡后,NO2(g)的转化率____ ,NO2(g)的百分含量____ 。
(1)PCl5(g)
 PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)再充入PCl5(g),平衡向
(2)2HI(g)
 I2(g)+H2(g)
I2(g)+H2(g)再充入HI(g),平衡向
(3)2NO2(g)
 N2O4(g)
N2O4(g)再充入NO2(g),平衡向
您最近一年使用:0次
2022高三·全国·专题练习
10 . 乙醇在催化剂存在下受热发生脱水反应,既可分子内脱水生成乙烯,也可分子间脱水生成乙醚,具体反应式如下:
①C2H5OH(g)=C2H4(g)+H2O(g)
②2C2H5OH(g)=C2H5OC2H5(g)+H2O(g)
已知:乙醇和乙醚的沸点分别为78.4℃和34.5℃。
反应进程与相对能量如图所示:
由图可知反应②的△H____ 0(填“>”“=”或“<”);要提高反应①的平衡转化率,可采取的措施为____ (填选项)。
A.体积不变,增大压强 B.升温
C.体积不变,增加乙醇的量 D.及时分离出乙烯
①C2H5OH(g)=C2H4(g)+H2O(g)
②2C2H5OH(g)=C2H5OC2H5(g)+H2O(g)
已知:乙醇和乙醚的沸点分别为78.4℃和34.5℃。
反应进程与相对能量如图所示:

由图可知反应②的△H
A.体积不变,增大压强 B.升温
C.体积不变,增加乙醇的量 D.及时分离出乙烯
您最近一年使用:0次



