2024高三下·全国·专题练习
解题方法
1 . 钒是重要的战略资源,以硫酸工业产生的废钒催化剂为原料(含 、
、 、
、 、
、 以及少量的
以及少量的 等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下:
等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下: 、
、 存在,
存在, 增大时
增大时 可转化为
可转化为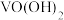 沉淀。
沉淀。
“萃取”时选择有机萃取剂,原理是: (有机层)
(有机层)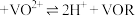 (有机层),“反萃取”应选择在
(有机层),“反萃取”应选择在___________ 环境中进行(选填“酸性”、“中性”或“碱性”)。
 、
、 、
、 、
、 以及少量的
以及少量的 等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下:
等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下: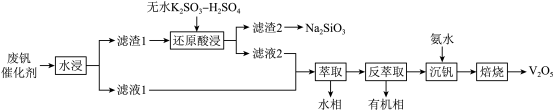
 、
、 存在,
存在, 增大时
增大时 可转化为
可转化为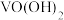 沉淀。
沉淀。“萃取”时选择有机萃取剂,原理是:
 (有机层)
(有机层)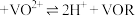 (有机层),“反萃取”应选择在
(有机层),“反萃取”应选择在
您最近一年使用:0次
2024高三下·全国·专题练习
2 . 推动 的综合利用、实现碳中和是党中央作出的重大战略决策。
的综合利用、实现碳中和是党中央作出的重大战略决策。
(1) 一定条件可转化为
一定条件可转化为 ,
,
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,分子筛膜能选择性分离出 。P点甲醇产率高于T点的原因为
。P点甲醇产率高于T点的原因为___________ 。 与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对
与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对 转化率的影响如图所示,
转化率的影响如图所示, 时
时 转化率低于
转化率低于 和
和 的原因可能为
的原因可能为___________ 。
 的综合利用、实现碳中和是党中央作出的重大战略决策。
的综合利用、实现碳中和是党中央作出的重大战略决策。(1)
 一定条件可转化为
一定条件可转化为 ,
,
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,分子筛膜能选择性分离出
 。P点甲醇产率高于T点的原因为
。P点甲醇产率高于T点的原因为
 与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对
与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对 转化率的影响如图所示,
转化率的影响如图所示, 时
时 转化率低于
转化率低于 和
和 的原因可能为
的原因可能为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 2023年杭州亚运会开幕式首次使用“零碳甲醇”作为主火炬塔燃料。NiO-In2O3可催化CO2的氢化,体系中产生CH3OH和CO。现将一定比例的CO2、H2以一定流速通过催化剂,某温度下,得到CO2的转化率、CH3OH或CO的选择性[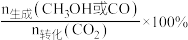 ]与催化剂中NiO质量分数的关系图:
]与催化剂中NiO质量分数的关系图:

(1)曲线_______ (填“X”或“Y”)表示CO2的转化率随催化剂中NiO的质量分数的变化。
(2)有利于提高CH3OH选择性的反应条件是_______ (填标号)。
A.减小压强 B.使用更合适的催化剂 C.原料气中掺入适量的CO
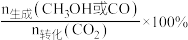 ]与催化剂中NiO质量分数的关系图:
]与催化剂中NiO质量分数的关系图:
(1)曲线
(2)有利于提高CH3OH选择性的反应条件是
A.减小压强 B.使用更合适的催化剂 C.原料气中掺入适量的CO
您最近一年使用:0次
2023高三·全国·专题练习
4 . 工业尾气H2S对环境和人体健康会产生严重危害,回收H2S制备高附加值的硫磺是保护环境和资源利用的有效措施。
已知:2H2S(g)⇌2H2(g)+S2(g) △H=+169.8kJ/mol。
回答下列问题:
(1)上述反应中相关键能数据:
①反应能自发进行的条件是___________ ,a=___________  。
。
②在恒温恒容密闭容器中,充入一定量 气体发生上述反应,下列说法正确的是
气体发生上述反应,下列说法正确的是___________ (填标号)。
A. 的体积分数不再改变,说明该反应达到平衡
的体积分数不再改变,说明该反应达到平衡
B. 与
与 体积比不再改变,说明该反应达到平衡
体积比不再改变,说明该反应达到平衡
C.平衡时向容器中充入情性气体,平衡正向移动
D.平衡时向容器中充入 和
和 ,再达平衡时,
,再达平衡时, 不变
不变
(2)保持压强恒定为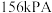 ,向密闭容器中充入
,向密闭容器中充入 和
和 (
( 不参与反应)发生上述反应,
不参与反应)发生上述反应, 的平衡转化率
的平衡转化率 ]与通入气体中
]与通入气体中 、温度
、温度 关系如下图所示。
关系如下图所示。

①从反应开始至反应体系分别达到M、N点状态,平均反应速率较快的是达到___________ (填“M”或“N”)的过程。
②相同温度下,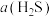 随着x增大而减小,其原因是
随着x增大而减小,其原因是___________ 。
已知:2H2S(g)⇌2H2(g)+S2(g) △H=+169.8kJ/mol。
回答下列问题:
(1)上述反应中相关键能数据:
| 化学键 |  |  |  |
键能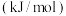 | a | 329 | 436 |
 。
。②在恒温恒容密闭容器中,充入一定量
 气体发生上述反应,下列说法正确的是
气体发生上述反应,下列说法正确的是A.
 的体积分数不再改变,说明该反应达到平衡
的体积分数不再改变,说明该反应达到平衡B.
 与
与 体积比不再改变,说明该反应达到平衡
体积比不再改变,说明该反应达到平衡C.平衡时向容器中充入情性气体,平衡正向移动
D.平衡时向容器中充入
 和
和 ,再达平衡时,
,再达平衡时, 不变
不变(2)保持压强恒定为
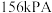 ,向密闭容器中充入
,向密闭容器中充入 和
和 (
( 不参与反应)发生上述反应,
不参与反应)发生上述反应, 的平衡转化率
的平衡转化率 ]与通入气体中
]与通入气体中 、温度
、温度 关系如下图所示。
关系如下图所示。
①从反应开始至反应体系分别达到M、N点状态,平均反应速率较快的是达到
②相同温度下,
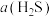 随着x增大而减小,其原因是
随着x增大而减小,其原因是
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
5 . 已知:I.CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
II.CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
III.CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
如图为一定比例的CO2、H2;CO、H2;CO、CO2、H2三个反应体系下甲醇生成速率与温度的关系。

490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因:_______ 。
 CO2(g)+H2(g)
CO2(g)+H2(g)II.CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)III.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)如图为一定比例的CO2、H2;CO、H2;CO、CO2、H2三个反应体系下甲醇生成速率与温度的关系。

490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因:
您最近一年使用:0次
2023高三·全国·专题练习
6 . 已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)  C2H5OH(g)+3H2O(g) ΔH<0,图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) ΔH<0,图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=



(1)图1中投料比相同,温度从高到低的顺序为___________ ,判断依据是___________
(2)图2中m1、m2、m3从大到小的顺序为___________ ,判断依据是___________
 C2H5OH(g)+3H2O(g) ΔH<0,图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) ΔH<0,图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=



(1)图1中投料比相同,温度从高到低的顺序为
(2)图2中m1、m2、m3从大到小的顺序为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . 在密闭容器中,反应: ,在一定条件下达到平衡状态,试回答下列问题:
,在一定条件下达到平衡状态,试回答下列问题:
(1)若保持体积不变,通入氦气,则平衡________ 移动。
(2)若保持压强不变,通入氦气,平衡向正反应方向移动,则x、y、之的关系为________ 。
 ,在一定条件下达到平衡状态,试回答下列问题:
,在一定条件下达到平衡状态,试回答下列问题:(1)若保持体积不变,通入氦气,则平衡
(2)若保持压强不变,通入氦气,平衡向正反应方向移动,则x、y、之的关系为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 . 已知: ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
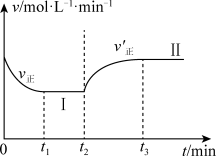
(1)容器内压强不变,表明反应达到平衡。(______)
(2) 时改变的条件是向容器中加入C。(______)
时改变的条件是向容器中加入C。(______)
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
(1)容器内压强不变,表明反应达到平衡。(______)
(2)
 时改变的条件是向容器中加入C。(______)
时改变的条件是向容器中加入C。(______)
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . 影响化学平衡的外界因素
若其他条件不变,改变下列条件对化学平衡的影响如下:
若其他条件不变,改变下列条件对化学平衡的影响如下:
改变的条件(其他条件不变) | 化学平衡移动的方向 | ||
| 浓度 | 增大反应物浓度或减小生成物浓度 | 向 | |
| 减小反应物浓度或增大生成物浓度 | 向 | ||
| 压强(对于有气体参加的可逆反应) | 反应前后气体体积改变 | 增大压强 | 向气体分子总数 |
| 减小压强 | 向气体分子总数 | ||
| 反应前后气体体积不变 | 改变压强 | 平衡 | |
| 温度 | 升高温度 | 向 | |
降低温度 | 向 | ||
| 催化剂 | 同等程度地改变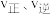 ,平衡不移动 ,平衡不移动 | ||
您最近一年使用:0次
2023高三·全国·专题练习
10 . 向黄色的 溶液中加入无色的
溶液中加入无色的 溶液,溶液变成红色。该反应在有的教材中用方程式
溶液,溶液变成红色。该反应在有的教材中用方程式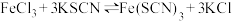 表示。
表示。
(1)向上述红色溶液中继续加入浓 溶液,溶液红色加深,这是由于
溶液,溶液红色加深,这是由于_______________ (填字母).
A.与 配合的
配合的 数目增多
数目增多
B.红色离子的数目增多
C.红色离子的浓度增加
(2)向上述红色溶液中加入 溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为
溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为_______________ ;能使该反应发生的可能原因是_______________ 。
 溶液中加入无色的
溶液中加入无色的 溶液,溶液变成红色。该反应在有的教材中用方程式
溶液,溶液变成红色。该反应在有的教材中用方程式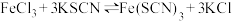 表示。
表示。(1)向上述红色溶液中继续加入浓
 溶液,溶液红色加深,这是由于
溶液,溶液红色加深,这是由于A.与
 配合的
配合的 数目增多
数目增多B.红色离子的数目增多
C.红色离子的浓度增加
(2)向上述红色溶液中加入
 溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为
溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为
您最近一年使用:0次



