2023高三·全国·专题练习
1 . 二甲醚既是重要的工业品,也是燃料电池制氢的重要原料。二甲醚水蒸气重整制氢的总反应为
 ,其过程包括:
,其过程包括:
Ⅰ.
Ⅱ.
Ⅲ.
Ⅳ.
 的选择性(
的选择性( )与水醚比[
)与水醚比[ ]和温度的关系如图1所示;
]和温度的关系如图1所示; 时,平衡时
时,平衡时 的物质的量分数与水醚比的关系如图2所示:
的物质的量分数与水醚比的关系如图2所示:

(1)图1中相同温度下,水醚比越大, 的选择性越高的原因是
的选择性越高的原因是_______ ;相同水醚比时,温度升高, 的选择性降低的原因是
的选择性降低的原因是_______ 。
(2)图2中水醚比大于3时,随水醚比的增大 的物质的量分数减小的原因是
的物质的量分数减小的原因是_______ 。

 ,其过程包括:
,其过程包括:Ⅰ.

Ⅱ.

Ⅲ.

Ⅳ.

 的选择性(
的选择性( )与水醚比[
)与水醚比[ ]和温度的关系如图1所示;
]和温度的关系如图1所示; 时,平衡时
时,平衡时 的物质的量分数与水醚比的关系如图2所示:
的物质的量分数与水醚比的关系如图2所示:
(1)图1中相同温度下,水醚比越大,
 的选择性越高的原因是
的选择性越高的原因是 的选择性降低的原因是
的选择性降低的原因是(2)图2中水醚比大于3时,随水醚比的增大
 的物质的量分数减小的原因是
的物质的量分数减小的原因是
您最近一年使用:0次
2023高三·全国·专题练习
2 . 恒温刚性密闭容器中通入气体分压比为p(C3H8)∶p(O2)∶p(N2)=2∶13∶85的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):
反应II:2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) k
反应III:2C3H6(g)+9O2(g)=6CO2(g)+6H2O(g) k′
实验测得丙烯的净生成速率方程为v(C3H6)=kp(C3H8)-k′p(C3H6),可推测丙烯的浓度随时间的变化趋势为_______ ,其理由是______ 。
反应II:2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) k
反应III:2C3H6(g)+9O2(g)=6CO2(g)+6H2O(g) k′
实验测得丙烯的净生成速率方程为v(C3H6)=kp(C3H8)-k′p(C3H6),可推测丙烯的浓度随时间的变化趋势为
您最近一年使用:0次
2023高三·全国·专题练习
3 . 某合成氨速率方程为:v=kcα(N2)•cβ(H2)•cγ(NH3),根据表中数据,γ=_____ 。
在合成氨过程中,需要不断分离出氨的原因为______ 。
a.有利于平衡正向移动
b.防止催化剂中毒
c.提高正反应速率
| 实验 | 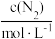 | 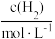 |  | 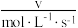 |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
a.有利于平衡正向移动
b.防止催化剂中毒
c.提高正反应速率
您最近一年使用:0次
2022高三·全国·专题练习
4 . 乙醇在催化剂存在下受热发生脱水反应,既可分子内脱水生成乙烯,也可分子间脱水生成乙醚,具体反应式如下:
①C2H5OH(g)=C2H4(g)+H2O(g)
②2C2H5OH(g)=C2H5OC2H5(g)+H2O(g)
已知:乙醇和乙醚的沸点分别为78.4℃和34.5℃。
反应进程与相对能量如图所示:
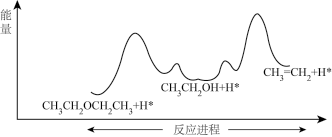
由图可知反应②的△H____ 0(填“>”“=”或“<”);要提高反应①的平衡转化率,可采取的措施为____ (填选项)。
A.体积不变,增大压强 B.升温
C.体积不变,增加乙醇的量 D.及时分离出乙烯
①C2H5OH(g)=C2H4(g)+H2O(g)
②2C2H5OH(g)=C2H5OC2H5(g)+H2O(g)
已知:乙醇和乙醚的沸点分别为78.4℃和34.5℃。
反应进程与相对能量如图所示:

由图可知反应②的△H
A.体积不变,增大压强 B.升温
C.体积不变,增加乙醇的量 D.及时分离出乙烯
您最近一年使用:0次
2022高三·全国·专题练习
5 . 研发CO2利用技术成为了研究热点,某科研团队采用一种类似“搭积木”的方式,在实验室中首次实现从二氧化碳到淀粉分子的全合成,“积木”中涉及如下两个反应:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
②CH3OH(g)+O2(g) HCHO(g)+H2O2(l)。
HCHO(g)+H2O2(l)。
写出检验HCOOH中是否含醛基的实验方法_______ 。
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) ②CH3OH(g)+O2(g)
 HCHO(g)+H2O2(l)。
HCHO(g)+H2O2(l)。写出检验HCOOH中是否含醛基的实验方法
您最近一年使用:0次
2022高二·上海·专题练习
6 . 一定温度下,在体积固定的密闭容器中发生如下反应:H2(g)+I2(g) 2HI(g)。达到平衡时,H2(g)、I2(g)的物质的量浓度均为0.01mol·L-1,HI(g)的物质的量浓度为0.06mol·L-1.现分别对平衡混合物进行下列操作,计算操作后反应的浓度商,并判断平衡移动的方向。
2HI(g)。达到平衡时,H2(g)、I2(g)的物质的量浓度均为0.01mol·L-1,HI(g)的物质的量浓度为0.06mol·L-1.现分别对平衡混合物进行下列操作,计算操作后反应的浓度商,并判断平衡移动的方向。
(1)保持其他条件不变,向容器中通入H2(g),使其浓度达到0.02mol·L-1___________ ;
(2)保持其他条件不变,向容器中通入HI(g),使其浓度达到0.08mol·L-1___________ ;
(3)保持其他条件不变,向容器中通入Ar(g),使其浓度达到0.01mol·L-1___________ 。
 2HI(g)。达到平衡时,H2(g)、I2(g)的物质的量浓度均为0.01mol·L-1,HI(g)的物质的量浓度为0.06mol·L-1.现分别对平衡混合物进行下列操作,计算操作后反应的浓度商,并判断平衡移动的方向。
2HI(g)。达到平衡时,H2(g)、I2(g)的物质的量浓度均为0.01mol·L-1,HI(g)的物质的量浓度为0.06mol·L-1.现分别对平衡混合物进行下列操作,计算操作后反应的浓度商,并判断平衡移动的方向。(1)保持其他条件不变,向容器中通入H2(g),使其浓度达到0.02mol·L-1
(2)保持其他条件不变,向容器中通入HI(g),使其浓度达到0.08mol·L-1
(3)保持其他条件不变,向容器中通入Ar(g),使其浓度达到0.01mol·L-1
您最近一年使用:0次
2022高二·上海·专题练习
7 . 对于CO+H2O(g) CO2+H2,已知700℃时,平衡常数K=1.67.若在反应中加入CO、H2O(g)、CO2、H2的浓度均为1mol/L,试判断该反应进行的方向
CO2+H2,已知700℃时,平衡常数K=1.67.若在反应中加入CO、H2O(g)、CO2、H2的浓度均为1mol/L,试判断该反应进行的方向___________ 。
 CO2+H2,已知700℃时,平衡常数K=1.67.若在反应中加入CO、H2O(g)、CO2、H2的浓度均为1mol/L,试判断该反应进行的方向
CO2+H2,已知700℃时,平衡常数K=1.67.若在反应中加入CO、H2O(g)、CO2、H2的浓度均为1mol/L,试判断该反应进行的方向
您最近一年使用:0次
2022高二·上海·专题练习
8 . 将2molA和1molB混合置于一容积可变的密闭容器中,在温度T下发生如下反应:2A(g)+B(g) 2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:
2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:
(1)该反应的平衡常数表达式为___________ ;
(2)下列有关化学平衡常数K的说法正确的是___________(填字母)
(3)若降低温度,则该反应的K值___________ (填“增大”、“减小”或“不变”,下同),A的转化率___________ ,化学反应速率___________ ;
(4)反应进行tmin后,C的体积分数为___________ 。
 2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:
2C(g)+Q,反应进行tmin后达到平衡,测得混合气体的总物质的量为2.1mol。试回答:(1)该反应的平衡常数表达式为
(2)下列有关化学平衡常数K的说法正确的是___________(填字母)
| A.在任何情况下,化学平衡常数K均为一个定值 |
| B.改变气体A或C的浓度,都会改变平衡常数K |
| C.平衡常数K只与温度有关,与反应物的浓度无关 |
| D.从平衡常数K的大小可以推断一个反应进行的限度 |
(4)反应进行tmin后,C的体积分数为
您最近一年使用:0次
2022高二·上海·专题练习
名校
9 . 高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH>0
Fe(s)+CO2(g)ΔH>0
其平衡常数可表示为K=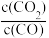 ,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比___________ ,平衡常数K___________ 。(以上均填“增大”“减小”或“不变”)
(2)1100℃时测得高炉中c(CO2)=0.025mol·L-1、c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于化学平衡状态:___________ (填“是”或“否”,若填“是”,则后面问题可不答),此时反应向___________ (填“正反应”或“逆反应”)方向进行,其原因是___________ 。
 Fe(s)+CO2(g)ΔH>0
Fe(s)+CO2(g)ΔH>0其平衡常数可表示为K=
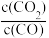 ,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比
(2)1100℃时测得高炉中c(CO2)=0.025mol·L-1、c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于化学平衡状态:
您最近一年使用:0次



