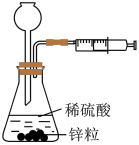
1 . 历史上曾用Deacon法生产Cl2,化学原理为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)。下列说法正确的是
2Cl2(g)+2H2O(g)。下列说法正确的是
 2Cl2(g)+2H2O(g)。下列说法正确的是
2Cl2(g)+2H2O(g)。下列说法正确的是| A.该反应ΔH>0、ΔS>0 |
B.反应平衡常数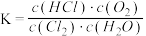 |
C.提高 的值可增大HCl的转化率 的值可增大HCl的转化率 |
| D.每生产1 mol Cl2,反应中转移电子数目约2×6.02×1023 |
您最近一年使用:0次
名校
解题方法
2 . 研究碘在不同溶剂中的溶解度。进行实验:
①向试管里放入一小粒碘晶体,再加入蒸馏水,充分溶解后,得到黄色溶液 和少量不溶的碘;
和少量不溶的碘;
②取5mL溶液 ,再加入1mL四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
,再加入1mL四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
③将②所得下层溶液全部取出,加入1mL 溶液,振荡,静置,下层溶液紫色变浅,上层溶液
溶液,振荡,静置,下层溶液紫色变浅,上层溶液 呈黄色(颜色比溶液
呈黄色(颜色比溶液 深)。
深)。
已知:i. ;ii.
;ii. 。
。
下列说法不正确的是
①向试管里放入一小粒碘晶体,再加入蒸馏水,充分溶解后,得到黄色溶液
 和少量不溶的碘;
和少量不溶的碘;②取5mL溶液
 ,再加入1mL四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
,再加入1mL四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;③将②所得下层溶液全部取出,加入1mL
 溶液,振荡,静置,下层溶液紫色变浅,上层溶液
溶液,振荡,静置,下层溶液紫色变浅,上层溶液 呈黄色(颜色比溶液
呈黄色(颜色比溶液 深)。
深)。已知:i.
 ;ii.
;ii. 。
。下列说法不正确的是
A. 是极性溶剂, 是极性溶剂, 是非极性溶剂,非极性 是非极性溶剂,非极性 更易溶于 更易溶于 |
| B.②中的下层溶液为碘的四氯化碳溶液 |
C.溶液 中 中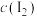 <溶液 <溶液 中 中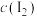 |
D.向①所得浊液中加入 ,使 ,使 增大,反应i平衡逆向移动,析出I2 增大,反应i平衡逆向移动,析出I2 |
您最近一年使用:0次
2024-05-28更新
|
30次组卷
|
2卷引用:北京市中国人民大学附属中学朝阳学校2023-2024学年高二下学期第一次统练 化学试题
名校
解题方法
3 . 体积相同,浓度均为 的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是
的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是
 的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是
的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是选项 | 试剂Ⅰ | 试剂Ⅱ |
A | 氨水 | 硫酸铜溶液 |
B |  溶液 溶液 |  溶液 溶液 |
C |  溶液 溶液 | NaOH溶液 |
D | KOH溶液 | 酸性 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列事实中,不能用勒夏特列原理解释的是
①在含有 的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
② ,工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾
,工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾
③实验室常用排饱和食盐水的方法收集氯气
④恒温恒压的容器中有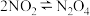 ,若通入Ar,气体的颜色先变浅后逐渐加深
,若通入Ar,气体的颜色先变浅后逐渐加深
⑤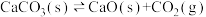 ,平衡时将容器的体积缩小至一半,新平衡的
,平衡时将容器的体积缩小至一半,新平衡的 浓度与原平衡相同
浓度与原平衡相同
⑥由 (g)、
(g)、 (g)和HI(g)组成的平衡体系加压后颜色变深
(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500℃时比室温更有利于合成氨的反应
⑧将混合气体中的氨液化有利于合成氨反应
①在含有
 的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去②
 ,工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾
,工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾③实验室常用排饱和食盐水的方法收集氯气
④恒温恒压的容器中有
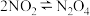 ,若通入Ar,气体的颜色先变浅后逐渐加深
,若通入Ar,气体的颜色先变浅后逐渐加深⑤
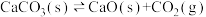 ,平衡时将容器的体积缩小至一半,新平衡的
,平衡时将容器的体积缩小至一半,新平衡的 浓度与原平衡相同
浓度与原平衡相同⑥由
 (g)、
(g)、 (g)和HI(g)组成的平衡体系加压后颜色变深
(g)和HI(g)组成的平衡体系加压后颜色变深⑦500℃时比室温更有利于合成氨的反应
⑧将混合气体中的氨液化有利于合成氨反应
| A.①②⑥⑧ | B.①③⑥⑧ | C.⑤⑥⑦ | D.②③⑦⑧ |
您最近一年使用:0次
名校
5 . 已知CH4-CO2重整制氢的主要反应如下:
反应Ⅰ:

反应Ⅱ:

反应Ⅲ: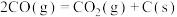

 下,将
下,将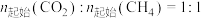 的混合气体置于密闭容器中时,在不同温度下重整体系中CH4和CO2的平衡转化率如右图所示(T2>T1)。下列说法正确的是
的混合气体置于密闭容器中时,在不同温度下重整体系中CH4和CO2的平衡转化率如右图所示(T2>T1)。下列说法正确的是
反应Ⅰ:


反应Ⅱ:


反应Ⅲ:
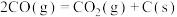

 下,将
下,将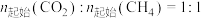 的混合气体置于密闭容器中时,在不同温度下重整体系中CH4和CO2的平衡转化率如右图所示(T2>T1)。下列说法正确的是
的混合气体置于密闭容器中时,在不同温度下重整体系中CH4和CO2的平衡转化率如右图所示(T2>T1)。下列说法正确的是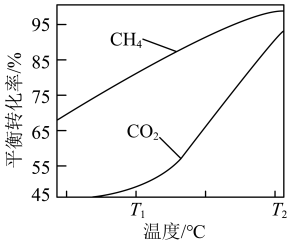
A.由图可知 |
| B.向重整体系中通入适量的H2O(g),不能减少C(s)的生成 |
| C.选择合适的催化剂可以提高T1时CH4的平衡转化率 |
D.相对 时, 时, 温度下 温度下 和 和 的转化率接近的主要原因是从 的转化率接近的主要原因是从 到 到 反应Ⅱ变化幅度大于反应Ⅲ变化幅度 反应Ⅱ变化幅度大于反应Ⅲ变化幅度 |
您最近一年使用:0次
名校
6 . 在 催化作用下发生反应:
催化作用下发生反应: 。其反应的机理如下图所示。下列说法不正确的是
。其反应的机理如下图所示。下列说法不正确的是
 催化作用下发生反应:
催化作用下发生反应: 。其反应的机理如下图所示。下列说法不正确的是
。其反应的机理如下图所示。下列说法不正确的是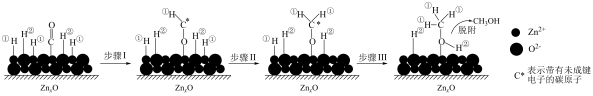
A.吸附在 上的H带正电荷 上的H带正电荷 |
| B.步骤Ⅰ、Ⅱ、Ⅲ均吸收能量 |
C.该过程中有s—  键的形成 键的形成 |
D.合成 过程中不断分离出 过程中不断分离出 ,有利于平衡正向移动 ,有利于平衡正向移动 |
您最近一年使用:0次
名校
7 . 下列实验目的、实验操作及现象与对应结论都正确的是
选项 | 实验目的 | 实验操作及现象 | 结论 |
A | 检验蔗糖是否水解 | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 ,无砖红色沉淀 ,无砖红色沉淀 | 蔗糖未发生水解 |
B | 探究镁和铝的金属活泼性 | 向盛有浓 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 | 金属活泼性: 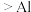 |
C | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 | 增大氢离子浓度,平衡向生成 的方向移动 的方向移动 |
D | 探究在相同条件下 和 和 的溶解度大小 的溶解度大小 | 向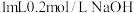 溶液中滴入2滴 溶液中滴入2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同条件下,溶解度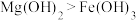 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 下列实验方案或装置能达到目的的是
| 选项 | 目的 | 实验方案或装置 |
| A | 定量测量化学反应速率 |
|
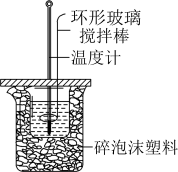
| B | 测定酸碱中和热 |
|
| C | 探究浓度影响化学平衡移动的因素 | 水煤气的反应C(s)+H2O(g) CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有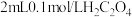 溶液的试管中分别加入 溶液的试管中分别加入 和 和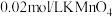 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . N2(g)+3H2(g) 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
| A.①④ | B.①②③⑤ | C.②③⑤ | D.③④ |
您最近一年使用:0次
名校
解题方法
10 . 反应 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
A. 位于元素周期表 位于元素周期表 区 区 |
B.反应过程中, 参与反应,降低了反应的焓变 参与反应,降低了反应的焓变 |
C.该反应的平衡常数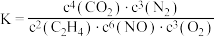 |
D.其他条件不变时,增大 , ,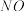 的平衡转化率下降 的平衡转化率下降 |
您最近一年使用:0次