解题方法
1 . 下列实验操作和现象与所得实验结论一致的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向 溶液中滴入几滴浓 溶液中滴入几滴浓 ,溶液橙色加深 ,溶液橙色加深 |  转化为 转化为 |
| B | 向含有少量 的 的 溶液中加入足量MgO粉末,搅拌一段时间后过滤 溶液中加入足量MgO粉末,搅拌一段时间后过滤 | 可除去 溶液中少量 溶液中少量 |
| C | 分别测定浓度均为 的 的 和 和 溶液的pH,后者大于前者 溶液的pH,后者大于前者 | 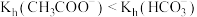 |
| D | 向2mL浓度均为 的NaCl、NaI的混合溶液中滴入2mL 的NaCl、NaI的混合溶液中滴入2mL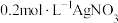 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 将 放入密闭的真空容器中,反应
放入密闭的真空容器中,反应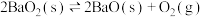 达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同
达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同
 放入密闭的真空容器中,反应
放入密闭的真空容器中,反应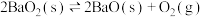 达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同
达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同| A.保持温度和体积不变,充入一定量的氧气 |
B.保持温度和体积不变,加入一定量的 |
| C.保持温度不变,缩小容器的体积 |
| D.保持体积不变,升高温度 |
您最近一年使用:0次
名校
3 . 由下列生产或实验事实得出的相应结论不正确的是
| 事实 | 结论 | |
| A | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
| B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
| C | 在容积可变的密闭容器中发生反应:2NH3(g)⇌N2H4(l)+H2(g),把容积的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
| D | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
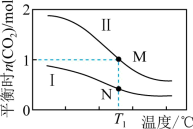
4 . 两个容积均为2 L的密闭容器Ⅰ和Ⅱ中充入NO和CO气体,发生反应:
 ,各物质的起始物质的量见表。实验测得两容器在不同温度下达到平衡时
,各物质的起始物质的量见表。实验测得两容器在不同温度下达到平衡时 的物质的量如图所示。下列说法正确的是
的物质的量如图所示。下列说法正确的是

 ,各物质的起始物质的量见表。实验测得两容器在不同温度下达到平衡时
,各物质的起始物质的量见表。实验测得两容器在不同温度下达到平衡时 的物质的量如图所示。下列说法正确的是
的物质的量如图所示。下列说法正确的是
| 容器 | 起始物质的量 | |
| NO | CO | |
| Ⅰ | 1 mol | 3 mol |
| Ⅱ | 2 mol | 6 mol |
A.M、N两点容器内的压强: |
| B.N点的平衡常数为0.08 |
C.若将容器Ⅰ的容积改为1 L, 温度下达到平衡时NO的转化率为25% 温度下达到平衡时NO的转化率为25% |
D.图中M点所示条件下,再通入CO、 各2 mol,此时v(正)<v(逆) 各2 mol,此时v(正)<v(逆) |
您最近一年使用:0次
名校
5 . 在密闭容器中的一定量混合气体发生反应:xA(s)+yB(g) zC(g)+wD(g),平衡时测得C的浓度为0.50mol·L-1,保持温度不变,将容器的容积压缩到原来的
zC(g)+wD(g),平衡时测得C的浓度为0.50mol·L-1,保持温度不变,将容器的容积压缩到原来的 ,再达平衡时,测得C的浓度升高为0.80mol·L-1。下列有关判断正确的是
,再达平衡时,测得C的浓度升高为0.80mol·L-1。下列有关判断正确的是
 zC(g)+wD(g),平衡时测得C的浓度为0.50mol·L-1,保持温度不变,将容器的容积压缩到原来的
zC(g)+wD(g),平衡时测得C的浓度为0.50mol·L-1,保持温度不变,将容器的容积压缩到原来的 ,再达平衡时,测得C的浓度升高为0.80mol·L-1。下列有关判断正确的是
,再达平衡时,测得C的浓度升高为0.80mol·L-1。下列有关判断正确的是| A.增加A的量平衡正向移动 | B.x+y<z+w |
| C.D的浓度增大 | D.B的转化率减小 |
您最近一年使用:0次
2022-11-04更新
|
73次组卷
|
2卷引用:海南省文昌中学2022-2023学年高二上学期第一次月考化学试题
6 . 一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g) ΔH=-196.0 kJ。mol-1,测得反应的相关数据如下,下列说法正确的是
2SO3(g) ΔH=-196.0 kJ。mol-1,测得反应的相关数据如下,下列说法正确的是
 2SO3(g) ΔH=-196.0 kJ。mol-1,测得反应的相关数据如下,下列说法正确的是
2SO3(g) ΔH=-196.0 kJ。mol-1,测得反应的相关数据如下,下列说法正确的是| 容器1 | 容器2 | 容器3 | |
| 应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol SO2、1mol O2 | 4mol SO3 | 2 mol SO3 |
| 平衡v正(SO2)/mol•L-1•S-1 | v1 | v2 | v3 |
| 平衡c(SO3)/mol•L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 反应能量变化 | 放出a KJ | 吸收b KJ | 吸收c KJ |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2>2c1 | B.K1>K3,p2>2p3 |
| C.v1<v3,a+c>196.0 | D.c2>2c3,α2(SO3 )+α1(SO2 )=1 |
您最近一年使用:0次
名校
7 . 将一定量的氨基甲酸铵置于恒容密闭容器中,发生反应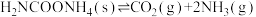 ,下列不能说明反应达到平衡的是
,下列不能说明反应达到平衡的是
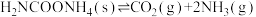 ,下列不能说明反应达到平衡的是
,下列不能说明反应达到平衡的是| A.混合气体的密度保持不变 | B.混合气体的平均摩尔质量保持不变 |
| C.二氧化碳体积分数保持不变 | D.混合气体的压强保持不变 |
您最近一年使用:0次
名校
8 . 工业制硫酸中的一步重要反应是SO2在400~500℃下发生的催化氧化反应2SO2+O2 2SO3,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,则下列有关说法错误的是
2SO3,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,则下列有关说法错误的是
 2SO3,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,则下列有关说法错误的是
2SO3,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,则下列有关说法错误的是| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.达到平衡时,SO2的浓度与SO3的浓度一定相等 |
| C.为了提高SO2的转化率,可适当提高SO2的浓度 |
| D.在上述条件下,SO2不可能100%地转化为SO3 |
您最近一年使用:0次
9 . 溶液 中存在以下平衡:
中存在以下平衡:
 。分别在
。分别在 ℃、
℃、 ℃恒温条件下,向100mL
℃恒温条件下,向100mL 的
的 溶液中加入等量
溶液中加入等量 固体(加入的固体完全溶解),持续搅拌下用pH传感器连续测量溶液的pH,得到实验图象。下列说法正确的是
固体(加入的固体完全溶解),持续搅拌下用pH传感器连续测量溶液的pH,得到实验图象。下列说法正确的是

 中存在以下平衡:
中存在以下平衡:
 。分别在
。分别在 ℃、
℃、 ℃恒温条件下,向100mL
℃恒温条件下,向100mL 的
的 溶液中加入等量
溶液中加入等量 固体(加入的固体完全溶解),持续搅拌下用pH传感器连续测量溶液的pH,得到实验图象。下列说法正确的是
固体(加入的固体完全溶解),持续搅拌下用pH传感器连续测量溶液的pH,得到实验图象。下列说法正确的是
A. |
B. 时平衡常数的数量级是 时平衡常数的数量级是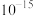 |
C.溶液中 |
D. 温度下,加入 温度下,加入 固体再次达到平衡后, 固体再次达到平衡后,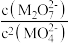 增大 增大 |
您最近一年使用:0次
名校
10 . 相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如下图。

下列说法不正确的是

下列说法不正确的是
A.由图1可知,Cl2溶于NaCl溶液时还发生了反应Cl2+Cl-=Cl |
B.随NaCl溶液浓度增大,Cl2+H2O H++Cl-+HClO平衡逆移,Cl2溶解度减小 H++Cl-+HClO平衡逆移,Cl2溶解度减小 |
| C.随盐酸浓度增加Cl2与H2O的反应被抑制,生成Cl3-为主要反应从而抑制Cl2溶解 |
| D.由上述实验可知,H+浓度增大促进 Cl2溶解,由此推知在稀硫酸中,随硫酸浓度增大Cl2的溶解度会增大 |
您最近一年使用:0次



