名校
解题方法
1 . 探究溶液中Ag+与单质S的反应。
资料:Ag2S不溶于6mol/L盐酸,Ag2SO3和Ag2SO4在6mol/L盐酸中均发生沉淀的转化
实验Ⅰ.在注射器中将10mL0.04mol/LAgNO3溶液(pH≈6)与0.01g S粉混合,水浴加热,充分反应后,过滤,得到无色溶液a(pH≈1),沉淀除S、洗涤后得到黑色固体b。
(1)研究黑色固体b的组成
①根据S具有__________ 性,推测b中可能含有Ag2S、Ag、Ag2SO3或Ag2SO4。
②检验黑色固体b的成分______ 。
ⅱ.用滤液c继续实验证明了黑色固体b中不含Ag2SO3,可选择的试剂是______ (填序号)。
a.酸性KMnO4溶液 b.H2O2和BaCl2的混合溶液 c.溴水
ⅲ.进一步实验证实了黑色固体b中不含Ag。根据沉淀e含有Ag、气体含有H2S,写出同时生成Ag和H2S的离子方程式:_________________ 。
(2)研究无色溶液a的组成
结合上述实验结果,分析溶液a中可能存在 或H2SO3,依据是
或H2SO3,依据是_______________ 。___________________ 。
②加入足量稀盐酸的作用是_________________ 。
(3)在注射器中进行实验Ⅳ,探究Ag2SO4溶液与S的反应,所得产物与实验Ⅰ相同。向注射器中加入的物质是__________________ 。
(4)用酸化的NaNO3溶液(pH≈6)与S进行实验Ⅴ,发现二者不反应。综合以上实验,写出溶液中Ag+与S反应的离子方程式并简要说明Ag+的作用:_______________ 。
资料:Ag2S不溶于6mol/L盐酸,Ag2SO3和Ag2SO4在6mol/L盐酸中均发生沉淀的转化
实验Ⅰ.在注射器中将10mL0.04mol/LAgNO3溶液(pH≈6)与0.01g S粉混合,水浴加热,充分反应后,过滤,得到无色溶液a(pH≈1),沉淀除S、洗涤后得到黑色固体b。
(1)研究黑色固体b的组成
①根据S具有
②检验黑色固体b的成分
实验Ⅱ.
ⅱ.用滤液c继续实验证明了黑色固体b中不含Ag2SO3,可选择的试剂是
a.酸性KMnO4溶液 b.H2O2和BaCl2的混合溶液 c.溴水
ⅲ.进一步实验证实了黑色固体b中不含Ag。根据沉淀e含有Ag、气体含有H2S,写出同时生成Ag和H2S的离子方程式:
(2)研究无色溶液a的组成
结合上述实验结果,分析溶液a中可能存在
 或H2SO3,依据是
或H2SO3,依据是实验Ⅲ.
②加入足量稀盐酸的作用是
(3)在注射器中进行实验Ⅳ,探究Ag2SO4溶液与S的反应,所得产物与实验Ⅰ相同。向注射器中加入的物质是
(4)用酸化的NaNO3溶液(pH≈6)与S进行实验Ⅴ,发现二者不反应。综合以上实验,写出溶液中Ag+与S反应的离子方程式并简要说明Ag+的作用:
您最近一年使用:0次
解题方法
2 . 废电池中含磷酸铁锂,提锂后的废渣主要含 、
、 和金属铝等,以废渣为原料制备电池级
和金属铝等,以废渣为原料制备电池级 的一种工艺流程如下。
的一种工艺流程如下。 、
、 均难溶于水。
均难溶于水。
ii.将 转化为
转化为 有利于更彻底除去
有利于更彻底除去 。
。
(1)酸浸前,将废渣粉碎的目的是________ 。
(2)从平衡移动的角度解释加入硝酸溶解 的原因:
的原因:________ 。
(3)在酸浸液中加入 进行电解,电解原理的示意图如下图所示,电解过程中
进行电解,电解原理的示意图如下图所示,电解过程中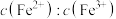 不断增大。结合电极反应说明
不断增大。结合电极反应说明 在电解中的作用:
在电解中的作用:________ 。 。向“氧化”后的溶液中加入HCHO,加热,产生NO和
。向“氧化”后的溶液中加入HCHO,加热,产生NO和 ,当液面上方不再产生红棕色气体时,静置一段时间,产生
,当液面上方不再产生红棕色气体时,静置一段时间,产生 沉淀。阐述此过程中HCHO的作用:
沉淀。阐述此过程中HCHO的作用:________ 。
(5)过滤得到电池级 后,滤液中主要的金属阳离子有
后,滤液中主要的金属阳离子有________ 。
(6)磷酸铁锂-石墨电池的总反应: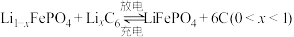 。
。
①高温条件下, 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成CO和
,同时生成CO和 ,反应的化学方程式是
,反应的化学方程式是________ 。
②放电时负极的电极反应式是________ 。
 、
、 和金属铝等,以废渣为原料制备电池级
和金属铝等,以废渣为原料制备电池级 的一种工艺流程如下。
的一种工艺流程如下。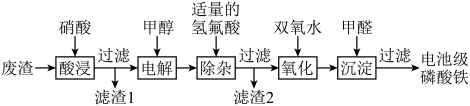
 、
、 均难溶于水。
均难溶于水。ii.将
 转化为
转化为 有利于更彻底除去
有利于更彻底除去 。
。(1)酸浸前,将废渣粉碎的目的是
(2)从平衡移动的角度解释加入硝酸溶解
 的原因:
的原因:(3)在酸浸液中加入
 进行电解,电解原理的示意图如下图所示,电解过程中
进行电解,电解原理的示意图如下图所示,电解过程中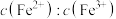 不断增大。结合电极反应说明
不断增大。结合电极反应说明 在电解中的作用:
在电解中的作用: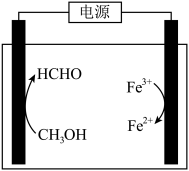
 。向“氧化”后的溶液中加入HCHO,加热,产生NO和
。向“氧化”后的溶液中加入HCHO,加热,产生NO和 ,当液面上方不再产生红棕色气体时,静置一段时间,产生
,当液面上方不再产生红棕色气体时,静置一段时间,产生 沉淀。阐述此过程中HCHO的作用:
沉淀。阐述此过程中HCHO的作用:(5)过滤得到电池级
 后,滤液中主要的金属阳离子有
后,滤液中主要的金属阳离子有(6)磷酸铁锂-石墨电池的总反应:
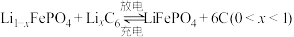 。
。①高温条件下,
 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成CO和
,同时生成CO和 ,反应的化学方程式是
,反应的化学方程式是②放电时负极的电极反应式是
您最近一年使用:0次
3 . 下列事实能用平衡移动原理解释的是
| A.合成氨工业中使用铁触媒作催化剂 |
B.铁钉放入浓 中不再变化后,加热能产生大量红棕色气体 中不再变化后,加热能产生大量红棕色气体 |
C.氯碱工业中阳极区的溶液用盐酸调pH为2~3,促进 的产生 的产生 |
D.锌片与稀 反应过程中,加入少量 反应过程中,加入少量 固体,促进 固体,促进 的产生 的产生 |
您最近一年使用:0次
名校
4 . 资料表明Co2+还原性很弱,某小组同学为实现 ,进行如下探究。
,进行如下探究。
(1)理论分析:氧化半反应 一般很难发生。从平衡移动的角度来看,降低c(Co3+)或
一般很难发生。从平衡移动的角度来看,降低c(Co3+)或_______ 均能促进Co2+失电子,提高其还原性。
【实验】①
②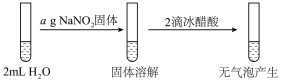
已知:ⅰ. ,
, ;
;
ⅱ.HNO2不稳定,易分解: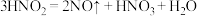
(2)②是①的对照实验,目的是_______ 。
(3)经检验,橙红色溶液中存在 。经分析,①中能实现
。经分析,①中能实现 的原因是Co3+形成配离子,且
的原因是Co3+形成配离子,且 的氧化性被提高。
的氧化性被提高。
a.解释Co3+能与 形成配位键的原因:
形成配位键的原因:_______ 。
b.结合还原半反应解释 的氧化性被提高的原因:
的氧化性被提高的原因:_______ 。
【实验Ⅱ】
③
④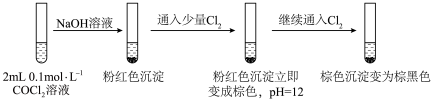
已知:Co(OH)2 (粉红色)和Co(OH)3 (棕黑色)的Ksp分别是10-14.2和10-43.8。
(4)对比③④可知,本实验条件下还原性:Co(OH)2_______ Co2+ (填“>”或“<”)。
(5)分析④中能实现 的原因:
的原因:
a.该条件下,Co2+的还原性同时受“c(Co3+)降低”和“c(Co2+)降低”的影响,前者影响更_______ (填“大”或“小”)。
b.当c(Co2+):c(Co3+)>1014时,Co2+能被Cl2氧化。结合Ksp计算,④中通入少量Cl2后溶液c(Co2+):c(Co3+)=_______ ,因此能实现转化。
(6)实验启示:通常情况下,为促进低价金属阳离子向高价转化,可将高价阳离子转化为_______ 或_______ 。
 ,进行如下探究。
,进行如下探究。(1)理论分析:氧化半反应
 一般很难发生。从平衡移动的角度来看,降低c(Co3+)或
一般很难发生。从平衡移动的角度来看,降低c(Co3+)或【实验】①

②

已知:ⅰ.
 ,
, ;
;ⅱ.HNO2不稳定,易分解:
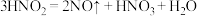
(2)②是①的对照实验,目的是
(3)经检验,橙红色溶液中存在
 。经分析,①中能实现
。经分析,①中能实现 的原因是Co3+形成配离子,且
的原因是Co3+形成配离子,且 的氧化性被提高。
的氧化性被提高。a.解释Co3+能与
 形成配位键的原因:
形成配位键的原因:b.结合还原半反应解释
 的氧化性被提高的原因:
的氧化性被提高的原因:【实验Ⅱ】
③

④

已知:Co(OH)2 (粉红色)和Co(OH)3 (棕黑色)的Ksp分别是10-14.2和10-43.8。
(4)对比③④可知,本实验条件下还原性:Co(OH)2
(5)分析④中能实现
 的原因:
的原因:a.该条件下,Co2+的还原性同时受“c(Co3+)降低”和“c(Co2+)降低”的影响,前者影响更
b.当c(Co2+):c(Co3+)>1014时,Co2+能被Cl2氧化。结合Ksp计算,④中通入少量Cl2后溶液c(Co2+):c(Co3+)=
(6)实验启示:通常情况下,为促进低价金属阳离子向高价转化,可将高价阳离子转化为
您最近一年使用:0次
名校
解题方法
5 . 某实验小组同学用KSCN探究久置FeSO4固体变质的情况。将0.3gFeSO4固体用10mL蒸馏水溶解,配成待测液,进行实验。
【初步实验】
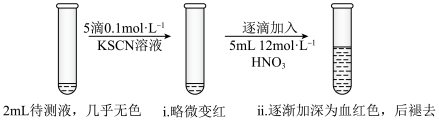
(1)用KSCN检验Fe3+的原理是___________ (用离子方程式表示)。
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被___________ (填化学式)氧化。结合平衡移动原理解释ⅱ中血红色褪去的可能原因___________ 。
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是___________ 。
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
(4)请补全步骤Ⅱ中的操作:___________ 。
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是___________ (填字母序号)。
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有___________ (至少2条)。
【初步实验】

(1)用KSCN检验Fe3+的原理是
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
| 步骤 | 操作 | 现象 |
| Ⅰ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,再加入5mL浓KNO3溶液 | 溶液无明显变化 |
| Ⅱ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,___________ | 溶液变为红色 |
| Ⅲ | 向Ⅱ中所得溶液中逐滴加入浓硝酸,边加边振荡 | 溶液逐渐加深为血红色,继续滴加浓硝酸,溶液褪色,pH变化始终不明显 |
(4)请补全步骤Ⅱ中的操作:
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有
您最近一年使用:0次
名校
解题方法
6 . 下列实验能达到实验目的的是
| A | B |
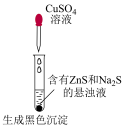 | 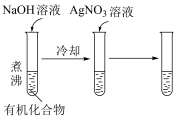 |
比较相同温度下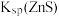 和 和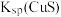 的大小 的大小 | 检验有机化合物中含溴原子 |
| C | D |
 | 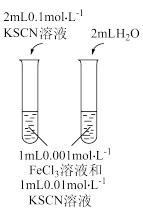 |
| 探究干燥的氯气是否具有漂白性 | 研究浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 某兴趣小组将4g铁钉放入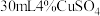 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
①CuSCN:白色固体,不溶于水;
②室温下,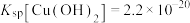 ,
, ,
, 。
。
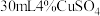 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是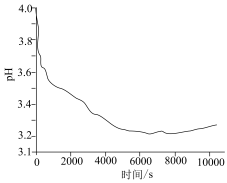
①CuSCN:白色固体,不溶于水;
②室温下,
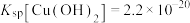 ,
, ,
, 。
。A. 溶液 溶液 的原因是 的原因是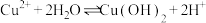 |
B.0~6000s,随着反应进行,溶液pH下降的原因可能是 被 被 氧化为 氧化为 |
C.反应后期溶液pH略有上升的可能原因是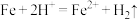 |
D.溶液先变红后又褪色的可能原因是 的反应速率快, 的反应速率快,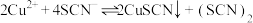 的反应限度大 的反应限度大 |
您最近一年使用:0次
2024-02-29更新
|
115次组卷
|
3卷引用:北京市第一七一中学2023-2024学年高三下学期开学考试化学试题
23-24高三下·北京·开学考试
名校
解题方法
8 . 下列方程式不正确 的是
A.用稀 清洗银镜: 清洗银镜: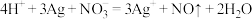 |
B.氢氧化亚铁露置在空气中变为红褐色: |
C.向苯酚钠溶液中通入 ,溶液变浑浊:2 ,溶液变浑浊:2  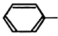 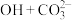 |
D.向 溶液中滴加少量硫酸,溶液橙色加深: 溶液中滴加少量硫酸,溶液橙色加深: |
您最近一年使用:0次
9 . 下列事实不能用平衡移动原理解释的是
A. 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| B.实验室用排饱和食盐水的方法收集氯气 |
C.工业合成氨:  ,采用400℃~500℃的高温条件 ,采用400℃~500℃的高温条件 |
D.工业制备 : :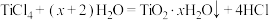 ,加入大量水,同时加热 ,加入大量水,同时加热 |
您最近一年使用:0次
2024-01-24更新
|
102次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末考试化学试题
名校
10 . 某同学为探究浓度对化学平衡的影响设计了如下实验:已知:
反应i:
反应ii: (黄色)
(黄色)不正确 的是
反应i:

反应ii:
 (黄色)
(黄色)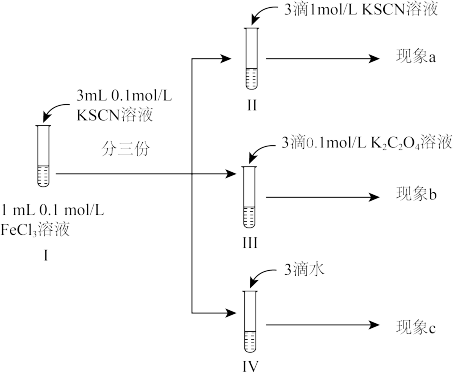
| A.观察到现象a比现象c中红色更深,即可证明增加反应物浓度,反应i平衡正向移动 |
| B.观察到现象b比现象c中红色浅,即可说明反应i平衡逆向移动,反应ⅱ平衡正向移动 |
| C.进行IV对比实验的主要目的是防止出于溶液体积变化引起各离子浓度变化而干扰实验结论得出 |
D.III中溶液一开始无 ,12小时后检出 ,12小时后检出 ,可能的原因是 ,可能的原因是 还原 还原 的速率较慢,反应ⅱ速率较快 的速率较慢,反应ⅱ速率较快 |
您最近一年使用:0次
2023-01-06更新
|
344次组卷
|
4卷引用:北京市人大附中2023-2024学年高二下学期期中考试化学试题



