解题方法
1 . 二氧化碳催化加氢合成乙烯的热化学方程式为
 ,恒压条件下,按
,恒压条件下,按 进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是

 ,恒压条件下,按
,恒压条件下,按 进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
A.图中曲线b表示平衡时 的物质的量分数随温度的变化 的物质的量分数随温度的变化 |
B.M点 的平衡转化率为60% 的平衡转化率为60% |
C.保持其他条件不变,在绝热密闭容器中发生上述反应,达到平衡时, 的物质的量分数比在恒温密闭容器中的低 的物质的量分数比在恒温密闭容器中的低 |
D.440K时反应达平衡后,保持其他条件不变,再向容器中按 投料,再次平衡时, 投料,再次平衡时, 的物质的量分数为0.39 的物质的量分数为0.39 |
您最近一年使用:0次
2 . 已知气相直接水合法制取乙醇的反应为H2O(g)+C2H4(g)  CH3CH2OH(g)。在容积为3L的密闭容器中,当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图所示:
CH3CH2OH(g)。在容积为3L的密闭容器中,当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图所示:
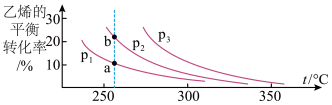
下列说法正确的是
 CH3CH2OH(g)。在容积为3L的密闭容器中,当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图所示:
CH3CH2OH(g)。在容积为3L的密闭容器中,当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图所示:
下列说法正确的是
| A.a、b两点平衡常数:b=a |
| B.压强大小顺序: P1>P2>P3 |
| C.当混合气的密度不变时反应达到了平衡 |
D.其他条件不变,增大起始投料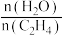 ,可提高乙烯转化率 ,可提高乙烯转化率 |
您最近一年使用:0次
名校
3 .  和
和 存在平衡:
存在平衡: 。下列分析正确的是
。下列分析正确的是
 和
和 存在平衡:
存在平衡: 。下列分析正确的是
。下列分析正确的是A. 平衡混合气体中含N原子大于 平衡混合气体中含N原子大于 |
| B.恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
C.恒容时,充入少量 ,平衡正向移动导致气体颜色变浅 ,平衡正向移动导致气体颜色变浅 |
D.断裂 中的共价键所需能量大于断裂 中的共价键所需能量大于断裂 中的共价键所需能量 中的共价键所需能量 |
您最近一年使用:0次
2022-05-05更新
|
614次组卷
|
4卷引用:湖南省怀化市沅陵县第一中学2022届高三下学期第四次模拟考试化学试题
名校
4 . 对于反应2CO(g)+2NO(g)=N2(g)+2CO2(g),下列说法正确的是
A.反应的平衡常数可表示为K=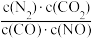 |
| B.使用催化剂可降低反应的活化能,减小反应的焓变 |
| C.增大压强能加快反应速率,提高反应物的平衡转化率 |
| D.用E总表示键能之和,该反应ΔH=E总(生成物)-E总(反应物) |
您最近一年使用:0次
名校
5 . 在固定容积的密闭容器中,按 与
与 的物质的量之比为1∶3进行投料,发生反应
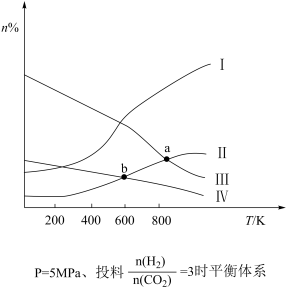
的物质的量之比为1∶3进行投料,发生反应 ,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表
,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表 。下列说法正确的是
。下列说法正确的是
 与
与 的物质的量之比为1∶3进行投料,发生反应
的物质的量之比为1∶3进行投料,发生反应 ,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表
,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表 。下列说法正确的是
。下列说法正确的是
A.图中曲线交点a、b对应的平衡常数 |
B.图中曲线交点b对应的 转化率为40% 转化率为40% |
| C.平衡时,向体系中加入氢气,氢气转化率变大 |
D.若其他条件相同,甲为恒温恒容,乙为绝热恒容,达到平衡时 产率:甲>乙 产率:甲>乙 |
您最近一年使用:0次
2022-03-24更新
|
586次组卷
|
6卷引用:湖南省怀化市沅陵县第二中学2021-2022学年高三下学期四月第一次调研考试化学试题
湖南省怀化市沅陵县第二中学2021-2022学年高三下学期四月第一次调研考试化学试题(已下线)2022年河北省新高考测评卷(七)(已下线)2022年湖南卷高考真题变式题(11-14)江西省南昌市第二中学2022-2023学年高三上学期第四次考试化学试题广东省广州市第二中学2022-2023学年高三 上学期(11月25日)周测化学试题天津市第二十五中学2022 -2023学年高二上学期期中考试化学试题
名校
6 . 在一密闭容器中反应aA(g) bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.6mol/L,则下列说法不正确的是
bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.6mol/L,则下列说法不正确的是
 bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.6mol/L,则下列说法不正确的是
bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.6mol/L,则下列说法不正确的是| A.平衡向正反应方向移动 | B.物质A的转化率增大 |
| C.物质B的质量分数增大 | D.a>b |
您最近一年使用:0次
2017-02-17更新
|
474次组卷
|
3卷引用:2017届湖南省怀化市高三上学期期中质检化学试卷
7 . 在一容积为2 L的密闭容器内加入0.2 mol 的N2和0.6 mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
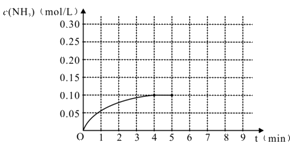
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为_________________ 。
(2)该反应的化学平衡常数表达式K=___________________ 。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________ 。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡_________________________ 移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________________ (填“增大”、“减小”或“不变”)。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。___________________
 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为
(2)该反应的化学平衡常数表达式K=
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
您最近一年使用:0次



